- Преподавателю
- Физика
- Конспект по физике на тему Молекулалық физика және термодинамика негіздері
Конспект по физике на тему Молекулалық физика және термодинамика негіздері
| Раздел | Физика |
| Класс | 9 класс |
| Тип | Конспекты |
| Автор | Кенесариева Ж.Ж. |
| Дата | 08.01.2016 |
| Формат | docx |
| Изображения | Есть |
«Өрлеу» біліктілікті арттыру ұлттық орталық АҚ филиалы облысы бойынша педагогикалық қызметкерлерді білімін арттыру институты
Курс 26.05-04.06.2014ж
Тақырыбы:
Физика пәні мұғалімдерінің кәсіптік шеберліктерін жетілдірудің
технологиялық әдіс-тәсілдері
Курстық жұмыс:
Термодинамика тарауы бойынша есептерді шығару және
теориялық мәселелерді бөлісу
Тексерген: Дуйсенбаев Б.
Орындаган: Кенесариева Ж.Ж
Ақтау - 2014 жыл
Жоспар
-
Кiрiспе.
1.1 Молекулалык физика. Термодинамика негiздерi туралы түсiнiк.
-
Негiзгi бөлiм.
2.1 Жылулық тепе-теңдiк, абсолют температура.
2.2 Термодинамика заңы, жылу двигательдері және жұмыс iстеу принциптерi.
-
Корытынды.
3.1 Термодинамика тарауын оқытудың маңызы.
Молекулалық физика және термодинамика негіздері
Жылу құбылыстары тарауына берілген есептерді шешу энергияның сақталу және айналу заңына негізделеді. Бұл жерде денелердің ішкі энергиясының өзгеруінің формулалары және механиканың кейбір теңдеулері ескеріледі. Басты қиыншылық энергияның сақталу заңын нақты физикалық процестерге қолдану болып табылады. Бұл жерде жылу мөлшері мен ішкі энергияның өзгерісі арасындағы айырмашылыққа және негізгі теңдеу құрылатын денелер жүйесін (немесе денені) таңдап алуға ерекше назар аударылуы тиіс.
Ішкі энергияның өзгеруіне берілген есептерді үш топқа бөлуге болады. Бірінші топ есептерінде оқшауланған жүйеде денелер өзара әсерлескенде олардың тек ішкі энергиясы ғана өзгеретін, бірақ сыртқы ортамен жұмыс істелмейтін құбылыстар қарастырылады. Бұл кезде жылу алмасуға қатысатын денелердің біреулері салқындайды, қалғандары - қызады. Термодинамиканың бірінші заңына сәйкес ішкі энергиясы кемитін денелер үшін былай жазуға болады:
Q_бер= ∆U_(1 )+ ∆U_2 + ⋯ + ∆U_n = ∑_(i=1)^n▒〖∆U_i 〗, (1)
Осыған ұқсас ішкі энергиясы артатын денелер үшін
Q_ал = ∆U_1^' + ∆U_2^' + ⋯ + ∆U_m^' = ∑_(k=0)^m▒〖∆U_k^' 〗 (2)
Жылу мөлшерінің түсінігінің анықтамасынан және энергияның сақталу заңынан салдар ретінде мына қатынасты алуға болады:
∑▒〖∆U=0〗 (3)
Соңғы теңдеу термодинамиканың бірінші бастамасының өзінен өзі көрініп тұрған салдары болып табылады - тек ғана жылу берілу процестері өтетін оқшауланған денелер жүйесінде, жүйенің ішкі энергиясы өзгермейді, яғни жекелеген денелердің энергиясының өзгерістерінің алгебралық қосындысы нольге тең болады.
Q_бер=〖 Q〗_ал түріндегі теңдеу жылу балансының теңдеуі деп аталады, ол бірінші топтың барлық есептерінің басты есептеу қатынасы болып табылады.
Бірінші топтың есептері төмендегідей тәртіппен шығарылады:
а) Есептің шартын оқып, қандай денелердің ішкі энергиясының кеміп, қайсыларының ішкі энергиясы артатындығын анықтау керек. Жылу алмасу процесінде агрегаттық өзгерулер бола ма, болмай ма - осыған мұқият назар аудару қажет.
б) Энергиясы кемитін денелер үшін (1), ал энергиясы артатын денелер үшін (2) теңдеулерді құрып, алынған қосындыларды бір біріне теңестіру керек.
Кейбір есептерде жылу алмасудың ПӘК-і беріледі ; бұл жағдайда оны көбейткіш ретінде Q_бер мүшесінің алдына қою керек.
Жылу алмасуға берілген барлық есептерде, арнайы ескертулер болмаса, барлық өзара әсерлесетін денелердің жылу өткізгіштігі шексіз үлкен және энергияның бір денеден келесісіне берілуі лезде жүреді деп есептеледі.
Екінші топтың есептерінде екі дененің өзара әсерлесуі кезінде энергияның бір түрден келесісіне айналуымен байланысты құбылыстар қарастырылады.Бұндай өзара әсерлесудің нәтижесі бір дененің ішкі энергиясының осы дененің жұмыс атқаруымен немесе осы денемен жұмыс атқарумен байланысты өзгеруі болып табылады. Бұл жерде денелер арасындағы жылу алмасу ескерілмейді.
Энергияның сақталу және айналу заңының теңдеуі бұл жағдайда былай жазылады:
Q = ∆U+A (4)
Бұндай есептерді шығаруды келесі схема бойынша жүргізген ыңғайлы.
а) Есептің шартын талдап, ең әуелі екі өзара әсерлесетін дененің қайсысының ішкі энергиясы өзгереді және осы өзгерудің себебі не - дененің атқаратын жұмысы ма әлде денемен істелінетін жұмыс па - осыны анықтап алу керек. Осыдан басқа денелердің өзара әсерлесу процесінде оларға жылу сырттан берілмей ме, яғни, шындығында, Q = 0 - осыған көз жеткізіп алу керек.
б) Ішкі энергиясы өзгеретін дене үшін 4 - теңдеуді жазу керек, бұл жерде жұмыстың алдындағы таңба және қарастырылып отырған процестің ПӘК-і ескерілуі керек. ПӘК-ін ескере отырып 4 - теңдеуді жазғанда былай істеген ыңғайлы. Егер есептің мазмұны бойынша жұмыс денелердің біреуінің ішкі энергиясының кемуі есебінен жасалса, және қайсыбір себептерге байланысты осы энергияның тек бөлігі ғана жұмыстың жасалуына жұмсалса, онда
A= η∆U (4')
Егер есептің шарты бойынша дененің ішкі энергиясы денемен жасалған жұмыс есебінен артса және қайсыбір себептерге бола осы жұмыстың тек бөлігі ғана жұмыстың жасалуына жұмсалса, онда
η∙A = ∆U (4'')
в) 4- теңдеуді құрып, A және ∆U шамаларының өрнектерін табу керек.
Жұмыс A шамасы үшін келесі қатынастардың біреуі мүмкін бола алады:
A = Fs;
A = Nτ;
A = W_2-W_1
Ішкі энергияның өзгерісі ∆U шамасы үшін көбіне келесі формулалардың біреуін пайдаланған жеткілікті:
∆U = qm - отынның жануы;
∆U = cm∆t+ λm - денені қыздыру және оның балқуы;
∆U = cm∆t+ rm - қыздыру және булану.
Бастапқы теңдеуге A және ∆U шамаларының өрнектерін қойып, белгісіз шаманы анықтау үшін қорытынды қатынасты аламыз.
Үшінші топтың есептері алғашқы екі топтың есептерін біріктіреді. Бұл есептерде үш және одан да көп денелердің өзара әсерлесуі қарастырылады. Бұндай өзара әсерлесу процесінде денелердің біреуіне қайсыбір жылу мөлшері беріледі де оның ішкі энергиясы өзгереді және жұмыс істеледі.
Бұл есептерді шешу үшін энергияның сақталуы мен айналу заңының толық теңдеуі құрылады.
Идеал газдың күйін сипаттайтын негізгі теңдеу Менделеев - Клапейрон теңдеуі болып табылады. Газдың қарастырылатын күйлерінің әрқайсысы үшін осы теңдеуді құрып және қосымша шарттарды формулалар түрінде жазып, кез келгенге дерлік есепті салыстырмалы түрде жеңіл шешуге болады. Алайда бұл әдіс кейбір жағдайларда шешуді күрделендіреді және құбылыстың физикалық мәнін аз түсіндіретін артық математикалық есептеулерге әкеледі.
Осыны ескере отырып,газдардың күйінің параметрлерін табуға арналған есептерді екі негізгі топқа бөлуге болады. Біріншісіне массасы тұрақты газдың екі немесе бірнеше күйлері қарастырылатын есептерді жатқызуға болады, оларға pV/T = const түріндегі біріккен газ заңының теңдеуін қолдануға болады.
Екінші топты шартында газдың массасы берілген немесе газдың массасы өзгеретін процестер қарастырылатын есептер қамтиды. Бұл есептерді шешкенде біріккен газ заңын пайдалануға болмайды, Менделеев - Клапейрон теңдеуін қолдану керек.
Изохоралық және изобаралық процесте газды қыздыруға және газдың жұмысына берілген есептерді шешу термодинамиканың бірінші заңына және
A = p (V_2 - V_1) = p∆V,
A = m/M R( T_2-T_1) = m/M R∆T
формулаларына негізделген.
Егер есептің шарты бойынша газдың екі күйі берілсе және газ бір күйден келесісіне өткенде оның массасы өзгермесе, онда есепті шығару үшін төмендегідей тізбекті ұсынуға болады:
а) Есептің шартын оқып, қандай газдың қандай процеске қатысып тұрғандығын анықтап, газдың күйінің параметрлері өзгерген кезде оның массасының тұрақты болып қалатындығына көз жеткізу керек.
б) Егер мүмкін болса, газдың әрбір күйін белгілеп схемалық чертеж жасап, онда осы күйлерін сипаттайтын p,V,T параметрлерін көрсету керек. Есептің шартынан осы үшеуінің қайсысының өзгермейтіндігін, айнымалы параметрлердің қандай газ заңына бағынатындығын анықтау керек. Жалпы жағдайда p,V және T параметрлерінің барлығы да өзгере алады.
в) Берілген екі күй үшін Клапейронның біріккен газ заңының теңдеуін жазу керек. Егер қандай да бір параметр өзгермесе, теңдеу Бойль- Мариотт, Гей- Люссак және Шарль заңдарын өрнектейтін үш теңдеудің біреуіне автоматты түрде ауысады.
г) Барлық көмекші шарттарды математикалық түрде жазып, алынған теңдеулер жүйесін белгісіз шамаға қатысты шешу керек.
Есептер шығару
-
Массасы 128г латуннан жасалған калориметрде 0,4°С - тағы масса 240г су бар. Оған 100°С-қа дейін қыздырылған массасы 192 г металл дене салынған. Калориметрдегі соңғы орныққан температура 21,5 °С. Зерттелетін дененін меншікті жылу сыйымдылығын анықтау керек.
Шешуі: Жылу алмасуға үш дене қатысады: калориметр, су және металл. Ал металл жылу мөлшерін береді. Су мен калориметр жылу алады. Жылу байланысының формуласын құрамыз:
Q3=Q1+Q2 (1) мұнда Q1=ΔU1=C1m1(T-T1).,
Q2=ΔU2=c2m2(T-T2) - калориметр мен судың алған жылу мөлшері.
Q3=ΔU3=c3m3(T3 - T) - дененің берген жылу мөлшері.
Бірінши формулаға осы шамаларды қоямыз.
c3m3(T3-T)=c1m1(T - T1)+c2m2( T - T1)
будан с3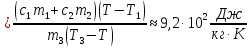
-
Теңіз түбінен бетіне жеткенше ауа көпіршігінің көлемі 3 есе көбейеді. Теңіздің терендігі қандай?
Берілгені: V2 = 3 V1
Табу керек: h=?
Шешуі:
Теніздің барлық терендігінде судың температурасы тұрақты деп есептейміз. Олай болса Бойль-Мариот заңы бойынша: P1V1= P2V2 мұнда P1, P2 теңіз тубіндегі және жер бетіндегі ауа көпіршігінің қысымы, V1, V2 теңіз түбі мен бетіндегі көпіршіктің көлемі.
Көрініп тұрғандай теңіз бетіндегі ауа көпіршігінің P2 қысымы P0 атмосфералық қысымға тең болады, яғни сонда P1, V1 = 3Р0. Теңіз түбіндегі қысым ΔР = Р1 - Р0=3Р0 - Р0= 2Р0
Гидростатикадан білетініміздей ΔР=ρgh
ρ-судың тығыздығы, h-теңіз терендігі.
Соңғы екі тендеудің оң жақтарын теңестіріп, алатынымыз 2P0= ρgh бұдан
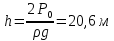
-
Көлемі 240 м2, температурасы 15°С және қысымы - 10°Па бөлмеде қанша ауаның молекуласы бар?
Шешуі: Ауа массасының өзгерісін берілген ( P1, V1, T1) және қалыпты
( P0, V0, T0) жағдайда салыстырамыз. Сонда 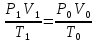
(1)
Қалыпты жағдайда ауа көлемі V=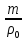 болғандықтан
болғандықтан 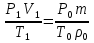 cонда
cонда 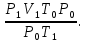 Берілген массада қанша моль бар екенін анықтаймыз.
Берілген массада қанша моль бар екенін анықтаймыз.
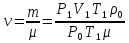 ,
, 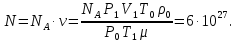
-
Бөлмедегі ауаның көлемі 100 м3 . Егер атмосфералық қысым 12кПа және температура 10°С - тан 25°С - қа дейін қыздырғанда бөлмеден қанша ауа массасы шығады.
Шешуі: ауа массасының өзгерісін берілген ( P, V, T) және қалыпты
( P0, V0, T0) жағдайында қарастырамыз,
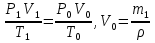 олай болса
олай болса 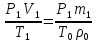 осыдан
осыдан 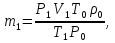 температура артқанда көлем мен қысым өзгермейді, бірақ масса өзгереді m2, болады.
температура артқанда көлем мен қысым өзгермейді, бірақ масса өзгереді m2, болады.
Осы m2 масса өзгерісін берілген ( P1, V1, T1) және қалыпты ( P0, V0, T0) жағдайда қарастырамыз. 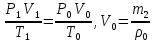 бұдан
бұдан 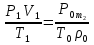 сонда m2 =
сонда m2 =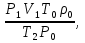
Бұдан ізделініп отырған ауа массасын табуға болады.
Δm=m1 - m2 = 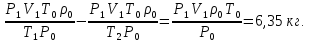
-
Ауданы 100 см2 цилиндирде ауа бар. Поршень цилиндр түбінен 50 см биікте түр. Поршенге массасы 50 кг жүк қояды. Сонда ол 10 см төмен түскен. Егер ол төмендегенге дейін қысым 101 кПа ал температурасы 12°С болса, ауа температурасы поршень төмендегенде қандай болған.
Шешуі: Ауа поршень төмен түспегенге дейін және түскеннен кейінгі ауа өзгерісі P1, V1, T1 параметрлерімен сипатталады. Поршень төмен түскен соң, P2, V2, T2 параметрмен сипатталады.
Мұнда, 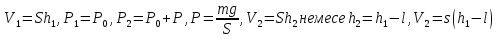 осы екі жағдайда Менделеев - Клайперон тендеуін қолданамыз.
осы екі жағдайда Менделеев - Клайперон тендеуін қолданамыз.
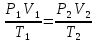 осыдан T2 =
осыдан T2 = 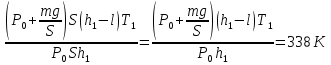
Қорытынды.
Жалпы «Термодинамика» бөлiмiн өту барысында оқушылар практикалық сипаттағы дағдылар мен бiлiмдер жүйесiн: дене температурасын, атмосфералық қысымды (барометр-анероидпен), газ қысымын (манометр көмегiмен) өлшеудi, жылу мөлшерiн есептеу, газ күйiн сипаттайтын негiзгi параметрлер арасындағы байланыс графигiн салуды,газ күйiнiң тендеуi негiзiнде идеал газ температурасын,көлемiн және қысымын есептейтiн есептердi шығара бiлудi меңгеру керек.
Физиканы оқытудың ең басты мiндеттерiнiң бiрi - ұғымдар жүйесiн қалыптастыру болып табылады.
Тарауды оқыту процесінде оқушылар салыстырмалы ылғалдылықты өлшейтiн кұралдармен (гигрометр жане психрометр), өлшеу әдiстерiмен танысады да, теориялык бiлiмдi өмiрде пайдалану бiлу дағдысы қалыптаcады.
Пайдаланылған әдебиеттер.
-
Физика информатика журналы 2000ж
-
Физика 10-сынып. Б. Кронгарт. В.Кем. Н. Қойшыбаев
-
Физика және Астрономия. Рауан 1999 ж.
-
В. А. Балаш «Задачи по физике и методы их решение»


