- Преподавателю
- Физика
- Практическая работа по физике «Решение задач на определение электрохимического эквивалента»
Практическая работа по физике «Решение задач на определение электрохимического эквивалента»
| Раздел | Физика |
| Класс | - |
| Тип | Конспекты |
| Автор | Кокуйская Н.В. |
| Дата | 16.12.2014 |
| Формат | doc |
| Изображения | Есть |
Инструкционно-технологическая карта
на выполнение практической работы № 11
по дисциплине «ФИЗИКА»
Тема: «Электрический ток в различных средах»
Наименование работы: «Решение задач на определение электрохимического эквивалента».
Цель работы: закрепить знания студентов по данной теме, умения решать задачи на расчёт электрохимического эквивалента применяя законы Фарадея.
Ход работы
1. Теоретическая часть
1 закон Фарадея. В 1832 году Фарадей установил, что масса M вещества, выделившегося на электроде, прямо пропорциональна электрическому заряду Q, прошедшему через электролит:
![]()
если через электролит пропускается в течение времени t постоянный ток с силой тока I.
Коэффициент пропорциональности k называется электрохимическим эквивалентом вещества. Он численно равен массе вещества, выделившегося при прохождении через электролит единичного электрического заряда, и зависит от химической природы вещества.
2 закон Фарадея. Электрохимические эквиваленты различных веществ относятся, как их химические эквиваленты.
Химическим эквивалентом иона называется отношение молярной массы М иона к его валентности n. Поэтому электрохимический эквивалент
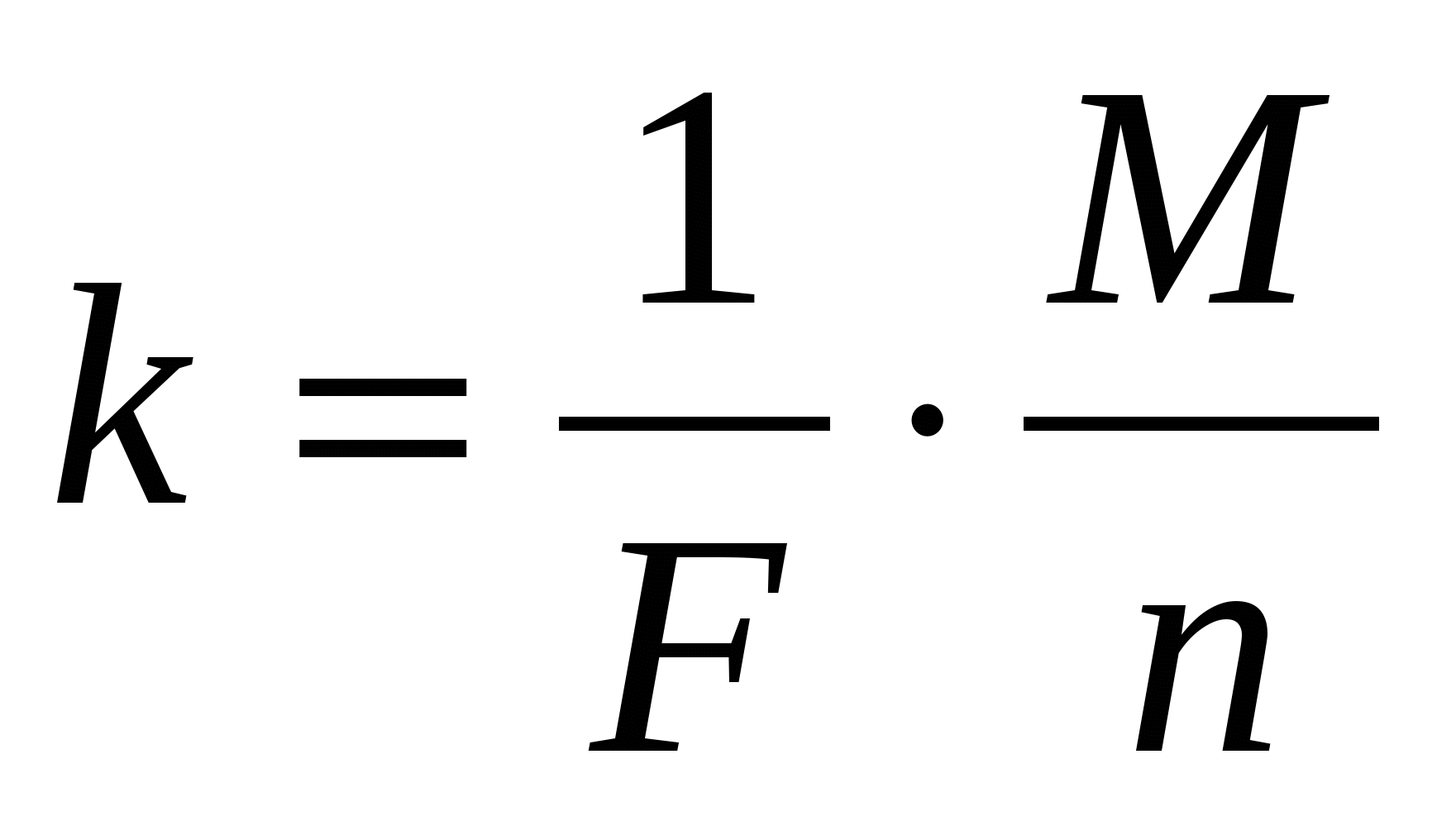
где F - постоянная Фарадея, F = 9,65∙10-4Кл/моль
Физический смысл F- численно равна заряду, который надо пропустить через раствор электролита, чтобы выделить на электроде 1 моль одновалентного вещества.
2. Практическая часть
Совместное решение задачи:
Для серебрения 12 ложек (площадь поверхности каждой 50 см2) через раствор соли серебра пропускается ток. Толщина покрытия должна составить 50 мкм. В течение какого времени должно проходить серебрение при силе тока 1,3 А? Молярная масса серебра 0,108 кг/моль, валентность 1, плотность 10,5 •103 кг/м3.
Решение задач в группах.
Задачи
№1. При серебрении изделия пользовались током 5А в течение 15 мин. Какое количество серебра израсходовано за это время?
№2. При каком токе протекал электролиз в растворе медного купороса, если за 5 мин на катоде выделилось 6 г меди?
№3. Какой разряд должен пройти через раствор сернокислой меди, чтобы на катоде отложилось 6,58 г меди?
№4. За сколько времени полностью израсходуется медный анод, размеры которого 100*50*2 (мм3), при условии. Что ток в ванне 3,0 А?
№5. При электрическом способе получения никеля расходуется 10кВт энергии на 1 кг. Электрохимический эквивалент никеля 3*10-7 кг/Кл.
№6. Сколько алюминия выделятся при затрате 1 кВт/ч электрической энергии, если электролиз ведется при напряжении 5,0 В. КПД установки 80%?
№7. Найдите электрохимический эквивалент 30г железа, если при электролизе за 8 мин по проводу протекает ток силой 10мА.
3. Справочный материал
Таблица Электрохимический эквивалент, мг/Кл или  10-4 кг/Кл
10-4 кг/Кл
Вещество
Валентность
k
Алюминий
3
0,0932
Бром
1
0,8282
Водород
1
0,01045
Железо
3
0,1929
Золото
3
0,6812
Кислород
2
0,0829
Медь
1
0,6588
Медь
2
0,3294
Натрий
1
0,2383
Никель
2
0,3041
Никель
3
0,2027
Олово
2
0,6150
ОН-группа
1
0,1763
Платина
4
0,5058
Ртуть
1
2,0789
Свинец
2
1,0736
Сера
2
0,1661
Серебро
1
1,1179
Хлор
1
0,3674
Цинк
2
0,3388
Приложение к практической работе № 11
«Решение задач на определение электрохимического эквивалента».
Ответы к задачам для самостоятельного решения
№ задачи
Ответ
1
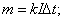 m=0,005кг .
m=0,005кг .
2
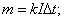
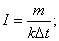 I=60,6 A
I=60,6 A
3
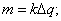
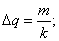
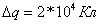
4
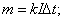
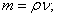
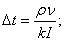
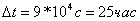
5
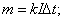
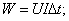
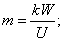
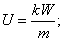 U=10,8B
U=10,8B
6
![]()
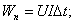
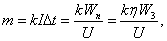 m=0,054 кг.
m=0,054 кг.
7
m=kIt , k=m/(It), 0.00625 кг/Кл = 6.25 г/Кл


