- Преподавателю
- Физика
- «Первый закон термодинамики. Применение первого закона термодинамики к изопроцессам»
«Первый закон термодинамики. Применение первого закона термодинамики к изопроцессам»
| Раздел | Физика |
| Класс | - |
| Тип | Конспекты |
| Автор | Зайцева Е.Ю. |
| Дата | 27.02.2014 |
| Формат | doc |
| Изображения | Есть |
Конспект урока по теме «Первый закон термодинамики.
Применение первого закона термодинамики к изопроцессам».
10 класс, учитель Коваль Н.А.
Задачи урока: 1 установить связь между изменением внутренней энергии системы,
работой и количеством теплоты, сообщенным систематизиро-
вать и углубить знания учащихся об изопроцессах;
2 научить учащихся экспериментальным путем определять изменение
внутренней энергии тела;
3 воспитывать внимание, аккуратность, умение работать в паре.
Оборудование: приборы для фронтальной лабораторной работы (пробирка с пробкой,
термометр лабораторный, стакан с водой, лист бумаги, таблица
«Удельная теплоемкость веществ»), проектор, ноутбук.
Ход урока.
-
Подготовка к восприятию нового материала.
-
Фронтальный опрос:
-
а) Дать определение внутренней энергии.
б) Способы изменения внутренней энергии.
в) Как определить работу газа при его расширении?
г) Какой геометрический смысл имеем работа?
д) Газ, занимающий объем V, и имеющий давление Р, расширяется до объема V1 один раз изобарно, другой раз - изотермически. В каком случае работа расширения газа больше? Докажите ответ графически.
е) Что называют количеством теплоты?
ж) Что показывает удельная теплоемкость вещества?
и) Найдите по таблице удельную теплоту плавления свинца; что это значит?
к) Что обладает большей внутренней энергией: кипящая вода или пар? На сколько? Ответ пояснить
2. Фронтальный эксперимент «Вычисление изменения внутренней энергии тела при совершении работы».
Порядок выполнения работы.
1.Налейте в пробирку 10 мл воды и измерьте ее температуру.
2. Закройте пробирку пробкой и заверните в бумагу. Энергично встряхивайте воду в
пробирке в течение 30-40с
3.Откройте пробирку и снова измерьте температуру воды.
4.Вычислите изменение внутренней энергии воды.
5. Результаты измерений и вычислений запишите в тетрадь.
6. Ответьте на вопросы:
- как изменилась внутренняя энергия воды во время опыта?
- каким способом вы изменяли внутреннюю энергию воды в опыте?
- зачем пробирку с водой необходимо было заворачивать в бумагу во время
опыта?
- что можно сказать о зависимости изменения внутренней энергии тела от совер-
шенной работы?
-
Изучение нового материала.
Итак, нагревание тела может происходить не только при теплообмене, но и при совершении работы. В больших масштабах такое явление наблюдал в 1798 г. Б. Румфорд. При сверлении пушечного ствола, которое производили с помощью лошадей, вращавших большое сверло, Румфорд успевал вскипятить поставленный на ствол котел с водой. Румфорд предположил, что вода нагревается в процессе совершаемой при сверлении работы. Используя сухие кусочки дерева можно добыть огонь, т.е. нагреть дерево до температуры, превышающей температуру его воспламенения.
Значит, работа, как и количество теплоты является мерой изменения энергии системы
Первый закон термодинамики указывает на способы изменения внутренней энергии. В общем случае при переходе системы из одного состояния в другое внутренняя энергия изменяется одновременно как за счет совершения работы, так и за счет передачи теплоты.
Задание уч-ся: выпишите из учебника (стр. 221-222) формулировку и формулу первого закона термодинамики и проанализируйте ее.
Вопросы
1.Чем отличается работа газа от работы внешних сил?
2. Как изменится формула 1 закона термодинамики, если работу будет совершать газ?
3. Попробуйте дать новую формулировку закона.
4. Как этот закон объясняет невозможность создания вечного двигателя первого рода?
Промежуточное закрепление знаний.
-
На рисунке схематично показаны случаи изменения внутренней энергии ( тело получает или отдает тепло, совершает работу или работа совершается над ним). Используя уравнение первого закона термодинамики, запишите формулу для расчета внутренней энергии в каждом случае
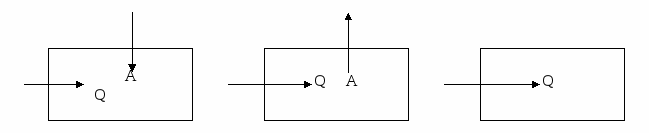
-
Газ находится в сосуде под давлением 2,5 * 104Па. При сообщении ему количества теплоты 6 * 104 Дж он изобарно расширился на 2 м3. На сколько изменилась внутренняя энергия газа? Как изменилась его температура?
Изучение нового материала.
С помощью первого закона термодинамики можно делать важные заключения о характере протекающих процессов. Рассмотрим процессы протекающие с идеальным газом.
Вопросы:
-
Что называется изопроцессом?
-
Какие изопроцессы вы знаете?
-
Какой процесс называется изотермическим? Изохорным? Изобарным?
Задание: работая с п. 81, заполнить таблицу.
Название процесса
График
Изменение внутренней энергии.
Работа газа.
Запись закона.
Физический смысл записи закона.
Изохорный
V
P
P= const
Н агревание
агревание
Q
Q> 0
Охлаждение
Q < 0
Q

V
ΔU > 0
ΔU < 0
А = 0
А = 0
ΔU = Q
ΔU = - Q
Внутренняя энергия газа увеличивается за счет подводимого тепла.
Внутренняя энергия газа уменьшается за счет того, что газ отдает тепло окружающей среде.
Изотермический Т = const
P
Расширение
А > 0 Q > 0
> 0 Q > 0
P
Q

V
Сжатие
A

V
Q< 0 Q< 0
ΔU = 0
ΔU = 0
A > 0
A < 0
Q = A газа
Aвн.сил = - Q
Все переданное газу тепло идет на совершение им же работы.
При совершении работы внешними силами газ отдает тепло внешней среде.
Изобарный
Р = const
Нагревание (расширение)
Aг > 0 Q > 0


P
V

P
V

Q
Q
ΔU > 0
∆U < 0
Aг > 0
Aг < 0
Q = ΔU+Aг
∆U = -Aг-Q
Подводимое к газу тепло идет на увеличение его внутренней энергии и на совершение газом работы.
Внутренняя энергия уменьшается за счет того, что над газом совершается работа и газ отдает тепло окружающей среде.
А
диабатный процесс (объяснение учителя)
-
Закрепление изученного материала
1.Как формулируется закон сохранения энергии?
2. В чем состоит эквивалентность количества теплоты и механической работы?
3.Что называют первым законом термодинамики?
4.Какой процесс называется адиабатным?
Решение задач.
1.При изотермическом расширении идеальным газом совершена работа 15 кДж. Какое количество теплоты сообщено газу?
2. В закрытом сосуде находится газ. При охлаждении его внутренняя энергия уменьшилась на 500 Дж. Какое количество теплоты отдал газ? Совершил ли он работу?
3.Вычислите увеличение внутренней энергии кислорода массой 0,5 кг при изохорном повышении температуры на 15 0С.
4. Для изобарного нагревания газа, количество вещества которого 400 моль, на 300 К ему сообщили количество теплоты 5,4 МДж. Определите работу газа и приращение его внутренней энергии.
5.Подведение итога урока.
Домашнее задание. П.80, 81, стр.240 задачи 9,10.


