- Преподавателю
- Физика
- Тест Основное уравнение МКТ, уравнение состояния идеального газа 10 класс
Тест Основное уравнение МКТ, уравнение состояния идеального газа 10 класс
| Раздел | Физика |
| Класс | 10 класс |
| Тип | Тесты |
| Автор | Сигайло Г.С. |
| Дата | 20.11.2015 |
| Формат | doc |
| Изображения | Есть |
10 класс (Основное уравнение МКТ, уравнение состояния идеального газа)
Вариант 1
-
При неизменной абсолютной температуре концентрация молекул идеального газа была увеличена в 4 раза. При этом давление газа:
1. Увеличилось в 4 раза. 2. Увеличилось в 2 раза.
3. Уменьшилось в 4 раза. 4. Не изменилось.
-
При неизменной концентрации молекул гелия средняя кинетическая энергия теплового движения его молекул увеличилась в 4 раза. При этом давление газа:
1. Увеличилось в 16 раз. 2. Увеличилось в 2 раза.
3. Увеличилось в 4 раза. 4. Не изменилось.
-
При температуре 2T0 и давлении р0 количество вещества идеального газа, равного 1 моль, занимает объем V0. Каков объем идеального газа, количество вещества которого равно 2 моль, при том же давлении р0 и температуре T0?
1. 4V0. 2. 2V0. 3. V0. 4. 8V0.
-
Кислород находится в сосуде вместимостью 0,4 м3 под давлением 8,3*105 Па и при температуре 320 К. Чему равна масса кислорода?
1. 2 кг. 2. 0,4 кг. 3. 4 кг. 4. 2*10-23 кг.
-
Какова плотность воздуха (М=29*10-3 кг/моль) в камере сгорания дизельного двигателя при температуре 5030 С, если давление воздуха равно 400 кПа?
1. 1,2 кг/м3. 2. 1,5 кг/м3. 3. 1,8 кг/м3. 4. 2,1 кг/м3. 5. Данных недостаточно.
-
Если в сосуде находится смесь двух невзаимодействующих между собой газов соответственно с массами m1 и m 2 и молярными массами М1 и М2, то масса одного моля такой смеси равна
1. (m1M1+m2M2)/(m1+m2). 2. (m1+m2)M1M2/(m1M2+m2M1). 3. (m1M2+m2M1)/(m1+m2).
4. M1M2/(m1M1+m2M2). 5. M1M2/(m1M2+m2M1).

7.
8
.
Вариант 2
-
При неизменной концентрации частиц абсолютная температура идеального газа была увеличена в 4 раза. Давление газа при этом:
1. Увеличилось в 4 раза. 2. Увеличилось в 2 раза.
3. Уменьшилось в 4 раза. 4. Не изменилось.
-
При неизменной концентрации частиц идеального газа средняя кинетическая энергия теплового движения его молекул уменьшилась в 4 раза. При этом давление газа:
1. Уменьшилось в 16 раз. 2. Уменьшилось в 2 раза.
3. Уменьшилось в 4 раза. 4. Не изменилось.
-
При температуре T0 и давлении р0 идеальный газ, взятый в количестве вещества 1 моль, занимает объем V0 . Каков объем газа, взятого в количестве 2 моль, при давлении 2р0 и температуре 2T0?
1. 4V0. 2. 2V0. 3. V0. 4. 8V0.
-
Азот массой 0,3 кг при температуре 280 К оказывает давление на стеки сосуда, равное 8,3*104 Па. Чему равен объем газа?
1. 0,3 м3. 2. 3,3 м3. 3. 0,6 м3. 4. 60 м3.
-
Средняя квадратичная скорость молекул кислорода при 9270 С равна 960 м/с. Какова средняя квадратичная скорость этих молекул при температуре газа 270 С?
1. 200 м/с. 2. 824 м/с. 3. 320 м/с. 4. 480 м/с. 5. 560 м/с.
-
Если в закрытом сосуде, где находится идеальный двухатомный газ, при неизменной температуре половина молекул газа распадается на атомы, то давление газа в сосуде
1. Уменьшится в 2 раза. 2. Уменьшиться в 1,5 раза. 3. Увеличится в 1,5 раза.
4
. Увеличится в 2 раза. 5. Останется неизменным.
7.
8
.
Вариант 3
-
Средняя квадратичная скорость теплового движения молекул при уменьшении абсолютной температуры идеального газа в 4 раза:
1. Уменьшится в 16 раз. 2. Уменьшится в 2 раза.
3. Уменьшится в 4 раза. 4. Не изменится.
-
При сжатии идеального газа его объем уменьшился в 2 раза, а температура увеличилась в 2 раза. Как изменилось при этом давление газа?
1. Увеличилось в 2 раза. 2. Уменьшилось в 2 раза.
3. Увеличилось в 4 раза. 4. Не изменилось.
-
При сжатии неизменного количества газа его объем уменьшился в 2 раза, а давление увеличилось в 2 раза. Как изменилась при этом температура газа?
1. Увеличилась в 2 раза. 2. Уменьшилась в 2 раза.
3. Увеличилась в 4 раза. 4. Не изменилась.
-
В сосуде долгое время находится смесь гелия и аргона. Определите, средняя квадратичная скорость молекул какого газа больше. Молярная масса аргона больше, чем гелия.
-
Скорости одинаковы. 2. Скорость молекул аргона больше.
-
Скорость молекул гелия больше.
-
Ответ на вопрос зависит от концентрации молекул каждого газа.
-
Для того, чтобы плотность идеального одноатомного газа при неизменном давлении увеличилась в 2 раза, абсолютную температуру газа следует
1. Увеличить в 2 раза. 2. Увеличить в 4 раза. 3. Увеличить в 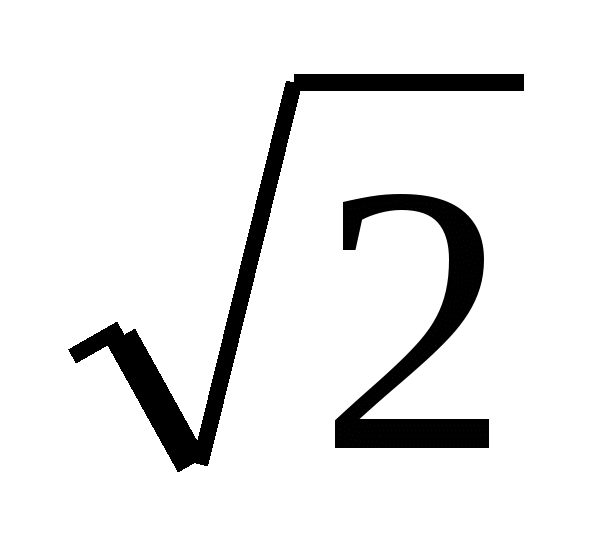 раз.
раз.
4. Уменьшить в 2 раза. 5. Уменьшить в 4 раза.
-
Если перегородку, разделяющую сосуд на две части с объемами V1 и V2, в которых находится один и тот же газ соответственно под давлениями Р1 и Р2, удалить, то в сосуде установится давление (температуру считать неизменной)
1. (P1V1-P2V2)/(V1+V2). 2. (P1V1-P2V2)/(V1-V2). 3. P1+P2.
4
. (P1V1+P2V2)/(V1+V2). 5. (P1V2+P2V1)/(V1+V2).
7.
8
.
Вариант 4
-
В результате нагревания газа средняя кинетическая энергия теплового движения его молекул увеличилась в 4 раза. Как изменилась при этом абсолютная температура газа?
1. увеличилась в 4 раза. 2. увеличилась в 2 раза.
3. уменьшилась в 2 раза. 4. не изменилась.
-
Давление идеального газа увеличилось в 2 раза, а его температура уменьшилась в 4 раза. Как изменился при этом объем газа?
1. Увеличился в 2 раза. 2. Уменьшился в 2 раза.
3. Увеличился в 8 раз. 4. Уменьшился в 8 раз.
-
Давление неизменного количества идеального газа уменьшилось в 2 раза, а его температура уменьшилась в 4 раза. Как изменился при этом объем газа?
1. Увеличился в 2 раза. 2. Уменьшился в 2 раза.
3. Увеличился в 8 раз. 4. Уменьшился в 8 раз.
-
Каково давление воздуха (М=29*10-3 кг/моль) в камере сгорания дизельного двигателя при температуре 5030 С, если плотность воздуха равна 1,8 кг/м3?
1. 400 кПа. 2. 4*106 Па. 3. 40 кПа. 4. 4000 Па. 5. 40 Па.
-
Какова средняя квадратичная скорость движения молекул газа, если, имея массу 6,1 кг, он занимает объем 5 м3 при давлении 2*105 Па?
1. 500 м/с. 2. 400 м/с. 3. 700 м/с. 4. 900 м/с. 5. 600 м/с.
-
Если в баллоне находится 50 кг идеального газа под давлением 10 Мпа, а затем при неизменной температуре давление в баллоне упало до 3 Мпа, то это означает, что из баллона выпустили … газа.
1. 7 кг. 2. 21 кг. 3. 9 кг. 4. 35 кг. 5. 30 кг.
7
.
8
.


