- Преподавателю
- Физика
- Урок по физике на темау: «Квантовые постулаты Бора. Модель атома водорода по Бору. » (11 класс)
Урок по физике на темау: «Квантовые постулаты Бора. Модель атома водорода по Бору. » (11 класс)
| Раздел | Физика |
| Класс | 11 класс |
| Тип | Тесты |
| Автор | Ратуева Л.П. |
| Дата | 16.03.2015 |
| Формат | doc |
| Изображения | Есть |
Урок №70 Дата проведения 11___________
Тема: «Квантовые постулаты Бора. Модель атома водорода по Бору.»
Цель урока: изучить квантовые постулаты Бора, модель атома водорода Бора, показать значение теории Бора в развитии физической науки.
Ход урока:
1. Организационный момент.
2. Проверка домашнего задания и актуализация изучаемой темы.
Выберите один правильный ответ из предложенных вариантов
1. Принятая в настоящий момент в науке модель структуры атома обоснована опытами по...
-
растворению и плавлению твердых тел
-
ионизации газа
-
химическому получению новых веществ
-
рассеянию a-частиц
Ответ: 4.
2.В опыте Резерфорда a-частицы рассеиваются...
-
электростатическим полем ядра атом
-
электронной оболочкой атомов мишени
-
гравитационным полем ядра атома
-
поверхностью мишени
Ответ: 1.
3.На рисунке показаны траектории a-частиц при рассеянии их на атоме, состоящем из тяжелого положительно заряженного ядра Z+ и легкого облака электронов е -. Какая из траекторий является правильной?
-
Только 1
-
Только 2
-
И 1, и 2
-
Ни 1, ни 2
Ответ: 2 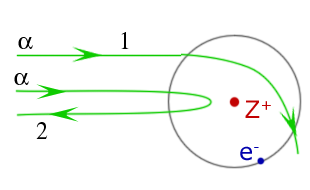
4.Какое утверждение соответствует планетарной модели атома?
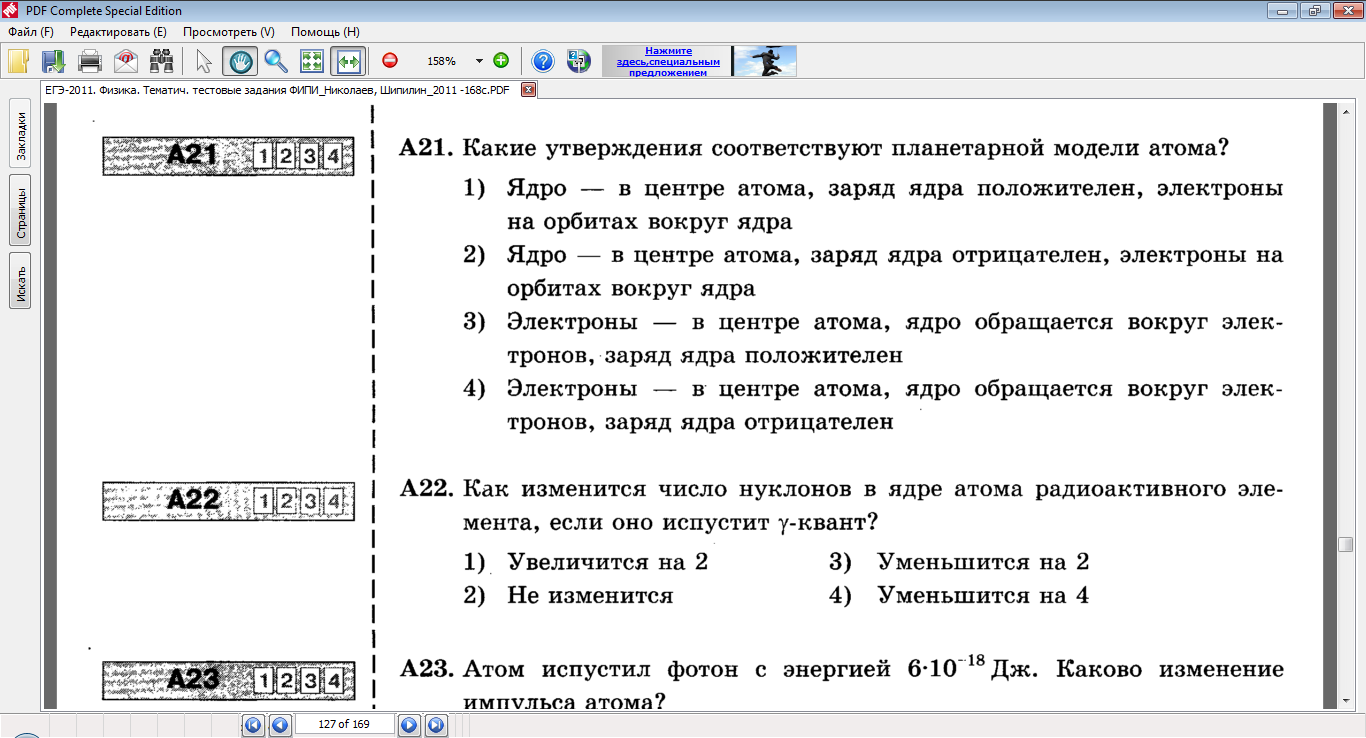



Ответ:1
5.На рисунке изображены схемы четырех атомов. Черными точками обозначены электроны. Атому 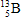 соответствует схема...
соответствует схема...
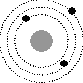
1
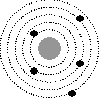
2
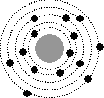
3

4
Ответ: 2.
6.Сравните массы частиц, фигурирующих в объяснении опыта Резерфорда: масса a-частицы - Мa, масса ядра атома золота МAu, масса электрона - Ме
1.
МAu » Мa>>Ме
2.
МAu>Мa>>Ме
3.
МAu>>Мa>>Ме
4.
МAu » Мa<Ме
Ответ: 3
Фронтальный опрос
- Какова была цель опыта Резерфорда? Опишите установку Резерфорда, ход эксперимента.
-Какие результаты получил Резерфорд?(Подавляющая часть альфа частиц проходила сквозь фольгу практически без отклонения или с отклонением на малые углы по отношению к направлению своего первоначального полёта. Но небольшая часть частиц отклонялась на значительные углы, достигающие почти 180°. Применив методы теории вероятностей, Резерфорд показал, что такие отклонения не могут быть следствием многократных столкновений альфа частиц с атомами, поэтому объяснить этот результат на основе модели атома Томсона невозможно.)
- Какие выводы сделал Резерфорд из опыта? (Существует атомное ядро, в котором сконцентрирована почти вся масса атома и весь положительный заряд. Вокруг ядра по замкнутым орбитам вращаются отрицательные частицы электроны.)
-- Почему большинство ученых отрицательно отнеслись к модели атома Резерфорда? (Ядерная модель атома, предложенная Резерфордом, не могла объяснить факт существования атома, точнее - его устойчивость. В соответствии с законами классической электродинамики Максвелла электроны при движении по орбитам c ускорением должны непрерывно излучать электромагнитные волны. Атом должен излучать свет и терять энергию. С потерей энергии электрон за время порядка 0.1 нс должен «упасть» на ядро, а атом прекратить своё существование. В действительности атомы излучают свет, но не исчезают при этом. Кроме того, частота вращения электрона по мере приближения к ядру будет изменяться плавно, т. е. спектр излучения атома должен быть непрерывным, а не линейчатым. Таким образом, по законам классической электродинамики атом Резерфорда должен быт неустойчивым, а его спектр излучения - непрерывным, что противоречило результатам экспериментов. Ученым пришлось признать ограниченность применения законов классической физики.)
3.Изучение нового материала
Постулаты Бора.
Первым решился на это признание выдающийся физик XX в. датский ученый Нильс Бор. В 1913 г. он с помощью гениальной интуиции сформулировал в виде постулатов основные положения новой теории.
Изучая противоречия модели атома Резерфорда и законами классической физики, Нильс Бор выдвигает постулаты, определяющие строение атома и условия испускания и поглощения им электромагнитного излучения.
Постулаты Бора показали, что атомы подчиняются законам микромира.
I постулат (постулат стационарных состояний).
Атомная система может находиться только в особых стационарных или квантовых состояниях, каждому из которых соответствует определенная энергия En. В стационарных состояниях атом не излучает энергию, при этом электроны в атомах движутся с ускорением.
Атом может находиться в стационарном состоянии сколь угодно долго.
Стационарные состояния отличаются друг от друга различными орбитами, по которым движутся электроны в атоме. Набор электронных орбит, по сути, определяет стационарные состояния электрона в атоме. Стационарные состояния можно пронумеровать, присвоив им порядковый номер n=1, 2, 3, ...,причем каждое состояние обладает своей фиксированной энергией Еn
II постулат (правило частот).
Излучение света происходит при переходе атома из стационарного состояния с большей энергией Ek в стационарное состояние с меньшей энергией En. Энергия излучённого фотона равна разности энергий стационарных состояний: 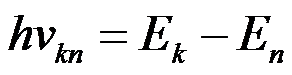
Отсюда можно выразить частоту излучения:
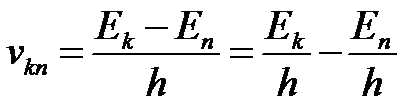
При поглощении света, атом переходит из стационарного состояния с меньшей энергией в стационарное состояние с большей энергией. При излучении атом переходит из стационарного состояния с большей энергией в стационарное состояние с меньшей энергией.
Второй постулат противоречит электродинамике Максвелла, т.к. частота излученного света свидетельствует не об особенностях движения электрона, а лишь об изменении энергии атома.
Модель атома водорода по Бору
Используя законы механики Ньютона и правило квантования, на основе которого определяются возможные стационарные состояния атома. Бор смог вычислить радиусы орбит электрона и энергии стационарных состояний атома. Минимальный радиус орбиты определяет размеры атома.
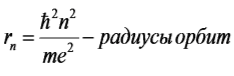
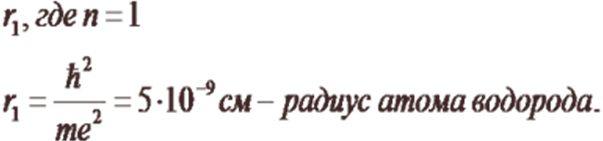
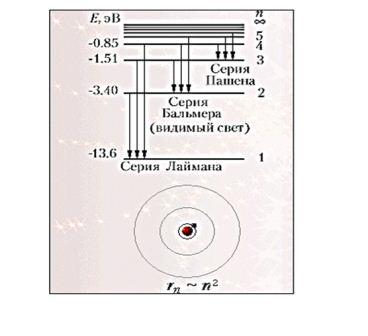
Для наглядного представления возможных энергетических состояний электрона в атоме используется энергетическая диаграмма, на которой каждому энергетическому состоянию электрона в атоме Еn соответствует горизонтальная линия - энергетический уровень. Энергетическую диаграмму можно считать своеобразной «лестницей» с «нижней площадкой» (основным состоянием) и поднимающимися вверх «ступенями» (возбужденными состояниями). Значения энергий стационарных состояний отложены на вертикальной оси (в электрон - вольтах).
Обычно атом находится в основном состоянии (в этом состоянии атома электрон движется по первой стационарной орбите) с наименьшим значением энергии, равны:
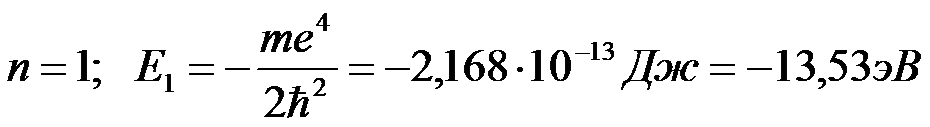
Второй постулат Бора позволяет вычислить (по известным значениям энергий стационарных состояний) частоты излучений атома водорода.
Теория Бора приводит к количественному согласию с экспериментом для значений этих частот. Все частоты излучений атома водорода составляют в своей совокупности ряд серий, каждая из которых образуется при переходах атома в одно из энергетических состояний со всех верхних энергетических состояний (состояний с большей энергией).
Переходы в первое возбужденное состояние (на второй энергетический уровень) с верхних уровней образуют серию, названную по имени швейцарского учёного серией И. Бальмера. Эти переходы изображены стрелками: красная, зеленая и две синие линии в видимой части спектра водорода (рис. V, 3 на цветной вклейке в учебнике) соответствуют переходам:Е3 - Е2 , Е4 - Е2 , Е5 - Е2 , Е6 - Е2.)

И. Бальмер еще в 1885 г. на основе экспериментальных данных вывел простую формулу для определения частот видимой части спектра водорода.
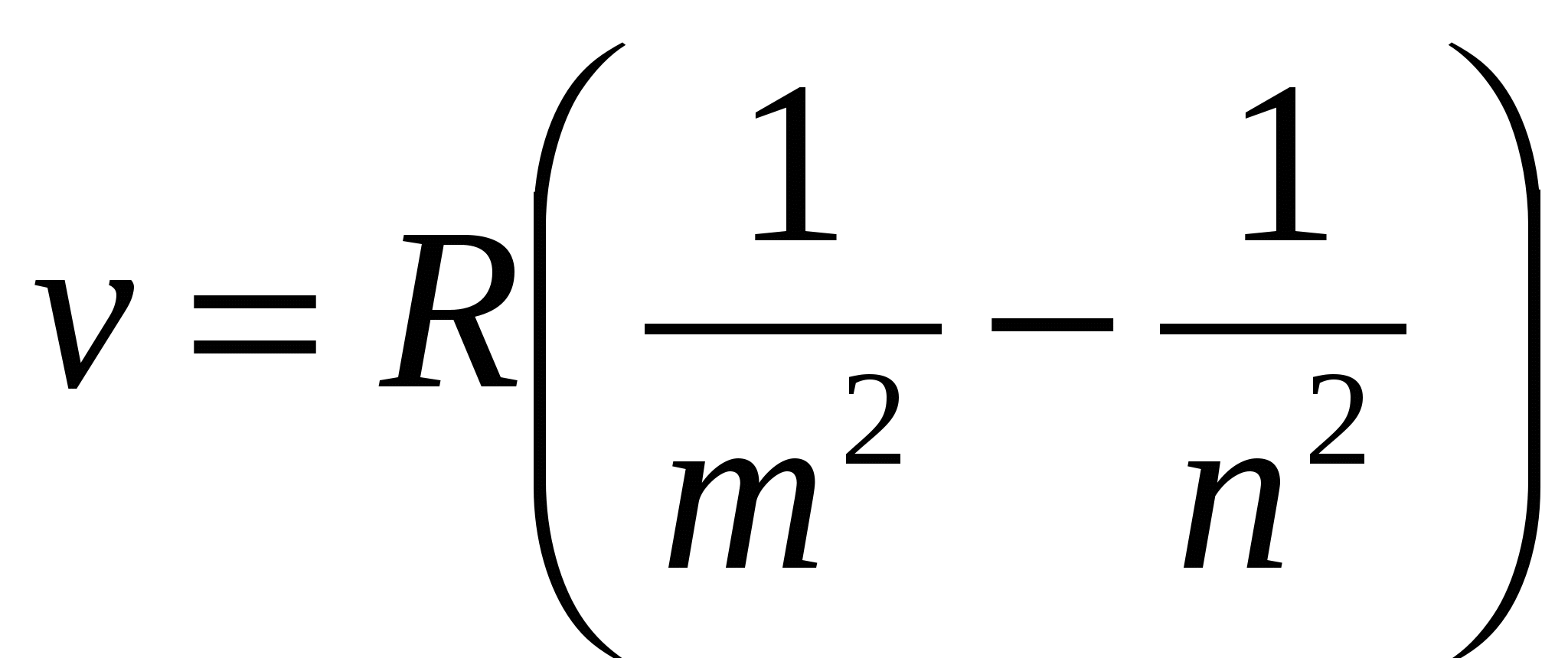
R=109737, 31 (1/ см) - постоянная Ридберга.
Поглощение света - процесс, обратный излучению. Атом, поглощая свет, переходит из низших энергетических состояний в высшие состояния. При этом он поглощает излучение той же самой частоты, которую излучает, переходя из высших энергетических состояний в низшие.
Значение постулатов Бора
Эйнштейн оценил проделанную работу Бором «как высшую музыкальность в области мысли», всегда его поражавшую.
На основе двух постулатов и правила квантования Бор определил радиус атома водорода и энергии стационарных состояний атома. Это позволило вычислить частоты излучаемых и поглощаемых атомом водорода электромагнитных волн. Теория Бора позволяет описать не только атом водорода, но и ионизированные атомы (ионы) других элементов, вокруг ядер которых, как и в атоме водорода, вращается один электрон. Такие ионы называются водородоподобными. Примерами водородоподобных ионов могут служить однократно ионизированный атом гелия (Не+), двукратно ионизированный атом лития (Li + +) и т. д.
Теория Бора явилась важным этапом в развитии квантовых представлений, введение которых в физику требовало кардинальной перестройки механики и электродинамики. Такая перестройка была осуществлена в 20-е - 30-е годы XX века, когда были созданы новые физические теории квантовая механика и квантовая электродинамика.
Однако надо помнить то, что для атомов с большим числом электронов (больше 1) расчеты по теории Бора неприменимы. Представление Бора об определенных орбитах, по которым движутся электроны в атоме, оказалось весьма условным. На самом деле движение электрона в атоме очень мало похоже на движение планет или спутников. Физический смысл имеет только вероятность нахождения электрона в том или ином месте окрестности ядра.

В настоящее время с помощью квантовой механики можно ответить практически на любой вопрос, относящийся к строению и свойствам электронных оболочек атомов. С количественным описанием электронных оболочек атомов вы познакомились в курсе химии.
4.Закрепление нового материала
- Какие затруднения вызвала модель Резерфорда для объяснения процессов излучения энергии атомами? ( Ядерная модель Резерфорда просто обосновывала экспериментальные данные, но не позволяла объяснить устройство атома исходя из классических законов физики).
- Сформулируйте первый постулат Бора.
- Сформулируйте и запишите второй постулат Бора.
- В чём заключаются противоречия между постулатами Бора и законами классической механики и классической электродинамики? (Как следует из постулатов, вопреки классической электродинамике электроны движутся по замкнутым орбитам и электромагнитные волны при этом не излучают.)
- При каком условии происходит излучение, а при каком условии происходит поглощение энергии атомом? (При поглощении света, атом переходит из стационарного состояния с меньшей энергией в стационарное состояние с большей энергией. При излучении атом переходит из стационарного состояния с большей энергией, в стационарное состояние с меньшей энергией.)
- Каково значение теории Бора в развитии физической науки? (Теория Бора явилась важным этапом в развитии квантовых представлений о строении атома. Бор определил радиус атома водорода и энергии стационарных состояний атома. Это позволило вычислить частоты излучаемых и поглощаемых атомом водорода электромагнитных волн. Теория Бора позволяет описать не только атом водорода, но и водородоподобные ионы других элементов.)
Работа с учебником: найдите в учебнике на стр.278 изображение диаграммы энергетических уровней атома водорода. Вопросы:
- На рисунке12.4,стр278 изображена диаграмма энергетических уровней атома водорода. Энергия ионизации атома равна: а)0; б)3.4эВ; в)0.54эВ; г)13.6эВ ( 13.6эВ. Энергия ионизации - энергия, которую нужно затратить для перевода электрона из основного состояния в состояние с нулевой энергией. Исходя из диаграммы, в основном состоянии электрон имеет энергию Е = -13.6эВ.)
- Сколько квантов (с различной энергией) может испускать атом водорода, если электрон находится на третьем возбужденном уровне. (Рис12.4,стр278) (атом водорода может испускать кванты с тремя различными энергиями .Возможные переходы: n=3 ---n=1,n=2--- n=1, n=3--- n=2.)
Домашнее задание: §94


