- Преподавателю
- Другое
- Урок по физике по теме Давление газа. Уравнение состояния идеального газа
Урок по физике по теме Давление газа. Уравнение состояния идеального газа
| Раздел | Другое |
| Класс | - |
| Тип | Конспекты |
| Автор | Самойлова С.А. |
| Дата | 16.02.2015 |
| Формат | doc |
| Изображения | Есть |
Урок № 75
Давление газа. Уравнение состояния идеального газа.
Цели:
Установить зависимость между параметрами, определяющими состояние газа.
Ход урока
I. Организация учебной деятельности учащихся на уроке.
Сообщение темы, цели, задач урока. Стимулирование мотивации учебной деятельности при обучении.
II. Проверка знаний и умений.
Организация самостоятельной работы.
III. Изучение нового материала.
Давление газа определяется столкновением молекул газа со стенками сосуда.
В СИ за единицу давления принимают 1 Па.
Давление, при котором на площадь 1 м2 действует сила давления в 1 Н, называется Паскалем.
1мм.рт.ст. = 133 Па
1атм = 1105 Па
Одной из основных задач молекулярно-кинетической теории газа является установление количественных соотношений между макроскопическими параметрами, характеризующими состояние газа (давлением, температурой), и величинами, характеризующими хаотическое тепловое движение молекул газа (скоростью молекул, их кинетической энергией). Одним из таких соотношений является зависимость между давлением идеального газа и средней кинетической энергией поступательного движения его молекул. Эту зависимость называют основным уравнением молекулярно-кинетической теории идеального газа:
![]() или
или 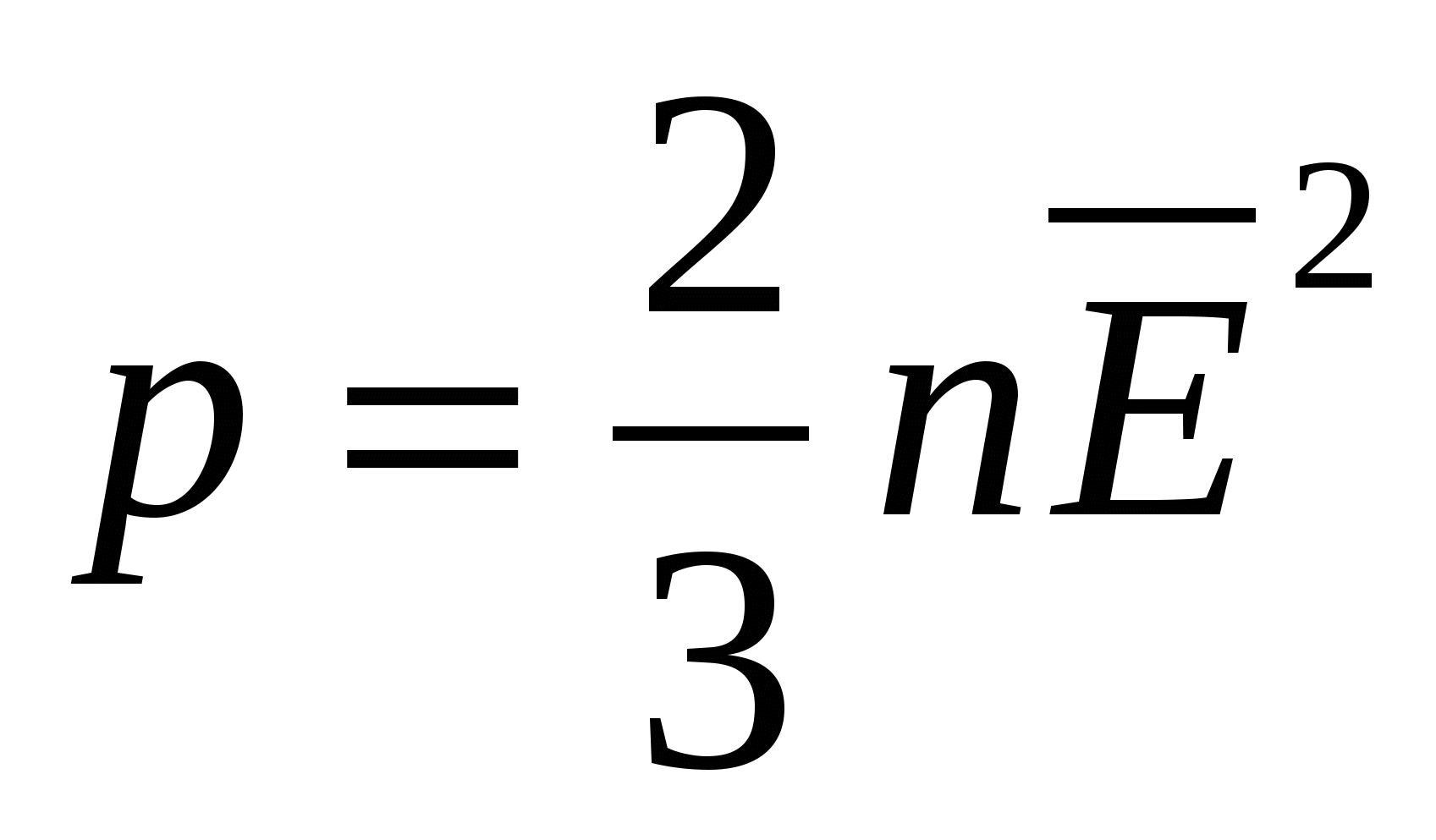
где р - давление газа; n - концентрация молекул газа (число его молекул в единичном объеме): m0 - масса молекулы газа, ![]() - средняя квадратичная скорость движения газовых молекул;
- средняя квадратичная скорость движения газовых молекул; 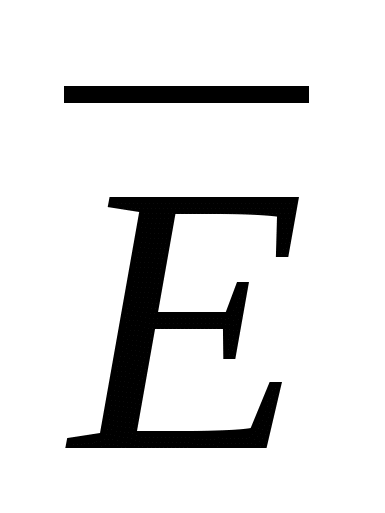 -средняя квадратичная энергия поступательного движения молекул идеального газа.
-средняя квадратичная энергия поступательного движения молекул идеального газа.
Давление идеального газа пропорционально средней кинетической энергии поступательного движения молекул и концентрации молекул.
Это давление тем больше, чем больше средняя кинетическая энергия поступательного движения молекул.
Средней квадратической скоростью называют величину, равную корню квадратному из среднего арифметического значения квадратов скоростей N молекул газа:
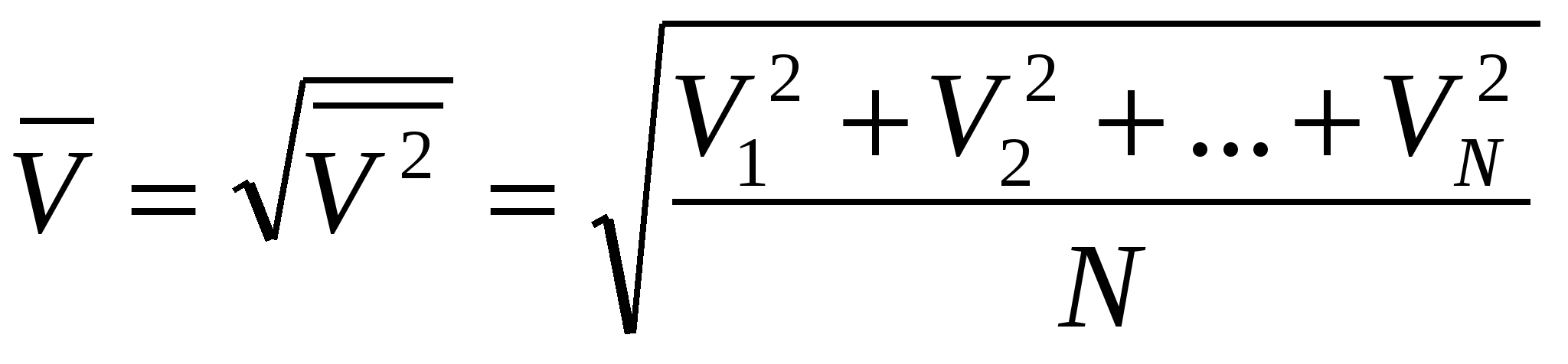
Средней кинетической энергией поступательного движения молекул идеального газа называют величину
![]() С учетом основного уравнения МКТ имеем:
С учетом основного уравнения МКТ имеем:
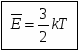
Из этой формулы видно, что средняя кинетическая энергия поступательного движения молекул газа пропорциональна абсолютной температуре.
В этой формуле k=1,3810-23 Дж/К - постоянная Больцмана.
Д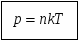 авление газа зависит от концентрации молекул. Эта зависимость выражается формулой:
авление газа зависит от концентрации молекул. Эта зависимость выражается формулой:
Давление газа не зависит от его природы, а определяется только концентрацией молекул и температурой газа.
Численное значение средней квадратичной скорости получим из формулы
![]() , т.к.
, т.к. 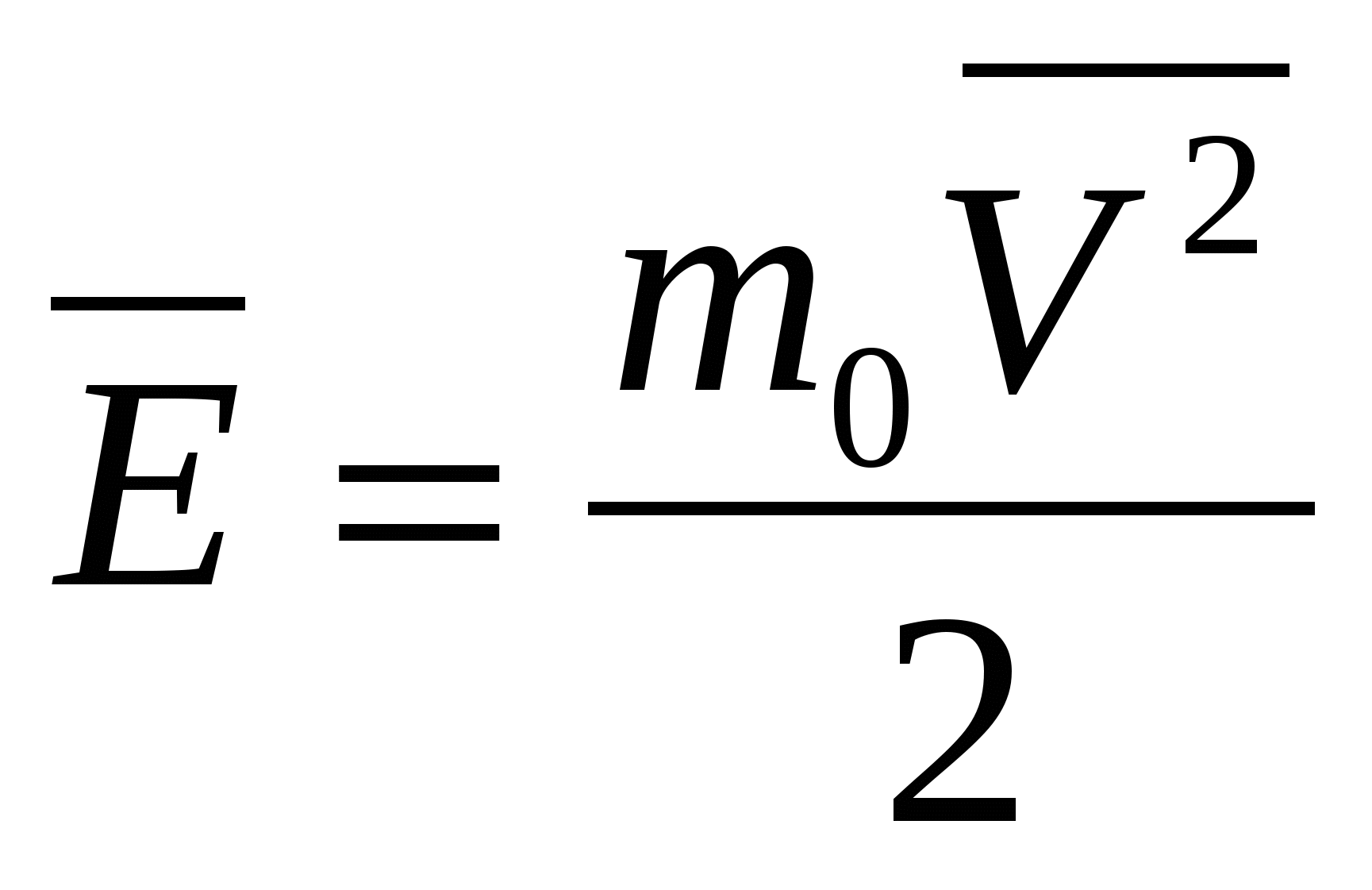 , то
, то 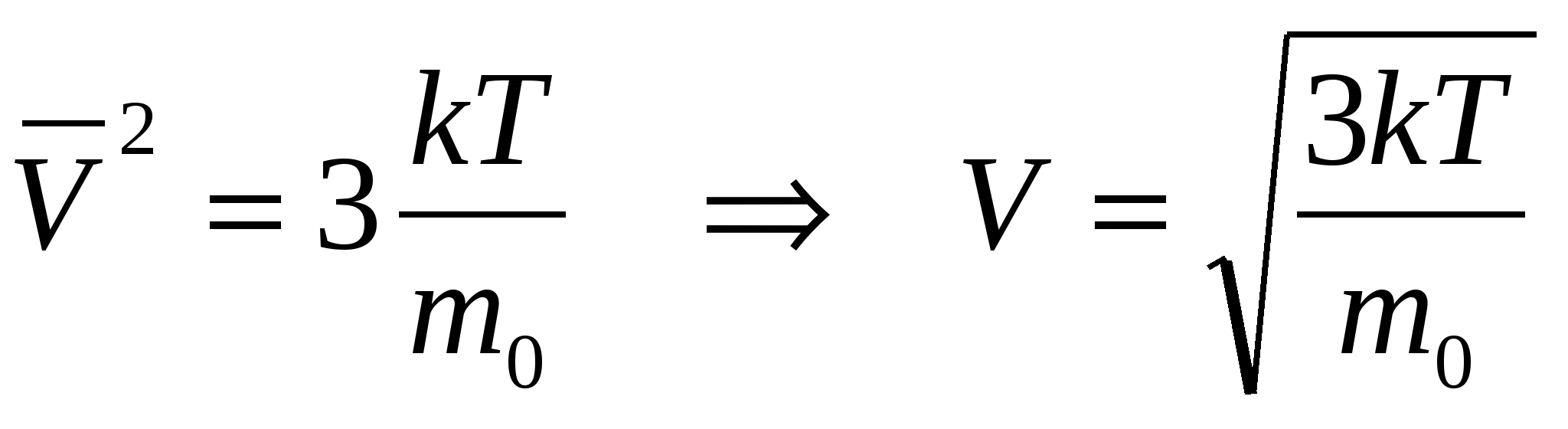
При одинаковых давлениях и температурах концентрация молекул всех газов одинакова. В частности, при нормальных условиях
n= Nл = 2,71025 м-3.
Величину Nл называют числом Лошмидта, оно равно количеству молекул идеального газа, содержащихся в 1 м3 газа при нормальных условиях.
Запишем зависимость давления газа от концентрации молекул и температуры
![]()
![]() подставляем вместо n
подставляем вместо n
![]()
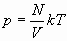 преобразуем
преобразуем
![]() ,
, ![]()
![]() где
где ![]()
![]() -универсальная газовая постоянная
-универсальная газовая постоянная
![]()
![]() -уравнение состояния идеального газа или уравнение Менделеева-Клапейрона.
-уравнение состояния идеального газа или уравнение Менделеева-Клапейрона.
Из данного уравнения вытекает связь между давлением, объемом и температурой идеального газа, который может находиться в двух любых состояниях.
Рассмотрим систему , находящуюся в двух состояниях, с параметрами p, V, T.
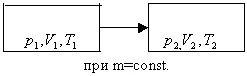
Запишем уравнения для двух состояний.
![]()
![]() поделим первое на второе
поделим первое на второе
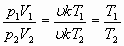
![]()
![]() при
при 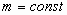 уравнение Клапейрона.
уравнение Клапейрона.
(Учащиеся самостоятельно делают вывод и формулируют определение).
Определение: при фиксированной массе отношение произведения давления и объема на температуру есть величина постоянная.
Учитель:
С помощью уравнения состояния идеального газа можно исследовать процессы, в которых масса газа и один из трех параметров - давление, объем или температура - остаются неизменными.
Определение: количественные зависимости между двумя параметрами газа при фиксированном значении третьего параметра называют газовыми законами (изопроцессамия).
IV. Решение количественных задач:
Задача №1.
Найти концентрацию молекул кислорода, если его давление 0,2 МПа, а средняя квадратичная скорость молекул равна 700 м/с.
Дано: Решение:
υ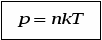 =700 м/с
=700 м/с
M =32·10 -3 кг/моль n=р/κТ
р =0,2 МПа
n=? n=3Nа р/υ2 М = 2,3·1025.
Ответ: 2,3·1025.
Задача №2.
Определить кинетическую энергию 105 атомов гелия при температуре 47 ºС. (6,62· 10-16 Дж)
Задача №3.
Определите температуру газу, если средняя кинетическая энергия равна 5,6 ·10-21 Дж.
(270 К)
Задача №4.
Сколько молекул содержится в 2 м3 газа при давлении 150 кПа и температуре 27 ºС.(7,2·1025 )
Задача №5.
На сколько процентов увеличивается средняя кинетическая энергия молекул газа при увеличении его температуры от 7 до 35 ºС? ( На 10%)
Задача №6.
Определить число n молекул, содержащихся в объеме V = 1 мм3 воды и массу m0 молекулы воды.
Решение:
Число молекул n, содержащихся в теле некоторой массы m:
![]() , где m - молярная масса. Так как
, где m - молярная масса. Так как 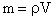 , где r - плотность воды, то:
, где r - плотность воды, то: 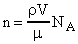 .
.
Расчет в СИ: V = 10-9 м3; r = 103![]() ; NA = 6,021023
; NA = 6,021023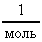 ; m = 1810-3
; m = 1810-3 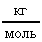 ; n =
; n = 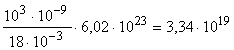 молекул.
молекул.
m0 подсчитываем по формуле (3) 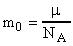 ;
; 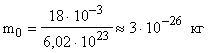 .
.
Задача №7.
Определить число молекул содержащихся в 10 г азота.
Решение:
![]()
Расчет в СИ:
m = 10 г = 10-2 кг; m = 2810-3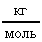 ; NA = 6,021023
; NA = 6,021023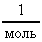 ;
; 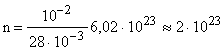 молекул.
молекул.
Задача №8.
Вычислить среднюю квадратичную скорость движения молекул водорода при 00С.
Решение:
Среднюю квадратичную скорость рассчитаем по формуле (17): 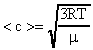 .
.
Расчет в СИ: R = 8,31 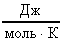 ; m = 210-3
; m = 210-3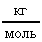 ; Т = 273 К.
; Т = 273 К.
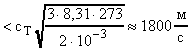 .
.
Задача №9.
Чему равна средняя квадратичная скорость движения молекул воздуха при температуре 270С?
Решение:
Среднюю квадратичную скорость молекул воздуха вычислим по формуле (17).
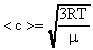 . В Си: m = 2910-3
. В Си: m = 2910-3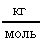 (для воздуха); Т = 2730К;
(для воздуха); Т = 2730К;
R = 8,31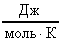 .
.
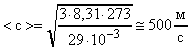 .
.
Задача №10.
Вычислить среднюю энергию поступательного движения молекулы газа при 270С.
Решение:
Для расчета используем формулу (5).
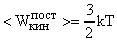 .
.
В Си: К = 1,3810-23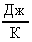 ; Т = 3000К.
; Т = 3000К.
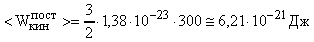 .
.
Задача №11.
Средняя квадратичная скорость молекул некоторого газа = 450 м/с. Давление газа р = 50 кПа. Найти плотность r газа при этих условиях.
Решение:
Основное уравнение молекулярно-кинетической теории запишем в виде:
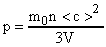 . Так как
. Так как 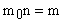 (масса газа); а
(масса газа); а 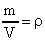 (плотность газа), то
(плотность газа), то 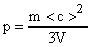 или
или 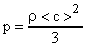 . Откуда
. Откуда 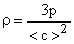 .
.
Расчет в Си: р = 50*103 Па; = 450 м/с.
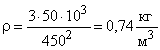 .
.
V. Итог урока, домашнее задание.


