- Преподавателю
- Другое
- Комплект оценочных средств по учебной дисциплине Естествознание По программе подготовки специалистов среднего звена 100126 «Сервис домашнего и коммунального хозяйства»
Комплект оценочных средств по учебной дисциплине Естествознание По программе подготовки специалистов среднего звена 100126 «Сервис домашнего и коммунального хозяйства»
| Раздел | Другое |
| Класс | - |
| Тип | Другие методич. материалы |
| Автор | Кулакова М.А. |
| Дата | 24.02.2015 |
| Формат | doc |
| Изображения | Есть |
Государственное бюджетное образовательное учреждение среднего профессионального образования «Обшаровский государственный техникум им.В.И.Суркова»
Рассмотрено на метод.комиссии Утверждаю
Протокол № зам.директора по УР
От « » _________ 2013 г.
Председатель метод.объединения ___________ Щетинина Н.Н.
_______ Э.В.Латыпова
«____»___________ 2013 г.
Комплект оценочных средств
по учебной дисциплине
Естествознание
По программе подготовки специалистов среднего звена
100126 «Сервис домашнего и коммунального хозяйства»
С.Обшаровка, 2013
Комплект оценочных средств разработан на основе программы подготовки специалистов среднего звена специальности СПО 100126 ««Сервис домашнего и коммунального хозяйства» программы учебной дисциплины Биология.
Разработчик(и):
ГБОУ СПО ОГТ преподаватель М.А. Кулакова
(место работы) (занимаемая должность) (инициалы, фамилия)
СОДЕРЖАНИЕ
-
Паспорт комплекта оценочных средств
-
Результаты освоения учебной дисциплины, подлежащие проверке
3. Оценка освоения учебной дисциплины
3.1. Формы и методы оценивания
3.2. Типовые задания для оценки освоения учебной дисциплины
4. оценочные материалы для итоговой аттестации по учебной дисциплине Биология по специальности СПО 100126 «Сервис домашнего и коммунального хозяйства»
4.1 Оценочные материалы для итоговой аттестации по биологии по специальности СПО 100126 «Сервис домашнего и коммунального хозяйства»
-
Паспорт комплекта оценочных средств
В результате освоения учебной дисциплины Биология обучающийся должен обладать предусмотренными ФГОС специальности СПО 100126 «Сервис домашнего и коммунального хозяйства»; следующими умениями, знаниями:
У1 - характеризовать понятия механики
У2- объяснять законы квантовой физики
У3- рассмотреть эволюцию вселенной
У 4 - ориентироваться в универсальных и специальных информационных ресурсах (поиск, отбор и использование информации);
У 5 - характеризовать химический состав клетки, обмен веществ в клетке;
У 6 - показать отличия в строении ДНК и РНК;
У 7 - объяснять процессы митоза и мейоза,
характеризовать сущность полового и бесполого размножения;
У 8 - объяснять законы наследственности;
У9 - решать генетические задачи, строить вариационные кривые, работать с учебной литературой;
У10- понимать необходимость практической селекции и теоретической генетики для повышения эффективности с/х производства;
У11 - объяснять причины возникновения многообразия видов живых организмов и их приспособленности к условиям окружающей среды;
З 1 - особенности жизни как формы существования материи, роли физических и химических процессов в живых системах.
З2 - положения клеточной теории, основные функции органелл, цитоплазмы, сущность и значение клеточной теории, особенности строения прокариот, эукариот.
З3 - сущность процессов наследственности и изменчивости, типы скрещиваний, генетическую терминологию, хромосомную теорию
наследственности значение генетики для селекции и медицины.
З4 - методы селекции растений и животных, центры происхождения культурных растений. Успехи селекционеров, направления биотехнологии.
З5 - об основной теории биологии - эволюционной, причины эволюции, ее закономерности, движущие силы.
З6 - основные гипотезы возникновения жизни на Земле
Формой аттестации по учебной дисциплине является зачет
2. Результаты освоения учебной дисциплины, подлежащие проверке
2.1. В результате аттестации по учебной дисциплине осуществляется комплексная проверка следующих умений и знаний:
Таблица 1.1
Результаты обучения: умения, знания
Показатели оценки результата
Следует сформулировать показатели
Раскрывается содержание работы
Уметь:
У1 - характеризовать понятия механики
Расширение навыков исследовательской деятельности
У2- объяснять законы квантовой физики
Развитие навыков самостоятельной деятельности
У3- рассмотреть эволюцию вселенной
развитие интеллектуальных и творческих способностей
У 4 - ориентироваться в универсальных и специальных информационных ресурсах (поиск, отбор и использование информации);
Расширение навыков исследовательской деятельности
У 5 - характеризовать химический состав клетки, обмен веществ в клетке;
Развитие навыков самостоятельной деятельности
У 6 - показать отличия в строении ДНК и РНК;
развитие интеллектуальных и творческих способностей
У 7 - объяснять процессы митоза и мейоза,
характеризовать сущность полового и бесполого размножения;
Расширение кругозора обучающихся
У 8 - объяснять законы наследственности;
Расширение навыков исследовательской деятельности
У9 - решать генетические задачи, строить вариационные кривые, работать с учебной литературой;
Развитие навыков самостоятельной деятельности
У10- понимать необходимость практической селекции и теоретической генетики для повышения эффективности с/х производства;
развитие интеллектуальных и творческих способностей
У11 - объяснять причины возникновения многообразия видов живых организмов и их приспособленности к условиям окружающей среды;
Расширение навыков исследовательской деятельности
Знать:
З 1 - особенности жизни как формы существования материи, роли физических и химических процессов в живых системах.
Расширение навыков исследовательской деятельности
З2 - положения клеточной теории, основные функции органелл, цитоплазмы, сущность и значение клеточной теории, особенности строения прокариот, эукариот.
Развитие навыков самостоятельной деятельности
З3 - сущность процессов наследственности и изменчивости, типы скрещиваний, генетическую терминологию, хромосомную теорию
наследственности значение генетики для селекции и медицины.
развитие интеллектуальных и творческих способностей
З4 - методы селекции растений и животных, центры происхождения культурных растений. Успехи селекционеров, направления биотехнологии.
Расширение навыков исследовательской деятельности
З5 - об основной теории биологии - эволюционной, причины эволюции, ее закономерности, движущие силы.
Развитие навыков самостоятельной деятельности
З6 - основные гипотезы возникновения жизни на Земле
развитие интеллектуальных и творческих способностей
3. Оценка освоения учебной дисциплины:
3.1. Формы и методы оценивания
Предметом оценки служат умения и знания по дисциплине Естествознание.
Контроль и оценка освоения учебной дисциплины по разделам Таблица 2.2
Элемент учебной дисциплины
Формы и методы контроля
Текущий контроль
Рубежный контроль
Промежуточная аттестация
Форма контроля
Проверяемые У, З
Форма контроля
Проверяемые
У, З
Форма контроля
Проверяемые
У, З
Раздел 1 Механика
Устный опрос
Практическая работа №1-9
Самостоятельная работа
У1,
У1, З1,
Раздел 2 Молекулярная физика. Термодинамика.
Устный опрос
Практическая работа №10-13 Тестирование
Самостоятельная работа
У2,
У2,З2,
Раздел 3 Электродинамика
Устный опрос
Практическая работа №14-19 Тестирование
Самостоятельная работа
У3,
У3,У4,У5,У6,
З3,
Раздел 4 Строение атома и квантовая физика
Устный опрос
Практическая работа №20-22 Тестирование
Самостоятельная работа
У7,З4,
У7,З4,
Раздел 5
Эволюция Вселенной
Устный опрос
Тестирование
Практическая работа №23
Самостоятельная работа
У8,У10,З5
У8,У10,З5
Раздел 6. Химические свойства и превращения веществ
Устный опрос
Тестирование
Практическая работа №24,25
Самостоятельная работа
У9,З6
У9,З6
Раздел 7. Неорганические соединения
Устный опрос
Тестирование
Практическая работа №26,27
У4,У5,У6,З1,З2,З3
У1,У2,У3,У4,У5, У6,У7,У8,
У9,У10, З1,З2
Раздел 8. Органические соединения
Устный опрос
Тестирование
Практическая работа №28,29,30,31
Самостоятельная работа
У4,У5,У6,З1,З2,З3
Раздел 9. Клеточное строение организмов
Устный опрос
Тестирование
Практическая работа №32
Самостоятельная работа
У4,У5,У6,З1,З2,З3
Раздел 10. Наследственность и изменчивость
Устный опрос
Тестирование
Практическая работа №33,34
У4,У5,У6,З1,З2,З3
Раздел 11. Многообразие и эволюция органического мира
Устный опрос
Тестирование
Практическая работа №35
Самостоятельная работа
У4,У5,У6,У7,У8,У10,З1,З2,З3
Раздел 12. Надорганизменные системы
Устный опрос
Тестирование
Практическая работа №36
У4,У10,У11,З1,З2,З3
зачет
У1,У2,У3,У4,У5, У6,У7,У8,У9,У10, З1,З2,З3,
3.2. Типовые задания для оценки освоения учебной дисциплины
3.2.1. Типовые задания для оценки знаний У1.
Практическая работа: «Относительность механического движения»
Проводится в форме контрольных вопросов
Вариант 1
-
Эскалатор метро поднимает неподвижно стоящего на нем пассажира в течение 1 минуты. По неподвижному эскалатору пассажир поднимается за 3 минуты. Сколько времени будет подниматься идущий вверх пассажир по движущемуся эскалатору. (Ответ: 45 с.)
-
Сделайте вывод о выполнении закона сложения скоростей.
Вариант 2
-
Самолет движется относительно воздуха со скоростью 50 м/с. Скорость ветра относительно земли 15 м/с. Какова скорость самолета относительно земли, если он движется по ветру? Против ветра? Перпендикулярно направлению ветра? (Ответ: v, = 65 м/с, v,= 35 м/с, v3 = 52 м/с.)
-
Для вычислений использовать калькулятор в компьютере. Нажать «инструменты», выбрать калькулятор, нажать «вид», выбрать нужный вам.
3.2.2. Типовые задания для оценки знаний У1
Практическая работа: «Равноускоренное движение»
Проводится в форме контрольных вопросов
-
Что такое ускорение и для чего его нужно знать?
-
При любом неравномерном движении изменяется скорость. Как ускорение характеризует это изменение?
-
Чем отличается «замедленное» прямолинейное движение от «ускоренного»?
-
Что такое равноускоренное движение?
3.2.3. Типовые задания для оценки знаний У1
Практическая работа: « Периодическое движение»
Проводится в форме контрольных вопросов.
-
Что такое механическое движение?
-
Какой раздел механики изучает механическое движение?
-
Какие виды механического движения вы знаете?
3.2.4. Типовые задания для оценки знаний У1
Практическая работа: «Взаимодействие тел»
Проводится в форме докладов
-
Взаимодействие тел
-
Виды взаимодействия
-
Значение и применение взаимодействия тел
3.2.5. Типовые задания для оценки знаний У1
Практическая работа: « Закон всемирного тяготения»
Проводится в форме рефератов
-
Закон всемирного тяготения
-
Применение закона всемирного тяготения
-
Значение закона.
3.2.6. Типовые задания для оценки знаний У1
Практическая работа: «Закон сохранения импульса»
Проводится в форме докладов.
-
Закон сохранения импульса.
-
Применение закона.
-
Значение закона сохранения импульса
3.2.7. Типовые задания для оценки знаний У1
Практическая работа: «Механические колебания»
Проводится в форме контрольных вопросов.
-
Нитяной маятник колеблется с частотой 2 Гц. Определите период колебаний и число колебаний в минуту.
-
Могут ли свободные колебания происходить в колебательной системе? в системе, не являющейся колебательной? Если могут, то приведите примеры.
-
В океанах длина волны достигает 270 м, а период колебаний 13,5с. Определите скорость распространения такой волны.
-
Могут ли вынужденные колебания происходить в колебательной системе? в системе, не являющейся колебательной? Если могут, то приведите примеры.
3.2.8. Типовые задания для оценки знаний У1
Практическая работа: «Свойства волн»
Проводится в форме докладов.
-
Свойства волн.
-
Применение волн.
-
Значение волн для человека.
3.2.9. Типовые задания для оценки знаний У1
Практическая работа «Исследование зависимости силы трения от веса тела »
Проводится в форме контрольных вопросов
1. Назовите известные вам силы в механике.
2. При каком условии появляются силы упругости?
3. Каким образом возникают деформации тел?
4. Сформулируйте закон Гука?
5. Каков физический смысл жёсткости пружины?
6. Определите границы применимости закона Гука.
7. Как формулируется закон всемирного тяготения?
8. Что называется гравитационной постоянной?
9. Каков физический смысл гравитационной постоянной?
10. Что называют силой тяжести?
11. По какой формуле определяют модуль силы тяжести?
12. Зависит ли ускорение свободного падения тела от массы?
13. От чего зависит ускорение свободного падения?
14. Что называют весом тела?
15. В чём различие между силой тяжести и весом тела?
16. В каком случае сила тяжести и вес тела равны?
3.2.10. Типовые задания для оценки знаний У2
Практическая работа: «Абсолютная температура»
Проводится в форме докладов
-
Абсолютная температура
-
Применение понятия абсолютная температура
3.2.11. Типовые задания для оценки знаний У2.
Практическая работа: «Модель жидкости».
Проводится в форме рефератов.
-
Модель жидкости.
-
Модель твердого вещества.
-
Модель газообразного вещества.
3.2.12. Типовые задания для оценки знаний У2.
Практическая работа: «Количество теплоты»
Проводится в форме контрольных вопросов.
-
Если прогретые в кипящей воде цилиндры из свинца, олова и стали массой 1 кг поставить на лед, то они охладятся, и часть льда под ними растает. Как изменится внутренняя энергия цилиндров? Под каким из цилиндров растает больше льда, под каким - меньше?
-
Нагретый камень массой 5 кг. Охлаждаясь в воде на 1 градус, передает ей 2,1 кДж энергии. Чему равна удельная теплоемкость камня
-
При закалке зубила его сначала нагрели до 6500, потом опустили в масло, где оно стыло до 500С. Какое при этом выделилось количество теплоты, если его масса 500 гр.
-
Какое количество теплоты пошло на нагревание от 200 до 12200С. стальной заготовки для коленчатого вала компрессора массой 35 кг.
3.2.13. Типовые задания для оценки знаний У3.
Практическая работа: «Закон Кулона»
Проводится в форме докладов.
-
Закон Кулона
-
Применение закона Кулона.
3.2.14. Типовые задания для оценки знаний У3
Практическая работа: «Постоянный электрический ток»
Проводится в форме докладов
1. Постоянный электрический ток. Направление тока.
2. Сила тока (определение, обозначение, формула, ед. измерения)
3. Напряжение (определение, обозначение, формула, ед. измерения)
4. Сопротивление (определение, обозначение, формула, ед. измерения)
5. Закон Ома для участка цепи без ЭДС (определение, формула)
6. ЭДС источника тока (определение, обозначение, формула, ед. измерения)
7. Последовательное соединение проводников (чертеж, законы)
8. Параллельное соединение проводников (чертеж, законы)
9. Закон Ома для полной цепи, содержащей ЭДС (определение, формула)
10. Работа электрического тока (определение, формулы, обозначение, ед. измерения)
11. Мощность электрического тока (определение, формулы, обозначение, ед. измерения)
12. Закон Джоуля-Ленца (определение, формула)
13. Собственная и примесная проводимость полупроводников (определения)
14. Полупроводники n-типа. Донорная примесь (определения)
15. Полупроводники p-типа. Акцепторная примесь (определения)
3.2.15. Типовые задания для оценки знаний У1, У5,У7,З1,З2,З5, З6.
Практическая работа «Сборка электрической цепи »
Проводится в форме контрольных вопросов
-
Чем различаются последовательное и параллельное соединение проводников?
-
Как связаны между собой сила тока, напряжение и сопротивление на участке цепи?
-
Перечислить виды проводов и их назначение.
3.2.16. Типовые задания для оценки знаний У3.
Практическая работа: «Магнитное поле».
Проводится в форме контрольных вопросов
-
Понятие магнитного поля. Причины, порождающие магнитное поле. Объекты, на которых воздействует магнитное поле.
-
Магнитная индукция. Направление магнитной индукции. Магнитные линии. Магнитные линии поля создаваемого прямолинейным проводником с током, кольцом с током, соленоидом, постоянным магнитом.
-
Заряженные частицы в магнитном поле. Сила Лоренца. Направление силы Лоренца. Движение заряженных частиц в магнитном поле. Применение силы Лоренца.
-
Взаимодействие проводов с током. Определение единицы силы тока. Сила Ампера. Применение силы Ампера (электроизмерительные приборы, динамик).
-
Магнитные свойства вещества. Ферромагнетики. Намагничивание ферромагнетиков. Магнитная проницаемость вещества. Точка Кюри.
-
Явление электромагнитной индукции. Понятие магнитного потока. Правило Ленца. Вывод правила Ленца из закона сохранении энергии.
-
Закон электромагнитной индукции. Причина возникновения ЭДС индукции при изменении магнитной индукции. Вихревое электрическое поле. Токи Фуко.
-
ЭДС в движущихся проводниках. (причина, расчетная формула).
-
ЭДС самоиндукции, индуктивность. Аналогия между индуктивностью в теории электрического тока и массой в механике. Энергия магнитного поля.
3.2.17. Типовые задания для оценки знаний У3.
Практическая работа: «Электромагнитное поле».
Проводится в форме контрольных вопросов
Задача № 1.
По проводнику длиной 45 см протекает ток силой 20 А. Чему равна индукция магнитного поля, в которое помещен проводник, если на проводник действует сила 9мН?
(Ответ: В = 1мТл).
Задача № 2.
Определите модуль силы, действующей на проводник с током длиной 20 см при силе тока 10 А в магнитном поле с индукцией 0,13 Тл.
(Ответ: F = 0,26Н).
3.2.18. Типовые задания для оценки знаний У3.
Практическая работа: «Интерференция и дифракция света».
Проводится в форме контрольных вопросов
1. Свет длиной волны 480 нм падает перпендикулярно на непрозрачную плоскость с двумя узкими параллельными щелями, находящимися на расстоянии 0,15 мм. В результате, на экране, находящемся на расстоянии 2 м от плоскости появляются интерференционные полосы. На каком расстоянии от центральной яркой полосы будетнаходится второй интерференционный максимум?
2. Свет длиной волны 694 нм падает перпендикулярно на непрозрачную плоскость с двумя узкими горизонтальными щелями. При этом четвёртый интерференционный максимум мы видим под углом 1° по отношению к направлению на центральную яркую полосу интерференционной картины. Чему равно расстояние между щелями?
3. Свет длиной волны 550 нм падает перпендикулярно на непрозрачную плоскость с двумя узкими параллельными щелями, находящимися на расстоянии 0,1 мм. В результате, на экране, находящемся на расстоянии 2 м от плоскости появляются интерференционные полосы. На каком расстоянии друг от друга будут находиться два интерференционных максимума третьего порядка?
4. Свет длиной волны 500 нм падает перпендикулярно на непрозрачную плоскость с двумя узкими параллельными щелями, находящимися на расстоянии 0,2 мм. В результате, на экране появляются интерференционные полосы. На каком расстоянии находится экран с интерференционными полосами, если первый интерференционный минимум находится на расстоянии 1 мм от центральной яркой полосы?
5. Свет длиной волны 450 нм падает перпендикулярно на непрозрачную плоскость с двумя узкими горизонтальными щелями. В результате, на экране, находящемся на расстоянии 4 м от плоскости появляются интерференционные полосы. Чему равно расстояние между щелями, если первые интерференционные минимумы находятся на расстоянии 0,5 см друг от друга?
6. Белый свет падает перпендикулярно на непрозрачную плоскость с двумя узкими параллельными щелями. В результате, на экране, находящемся на некотором расстоянии от плоскости появляются интерференционные полосы. При этом первый интерференционный максимум для красного цвета (l=780 нм) накладывается на второй интерференционный максимум для фиолетового цвета. Чему равна длина волны фиолетового цвета?
7. Солнечный свет падает перпендикулярно на непрозрачную плоскость с двумя узкими параллельными щелями, находящимися на расстоянии 0,2 мм. В результате, на экране, находящемся на расстоянии 2 м от плоскости появляются интерференционные полосы. Чему равно расстояние между первым интерференционным максимумом для фиолетового цвета (l=400 нм) и вторым интерференционным максимумом для красного цвета (l=600 нм)?
3.2.19. Типовые задания для оценки знаний У4,У5,У6,З1,З2,З3, З6.
Практическая работа: «Лазеры».
Проводится в форме докладов
-
Понятие лазер
-
Применение лазера
-
Виды лазера
3.2.20. Типовые задания для оценки знаний У4,У5,У6,З1,З2,З3, З6.
Практическая работа: «Ядерные реакции»
Проводится в форме в форме рефератов
-
Ядерные реакции
-
Применение ядерных реакций
-
Значение ядерных реакций для человека
3.2.21. Типовые задания для оценки знаний У4,У5,У6,З1,З2,З3, З6.
Практическая работа: «Биологическое действие радиоактивных излучений».
Проводится в форме докладов
-
Радиоактивное излучение
-
Вред от радиоактивного излучения
3.2.22. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Термоядерный синтез»
Проводится в форме контрольных вопросов
-Чем вызывается деление тяжёлых ядер?
-Что образуется при делении тяжёлых ядер?
- Чем сопровождается деление тяжёлых ядер?
-В чем причина выделения энергии?
3.2.23. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Химическая связь»
Проводится в форме контрольных вопросов
1.Дать понятие химическая связь
2.Рассмотреть виды химической связи
3.Примеры химической связи
3.2.24. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Окислительно-восстановительные реакции»
Проводится в форме докладов
-
Окислительно-восстановительные реакции
-
Значение окислительно-восстановительных реакций
3.2.25. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Кислоты»
Проводится в форме докладов
-
Свойства соляной кислоты
-
Свойства серной кислоты
-
Свойства уксусной кислоты
3.2.26. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Соли»
Проводится в форме контрольных вопросов
1. Как проходит диссоциация солей в водных растворах?
2. Напишите уравнения диссоциации солей:
а) K2S, Mg(N03)2, Na2C03, NiS04;
б) MnS04, A1C13> ZnCl2, CoCl3;
в) NaHC03 и KHS04;
r) Mg(OH)N03 и Fe(OH)Cl2.
3. Что такое степень диссоциации электролита?
4. От чего зависит степень диссоциации электролита?
3.2.27. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Предельные углеводороды».
Проводится в форме теста
Проводится в форме теста
ЗАДАНИЕ
ЭТАЛОН ОТВЕТА
БАЛЛЫ
А 1. Общая формула гомологического ряда алканов:
-
СnH2n 2. CnH2n+2 3. CnH2n-2 4. CnH2n-6
А 2. Число элементов в веществе бутан равно :
-
1 2. 2 3. 3 4. 4
А 3. Гомологи - это :
-
Гексан и гексаналь. 2. Гексан и гексен. 3. Бутан и пентан. 4.Бутан и пентил.
А 4. Реакции замещения характерны для :
-
Этана. 2. Пропена. 3. Бутадиена. 4. Пентина.
А 5. Структурные изомеры - это :
1. Гексан и бутан. 2. Циклобутан и циклопропан. 3. Бутан и 2-метилбутан. 4. Бутан и 2-метилпропан.
А 6. В молекуле какого вещества отсутствуют π-связи :
-
Этина. 2. Изобутана. 3. Этена. 4. Циклопентена.
А 7. Число атомов углерода в 5,6 л (н. у. ) пропана, равно :
-
5 . 1022 2. 1,5 . 1023 3. 0,1 . 1023 4. 4,5 . 1023
А 8. Углеводород, в котором орбитали всех атомов углерода имеют sp3-гибридизацию, - это
-
Изобутан. 2. Бутадиен -1,3. 3. Пропин. 4. Бензол.
А 9. Массовая доля водорода будет наибольшей в соединении:
-
С3Н8 2. С4Н10 3. С6Н6 4. С5Н12
А 10. 2 -бром- 2 -метилбутан взаимодействует с
1. Концентрированной серной кислотой. 2. Азотом. 3. Хлороводородом. 4. Гидроксидом калия в спиртовом растворе.
А 11. Объем (в литрах, н. у.) порции этана, содержащей 7,224 . 1023 атомов водорода, равен:
-
26,88 2. 13,44 3. 4,48 4. 53,2
А 12. Наиболее близкие химические свойства имеют оба вещества набора:
Сульфаты кальция и марганца (II). 2. Этан и пропан. 3. Диоксиды кремния и серы.4. Этилен и ацетилен.
А 13. В схеме превращений этанол → Х →бутан веществом Х является :
-
Бутанол - 1. 2. Бромэтан. 3. Этан. 4. Этилен.
А 14. Масса ( в граммах ) смеси, состоящей из 2,24 л ( н. у. ) метана и 1,12 л ( н. у. ) азота равна :
-
1 2. 2,3 3. 3 4. 4,6
А 15. Общая формула гомологического ряда циклоалканов :
-
СnH2n+2 2. CnH2n 3. CnH2n-2 4. CnH2n-6
А 16. Реакция отщепления (элиминирования ) не характерна для :
-
Бромэтана. 2. Пропанола. 3. 1,2 - дибромэтана. 4. 2,2,3,3 - тетраметилэтана.
А 17. В результате следующих превращений
С + Н2 → Х1 → Х2 → Х3 → Х4 → Х5 образуется конечный продукт (Х5 ):
-
Пропан. 2. Бутан. 3. Этан. 4. Этилен.
А 18. Масса (кг ) тетрахлорметана, полученного из 64 кг метана с практическим выходом 97,4 %, составляет :
-
600 2. 300 3. 900 4. 1500
А 19. Назовите вещество по международной номенклатуре ИЮПАК :
СН3 - СН - СН2 - СН3
-
2 - этилпропан. 2. 3 - этилпропан. 3. 3 - метилпентан. 4. 3 - метилбутан.
А 20. Масса углеводорода ( в граммах ), полученного при нагревании 48 г 2 - бромбутана с 7,67 г натрия, составляет :
10 2. 19 3. 38 4.76
Оценочная шкала
№
Эталон ответа
Баллы
1
4
2
2
3
2
3
2
2
4
1
2
5
2
2
6
3
2
7
4
5
8
2
2
9
3
2
10
4
2
11
2
2
12
3
5
13
4
5
14
3
5
15
2
5
16
1
5
17
1
5
18
3
5
19
4
5
20
2
5
Максимальные
баллы
баллы
70
3.2.28. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Природные источники углеводородов».
Проводится в форме докладов
-
Значение природных источников углеводородов
-
Природные источники углеводородов
-
Применение природных источников углеводородов
3.2.29. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Сложные эфиры»
Проводится в форме контрольных вопросов
Вариант I.
1.Напишите 2 структурные формулы веществ, отвечающих составу С4Н8О2 и относящихся к разным классам веществ. Назовите оба вещества и укажите классы, к которым они относятся.
2. Напишите уравнения реакций, при помощи которых можно осуществить превращения по схеме:
этилен → этиловый спирт →
уксусноэтиловый эфир
ацетат натрия → уксусная кислота →
Укажите условия осуществления реакций и названия всех веществ.
3. Сколько граммов уксусной кислоты можно получить при окислении
88 г.этаналя, если практический выход продукта реакции равен 80%?
4. Жиры представляют собой
1) сложные эфиры глицерина и высших карбоновых кислот
2) сложные эфиры этиленгликоля и высших карбоновых кислот
3) натриевые соли высших карбоновых кислот
4) смесь высших карбоновых кислот
5. Укажите формулу предельной одноосновной карбоновой кислоты
1)С3Н6О2 2)С2Н6О2 3)С4Н6О2 4) С6Н6О2
6. л-Связь есть в молекуле
1) 2-метилбутановой кислоты
2) 2,3-диметилбутанола-1
3)этандиола-1,2
4) пропантриола-1,2,3
Вариант II.
1.Напишите 2 структурные формулы веществ, отвечающих составу С5Н10О2 и относящихся к разным классам веществ. Назовите оба вещества и укажите классы, к которым они относятся.
2. Напишите уравнения реакций, при помощи которых можно осуществить превращения по схеме:
пропилен → пропиловый спирт →
пропиловый эфир муравьиной
формиат натрия → муравьиная кислота → кислоты
Укажите условия осуществления реакций и названия всех веществ.
3. Сколько граммов сложного эфира получится при взаимодействии
120 г. уксусной кислоты с этанолом, если практический выход продукта реакции равен 90%?
4.Сколько перечисленных веществ реагируют с уксусной кислотой: гидроксид железа (III), пропанол-1, цинк, хлор (в присутствии катализатора), карбонат натрия, формальдегид
1) три 2) четыре 3) пять 4) шесть
5. Какая кислота не существует:
1) 2-этилпропановая 2) 2,2-дихлорбутановая 3) 4-метилбензойная
4) пропеновая
6. По химическому строению жиры представляют собой
1) сложные эфиры 3) карбоновые кислоты
2) трехатомные спирты 4) альдегиды
3.2.30. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Белки»
Проводится в форме рефератов.
1. Качественные реакции на белки
2. Методы определения белков.
3. Кислотный метод измерения жирности продуктов
4. Химия и функции белков.
3.2.31. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Размножение организмов».
Проводится в форме докладов
-
Размножение организмов
-
Виды размножения
-
Значение размножения организмов
3.2.32. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Наследственная и ненаследственная изменчивость»
Проводится в форме рефератов
-
Дать понятие изменчивость.
-
Виды изменчивости у растений.
-
Дать понятие изменчивость.
-
Виды изменчивости у животных.
3.2.33. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Мутагены и мутации»
Проводится в форме докладов
-
Мутагены
-
Мутации
-
Значение мутаций
3.2.34. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Движущие силы эволюции»
Проводится в форме контрольных вопросов
Каково эволюционное значение непрямого развития?
Почему именно популяции являются единицей эволюции?
Как можно объяснить совпадение формы некоторых цветков с формой тела насекомых или с формой отдельных его частей?
Назовите основные положения синтетической теории эволюции?
В чём заключается различие между естественным и искусственным отбором?
3.2.35. Типовые задания для оценки знаний У5, У7,У8,З1,З2,З3, З6.
Практическая работа: «Экологические факторы»
Проводится в форме контрольных вопросов
1. На какие две группы традиционно делятся экологические факторы?
2. На какие параметры жизнедеятельности организма влияют экологические факторы?
3. Что такое зимний покой?
4. Что является характерной чертой зимнего покоя?
5. В чем различие пойкилотермных и гомойотермных животных?
6. Что такое анабиоз?
7. Что такое криопротекторы?
8. Что такое фотопериодизм?
4. Контрольно-оценочные материалы для итоговой аттестации по учебной дисциплине Естествознание
Предметом оценки являются умения и знания. Контроль и оценка осуществляются с использованием следующих форм и методов: зачета.
Оценка освоения дисциплины предусматривает использование оценочной шкалы для зачета
I. ПАСПОРТ
Назначение:
КОМ предназначен для контроля и оценки результатов освоения учебной дисциплины название по специальности СПО «Сервис домашнего и коммунального хозяйства»
Умения
У1 - характеризовать понятия механики
У2- объяснять законы квантовой физики
У3- рассмотреть эволюцию вселенной
У 4 - ориентироваться в универсальных и специальных информационных ресурсах (поиск, отбор и использование информации);
У 5 - характеризовать химический состав клетки, обмен веществ в клетке;
У 6 - показать отличия в строении ДНК и РНК;
У 7 - объяснять процессы митоза и мейоза,
характеризовать сущность полового и бесполого размножения;
У 8 - объяснять законы наследственности;
У9 - решать генетические задачи, строить вариационные кривые, работать с учебной литературой;
У10- понимать необходимость практической селекции и теоретической генетики для повышения эффективности с/х производства;
У11 - объяснять причины возникновения многообразия видов живых организмов и их приспособленности к условиям окружающей среды;
З 1 - особенности жизни как формы существования материи, роли физических и химических процессов в живых системах.
З2 - положения клеточной теории, основные функции органелл, цитоплазмы, сущность и значение клеточной теории, особенности строения прокариот, эукариот.
З3 - сущность процессов наследственности и изменчивости, типы скрещиваний, генетическую терминологию, хромосомную теорию
наследственности значение генетики для селекции и медицины.
З4 - методы селекции растений и животных, центры происхождения культурных растений. Успехи селекционеров, направления биотехнологии.
З5 - об основной теории биологии - эволюционной, причины эволюции, ее закономерности, движущие силы.
З6 - основные гипотезы возникновения жизни на Земле
II. ЗАДАНИЕ ДЛЯ ЭКЗАМЕНУЮЩЕГОСЯ.
Вариант 1
Инструкция для обучающихся
При выполнении заданий укажите цифру правильного ответа.
Внимательно прочитайте задание.
Время выполнения задания - 40 мин.
Вариант-1.
ЗАДАНИЕ
ЭТАЛОН ОТВЕТА
БАЛЛЫ
1. Выбрать правильный ответ.
1.Генетика-это наука о:
а) селекции организмов б) наследственности и изменчивости организмов
в) эволюции органического мира г) генной инженерии.
2. Ген кодирует информацию о структуре:
а) молекулы аминокислоты б) одной молекулы т-РНК
в) одной молекулы фермента г) нескольких молекул белка.
3. Фенотип организма-это:
а) проявляющиеся внешние и внутренние признаки
б) наследственные признаки организма
в) способность организма к изменениям
г) передача признака от поколения к поколению.
4. Аллельными считаются следующие пары генов:
а) рост человека-форма его носа б) карие глаза- голубые глаза
в) рогатость коров-окраска коров г) чёрная шерсть- гладкая шерсть.
5. Гетерозигота-это пара:
а) аллельных доминантных генов
б) неаллельных доминантного и рецессивного генов
в) аллельных доминантного и рецессивного генов
г) аллельных рецессивных генов.
6. Потомство, рождающееся от одного самоопыляющегося растения в течении нескольких лет, называется:
а) доминантным б) гибридным в) рецессивным г) чистой линией.
7. Наследственность- это свойство организмов, которое обеспечивает:
а) внутривидовое сходство организмов
б) различия между особями внутри вида
в) межвидовое сходство организмов
г) изменения организмов в течение жизни.
8. В каком случае приведены примеры анализирующего скрещивания:
а) ВВ х Вв и вв х вв б) Аа х аа и АА х аа
в) Сс х Сс и сс х сс г) DD x Dd и DD x DD
9. Явление сцепленного наследования получило название:
а) третьего закона Менделя б) гипотезы чистоты гамет
в) кроссинговера г) закона Моргана.
10. Модификационная изменчивость:
а) наследуется б) связана с изменениеми генотипа
в) не наследуется г) не зависит от внешней среды.
11. Закон гомологических рядов наследственной изменчивости утверждает, что генетически близкородственные виды:
а) обладают сходной наследственной изменчивостью
б) мутируют с одинаковой частотой
в) обладают одинаковыми генотипами
г) мутируют чаще, чем родственные виды.
12. Мутации, приводящие к изменению числа хромосом:
а) генные б) геномные в) хромосомные г) соматические.
13. Признак, наследуемый сцепленно с полом:
а) острота зрения б) свёртываемость крови
б) форма волос г) число пальцев.
14. Женская гетерогаметность имеет место у:
а) дрозофиллы б) человека в) вороны г) кошки.
Оценочная шкала
Вариант 1
№
Эталон ответа
Баллы
1
А
4
2
Б
5
3
В
4
4
А
4
5
В
5
6
Б
5
7
В
4
8
А
5
9
А
4
10
Б
5
11
А
5
12
В
5
13
А
5
14
Б
5
Максимальные баллы
65
ЗАДАНИЕ
ЭТАЛОН ОТВЕТА
БАЛЛЫ
1. Вещество SO3 -
1) кислотный оксид
2) основный оксид
3) амфотерный оксид
4) несолеобразующий оксид
1
2
2. В каком ряду записаны формулы только тех веществ, которые взаимодействуют с соляной кислотой?
1) Na2CO3; Cu; Na2O; Zn(OH)2
2) CO2; Al(OH)3; Ba(OH)2; Fe
3) Zn; CaO; KOH; AgNO3
4) Pb(NO3)2; Ca(OH)2; SO3; HNO3
3
2
3. Свойства веществ зависят не только от состава, но и от
1) условий получения вещества
2) порядка связи атомов в соединении
3) валентности химических элементов
4) агрегатного состояния вещества
2
2
4. Вещество CH2-CH-CH2 относится к классу
| | |
OH OH OH
1) спиртов
2) многоатомных спиртов
3) альдегидов
4) карбоновых кислот
2
2
5. В веществе CH3-CH2-OH связь между атомами углерода
1) ковалентная неполярная
2) ковалентная полярная
3) ионная
4) водородная
1
2
6. Степень окисления атома серы в веществе (NH4)2SO4 равна
1) -2
2) 0
3) +4
4) +6
4
2
7. Какое из перечисленных веществ образует атомную кристаллическую решетку?
1) кислород
2) бром
3) азот
4) бор
4
2
8. На скорость химической реакции не оказывает влияние
1) концентрация вещества в растворе или концентрация газа
2) площадь поверхности твердого вещества
3) условия хранения реактивов
4) температура проведения реакции
3
2
9. Окислительно-восстановительной реакции соответствует уравнение
1) KOH + HCl = KCl + H2O
2) CH2=CH2 + HCl CH3-CH2Cl
3) CuO + 2HCl = CuCl2 + H2O
4) CH3-CH2OH + HCl CH3-CH2Cl + H2O
2
2
10. В каком ряду знаки химических элементов расположены в порядке увеличения атомных радиусов?
1) C N O F
2) Sr Ca Mg Be
3) Na Al P Cl
4) Si Al Mg Na
11. Термин «молекула» нельзя употреблять при характеристике строения
1) сероводорода
2) азотной кислоты
3) озона
4) фторида кальция
4
2
12. Простым веществом является
1) H2S
2) S8
3) SO2
4) H2SO4
4
2
13. Вещество состава C4H10O имеет
1) 7 изомеров
2) 6 изомеров
3) 4 изомера
4) 2 изомера
2
2
14. Если оксид растворяется в воде, то
1) это основный оксид
2) это кислотный оксид
3) это амфотерный оксид
4) на основании этих данных нельзя сделать вывод о кислотно-основных свойствах оксида
1
2
15. В результате реакции пропена с водой образуется
1) пропаналь
2) пропанол-1
3) пропанол-2
4) ацетон
4
2
16. Атом углерода карбоксильной группы находится в гибридном состоянии
1) sp
2) sp2
3) sp3
4) sp3d2
2
2
17. Степень диссоциации не зависит от
1) объема раствора
2) природы электролита
3) растворителя
4) концентрации
1
2
18. Веществом, вступившим в реакцию, сокращенное ионное уравнение которой
… + 2H+ = Cu2+ + 2H2O, является
1) нитрат меди(II)
2) карбонат меди(II)
3) гидроксид меди(II)
4) хлорид меди(II)
3
2
19. В уравнении реакции горения ацетилена коэффициент перед формулой окислителя равен
1) 5
2) 2
3) 3
4) 4
1
2
20. Молекулы какого из перечисленных веществ имеют наименьшую энергию связи?
1) HI
2) HCl
3) HF
4) HBr
1
2
21. Электроны атома фосфора, находящегося в основном состоянии, расположены на орбиталях так:
1) 5s25p5
2) 3s23p5
3) 3s23p3
4) 5s25p3
3
2
22. Различие в значении температур плавления CO2 (- 56,6оС) и SiO2 (1728оС) объясняется
1) различиями в строении атомов углерода и кремния
2) различием в значениях масс молекул
3) разным видом химической связи
4) разным типом кристаллической решетки
4
2
23. Изомерами не являются
1) циклобутан и 2-метилпропан
2) пентен-1 и метилциклобутан
3) бутадиен-1,3 и бутин-1
4) гексан и 2,3-диметилбутан
1
2
24. Сокращенное ионное уравнение реакции между водными растворами хлорида кальция и карбоната натрия
1) CaCl2 + 2Na+ = 2NaCl + Ca2+
2) Ca2+ + Na2CO3 = CaCO3 + 2Na+
3) Ca2+ + CO32- = CaCO3
4) Ca2+ + 2Cl- + 2Na+ + CO32- = 2NaCl + CaCO3
3
2
25. Жиры состоят из фрагментов молекул
1) этиленгликоля и высших карбоновых кислот
2) глицерина и высших карбоновых кислот
3) глицерина и альдегидов
4) этиленгликоля и альдегидов
2
2
26. Какой из перечисленных химических элементов образует только одно простое вещество?
1) водород
2) углерод
3) кислород
4) фосфор
1
2
27. Вещество HCl
1) может быть только окислителем
2) может быть только восстановителем
3) может быть и окислителем, и восстановителем
4) не вступает в окислительно-восстановительные реакции
3
2
28. Амфотерными свойствами обладает оксид элемента, расположенного в
1) IV периоде и побочной подгруппе II группы
2) V периоде и побочной подгруппе I группы
3) III периоде и главной подгруппе II группы
4) II периоде и главной подгруппе I группы
1
2
29. Максимальная валентность азота равна
1) II
2) III
3) IV
4) V
3
2
30. Согласно современным представлениям, периодическое изменение свойств химических элементов зависит от
1) массы ядра атома
2) массы атома
3) заряда атома
4) заряда ядра атома
4
2
31. В основном состоянии наибольшее число неспаренных электронов - в атоме
1) серы
2) кремния
3) хлора
4) фосфора
4
2
32. Закон постоянства состава веществ
1) справедлив для всех веществ
2) справедлив для веществ молекулярного строения
3) справедлив для веществ немолекулярного строения
4) оказался ошибочным
2
2
33. В ряду углеводородов этан - этен - этин длина связи С-С
1) увеличивается
2) уменьшается
3) не изменяется
4) от этана к этену увеличивается, от этена к этину уменьшается
2
2
34. Если к толуолу добавить бром, то
1) образуется вещество 3,5-дибромтолуол
2) образуется вещество бромфенилметан
3) образуется вещество строения 2,4,6-трибромтолуол
4) реакция между веществами не пойдет
3
2
35. Общая формула вторичных аминов
1) R-C-NH2
|
2) R-N-R
|
H
3) H2N-R-NH2
4) R-N=N-R
2
2
№
задания
Ответ
№
задания
Ответ
№
задания
Ответ
1
1
16
2
31
4
2
3
17
1
32
2
3
2
18
3
33
2
4
2
19
1
34
3
5
1
20
1
35
2
6
4
21
3
7
4
22
4
8
3
23
1
9
2
24
3
10
4
25
2
11
4
26
1
12
2
27
3
13
1
28
1
14
4
29
3
15
3
30
4
2 вариант
Инструкция для обучающихся
При выполнении заданий укажите цифру правильного ответа.
Внимательно прочитайте задание.
Время выполнения задания - 40 мин.
2 вариант:
ЗАДАНИЕ
ЭТАЛОН ОТВЕТА
БАЛЛЫ
1. Сумма протонов, нейтронов и электронов в атоме 40Са равна
1)
40
2)
60
3)
30
4)
50
2
2
2. Электронная конфигурация 1s22s22p63s23p6 соответствует иону
1)
Sc2+
2)
Al3+
3)
Cr3+
4)
Ca2+
4
2
3. В молекуле аммиака NH3 химическая связь
1)
ионная
2)
ковалентная неполярная
3)
ковалентная полярная
4)
водородная
3
2
4. Степень окисления элемента в высшем оксиде равна + 6, а в водородном соединении его степень окисления равна
1)
- 2
2)
+ 2
3)
+ 6
4)
- 6
1
2
5. Молекулярную кристаллическую решетку имеет соединение
1)
HBr
2)
Li2O
3)
BaO
4)
KCl
1
2
6. Аллотропные модификации кислорода не отличаются
1)
физическими свойствами
2)
типом химической связи между атомами
3)
химическими свойствами
4)
числом атомов, входящих в состав молекул
2
2
7. Из приведенных ниже металлов наиболее активным является
1)
бериллий
2)
магний
3)
кальций
4)
барий
4
2
8.
2
2
9. Элемент, образующий водородное соединение с наиболее сильными оснóвными свойствами - это
1)
C
2)
N
3)
F
4)
O
2
2
10. В ряду F2 - Cl2 - Br2 - I2
окислительная активность
1)
увеличивается
2)
уменьшается
3)
не изменяется
4)
изменяется периодически
2
2
11. Водные растворы серной и азотной кислот можно различить с помощью
1)
Cu
2)
MgO
3)
Fe(OH)3
4)
Na2CO3
1
2
12. В цепочке превращений
Сa 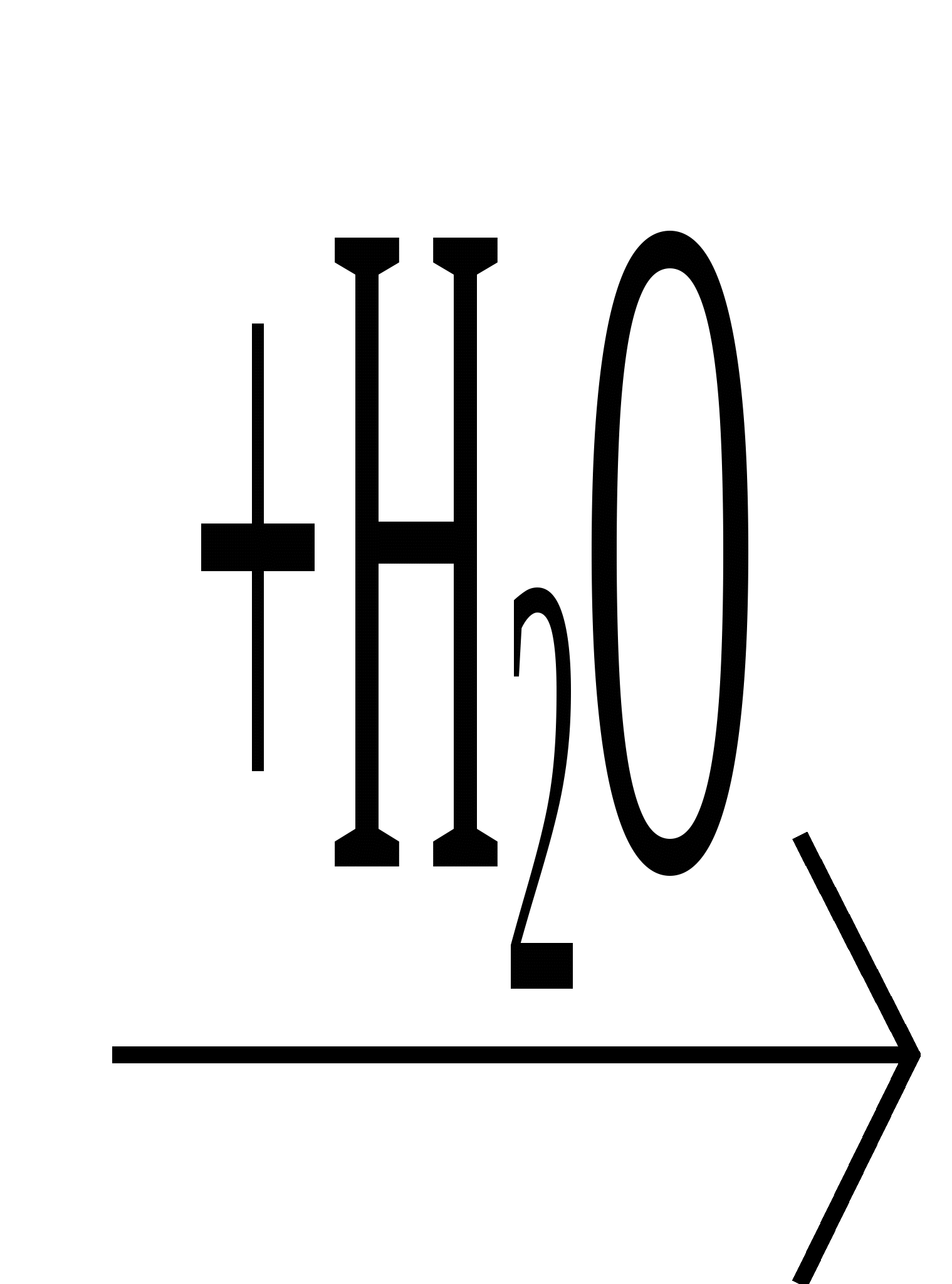 X1
X1 X2
X2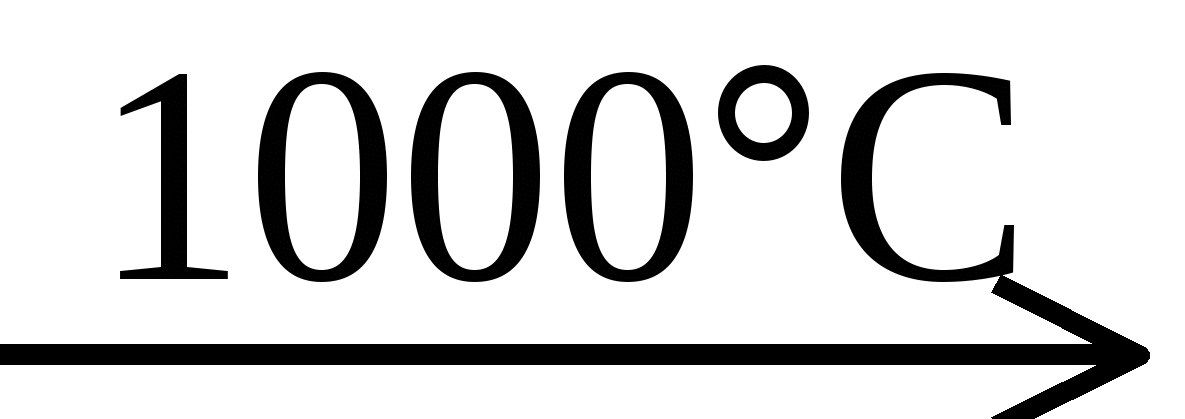 X3
X3
конечным продуктом «Х3» является
1)
CaO
2)
CaСО3
3)
CaH2
4)
CaC2
1
2
13.
2
2
14.
3
2
15. Жидкий углеводород, молекула которого при жестком УФ освещении присоединяет шесть атомов хлора, а в присутствии железа с хлором образует монохлорпроизводное, называется
1)
пропеном
2)
бензолом
3)
гексаном
4)
метилциклопентаном
2
2
16.
1
2
17.
Вещество, которое может реагировать с уксусной кислотой и с этаналем, имеет формулу
1)
NaOH
2)
Cu(OH)2
3)
CH4
4)
HBr
2
2
18. Сложный эфир можно получить при взаимодействии уксусной кислоты с
1)
пропеном
2)
метанолом
3)
диэтиловым эфиром
4)
муравьиной кислотой
2
2
19. Углевод, для которого характерна реакция «серебряного зеркала», - это
1)
сахароза
2)
крахмал
3)
фруктоза
4)
глюкоза
4
2
20.
3
2
21. Аминоуксусная кислота реагирует с каждым из двух веществ:
1)
HСl, KOH
2)
NaCl, NH3
3)
C2H5OH, KCl
4)
CO2, HNO3
1
2
22. Аминоуксусная кислота реагирует с каждым из двух веществ:
1)
HСl, KOH
2)
NaCl, NH3
3)
C2H5OH, KCl
4)
CO2, HNO3
2
2
23. Реакция, уравнение которой
CaCO3 (к) CaO (к) + CO2 (г) - Q,
CaO (к) + CO2 (г) - Q,
относится к реакциям
1)
соединения, экзотермическим
2)
разложения, эндотермическим
3)
соединения, эндотермическим
4)
разложения, экзотермическим
1
2
24. При комнатной температуре с наибольшей скоростью протекает реакция между
1)
NaOH(р-р) и HCl(р-р)
2)
CuO(тв.) и H2SO4 (р-р)
3)
CaCO3 (тв.) и HCl(р-р)
4)
Zn(тв.) и H2SO4 (р-р)
3
2
25.
Согласно термохимическому уравнению
C2H4 + H2![]() C2H6 + 311,4 кДж
C2H6 + 311,4 кДж
можно утверждать, что при образовании 2 моль этана
1)
выделяется 311,4 кДж теплоты
2)
поглощается 311,4 кДж теплоты
3)
выделяется 622,8 кДж теплоты
4)
поглощается 622,8 кДж теплоты
4
2
26. Химическое равновесие в системе
CO2 (г) + C (тв)  2CO (г) - Q
2CO (г) - Q
сместится вправо при
1)
повышении давления
2)
понижении температуры
3)
повышении концентрации СO
4)
повышении температуры
4
2
27.
1
2
28.
3
2
29.
Только окислительные свойства проявляет
1)
сульфид натрия
2)
сера
3)
серная кислота
4)
сульфит калия
2
2
30. При пропускании избытка пропилена через бромную воду наблюдается
1)
выпадение осадка
2)
обесцвечивание раствора
3)
синее окрашивание раствора
4)
пожелтение раствора
4
2
31.
При щелочном гидролизе 1,2-дихлорпропана образуется
1)
пропанол-1
3)
пропанол-2
2)
пропаналь
4)
пропандиол-1,2
1
2
32.
1
2
33. Присоединение HCl к метилпропену, в соответствии с правилом В.В. Марковникова, приводит к образованию
1)
2-метил-2-хлорпропана
2)
2-метил-1-хлорпропана
3)
2-метил-2-хлорпропена
4)
2-метил-1-хлорпропена
2
2
34. Реактивами для получения водорода и кислорода в лаборатории могут быть, соответственно, следующие вещества:
1)
Cu и HCl; KClO3
2)
Zn и HCl; KMnO4
3)
H2O2; HgO
4)
HCl; Na2O
1
2
35.
4
2
№ задания
Ответ
№ задания
Ответ
№ задания
Ответ
1
2
13
2
25
4
2
4
14
3
26
4
3
3
15
2
27
1
4
1
16
1
28
3
5
1
17
2
29
2
6
2
18
2
30
4
7
4
19
4
31
1
8
2
20
3
32
1
9
2
21
1
33
2
10
2
22
2
34
1
11
1
23
1
35
4
12
1
24
3
Вариант-2.
ЗАДАНИЕ
ЭТАЛОН ОТВЕТА
БАЛЛЫ
1. Ген человека- это часть:
а) молекулы белка б) углевода
в) ДНК г) и-РНК.
2.Генотип организма-это:
а) проявляющиеся внешние и внутренние признаки организма
б) наследственные признаки организма
в) способность организма к изменениям
г) передача признака от поколения к поколению
3. Чистой линией называется:
а) потомство, не дающее разнообразия по изучаемому признаку
б) разнообразное потомство, полученное от скрещивания разных особей
в) пара родителей, отличающихся друг от друга одним признаком
г) особи одноговида.
4. Гомозигота - это пара только:
а) рецессивных аллельных генов б) доминантных аллельных генов
в) неаллельных генов г) одинаковых по проявлению аллельных генов.
5. Локус -это:
а) пара аллельных генов б) пара неаллельных генов
в) сцепленные гены г) место расположения гена на хромосоме.
6.Заслуга Г. Менделя заключается в выявлении:
а) распределения хромосом по гаметам в процессе мейоза
б) закономерностей наследования родительских признаков
в) изучение сцепленного наследования
г) выявлении взаимосвязи генетики и эволюции.
7.Гибридологический метод Г. Менделя основан на:
а) межвидовом скрещивании растений гороха
б) выращивании растений в различных условиях
в) скрещивании разных сортов гороха, отличающихся по определённым признакам
г) цитологическом анализе хромосомного набора.
8.Анализирующее скрещивание проводят для:
а) выявление доминантного аллеля
б) того, чтобы выяснить, какой аллель рецессивен
в) выведения чистой линии
г) обнаружения гетерозиготности организма по определённому признаку.
9.Не наследуется изменчивость:
а) цитоплазматическая б) комбинативная в) фенотипическая г) мутационная
10.Признаки, степень выраженности которых плавно варьирует в определённых граниуах:
а) качественные б) количественные в) полуколичественные г) неопределённые.
11.Пол, образующий гаметы, различающиеся по половой хромосоме:
а) гомогаметный б) гетерозиготный в) гомозиготный г) гетерогаметный
12. Геномные - это мутации:
А
) происходящие в гене б) изменяющие внутреннюю структуру хромосом
в) изменяющие число хромосом
г) изменяющие генотип соматических клеток.
13.Различия в размерах листьев одного дерева-это пример изменчивости:
а) генотипической б) модификационной в) мутационной г) комбинативной.
14.Гены, определяющие развитие альтернативных состояний признака:
а) доминантные б) аллельные в) рецессивные г) мутантные.
Оценочная шкала
Вариант 2
№
Эталон ответа
Баллы
1
А
4
2
Б
5
3
В
4
4
А
4
5
В
5
6
Б
5
7
В
4
8
А
5
9
А
4
10
Б
5
11
Б
5
12
А
5
13
Б
5
14
В
5
Максимальные баллы
65
III. ПАКЕТ ЭКЗАМЕНАТОРА
III а. УСЛОВИЯ
Количество вариантов задания для экзаменующегося - 2
Время выполнения задания - 40 мин.
Вариант 1
ЗАДАНИЕ
ЭТАЛОН ОТВЕТА
БАЛЛЫ
1. Выбрать правильный ответ.
1.Генетика-это наука о:
а) селекции организмов б) наследственности и изменчивости организмов
в) эволюции органического мира г) генной инженерии.
А
4
2. Ген кодирует информацию о структуре:
а) молекулы аминокислоты б) одной молекулы т-РНК
в) одной молекулы фермента г) нескольких молекул белка.
Б
5
3. Фенотип организма-это:
а) проявляющиеся внешние и внутренние признаки
б) наследственные признаки организма
в) способность организма к изменениям
г) передача признака от поколения к поколению.
В
4
4. Аллельными считаются следующие пары генов:
а) рост человека-форма его носа б) карие глаза- голубые глаза
в) рогатость коров-окраска коров г) чёрная шерсть- гладкая шерсть.
А
4
5. Гетерозигота-это пара:
а) аллельных доминантных генов
б) неаллельных доминантного и рецессивного генов
в) аллельных доминантного и рецессивного генов
г) аллельных рецессивных генов.
В
5
6. Потомство, рождающееся от одного самоопыляющегося растения в течении нескольких лет, называется:
а) доминантным б) гибридным в) рецессивным г) чистой линией.
Б
5
7. Наследственность- это свойство организмов, которое обеспечивает:
а) внутривидовое сходство организмов
б) различия между особями внутри вида
в) межвидовое сходство организмов
г) изменения организмов в течение жизни.
В
4
8. В каком случае приведены примеры анализирующего скрещивания:
а) ВВ х Вв и вв х вв б) Аа х аа и АА х аа
в) Сс х Сс и сс х сс г) DD x Dd и DD x DD
А
5
9. Явление сцепленного наследования получило название:
а) третьего закона Менделя б) гипотезы чистоты гамет
в) кроссинговера г) закона Моргана.
А
4
10. Модификационная изменчивость:
а) наследуется б) связана с изменениеми генотипа
в) не наследуется г) не зависит от внешней среды.
Б
5
11. Закон гомологических рядов наследственной изменчивости утверждает, что генетически близкородственные виды:
а) обладают сходной наследственной изменчивостью
б) мутируют с одинаковой частотой
в) обладают одинаковыми генотипами
г) мутируют чаще, чем родственные виды.
А
5
12. Мутации, приводящие к изменению числа хромосом:
а) генные б) геномные в) хромосомные г) соматические.
В
5
13. Признак, наследуемый сцепленно с полом:
а) острота зрения б) свёртываемость крови
б) форма волос г) число пальцев.
А
5
14. Женская гетерогаметность имеет место у:
а) дрозофиллы б) человека в) вороны г) кошки.
Б
5
ЗАДАНИЕ
ЭТАЛОН ОТВЕТА
БАЛЛЫ
1. Вещество SO3 -
1) кислотный оксид
2) основный оксид
3) амфотерный оксид
4) несолеобразующий оксид
1
2
2. В каком ряду записаны формулы только тех веществ, которые взаимодействуют с соляной кислотой?
1) Na2CO3; Cu; Na2O; Zn(OH)2
2) CO2; Al(OH)3; Ba(OH)2; Fe
3) Zn; CaO; KOH; AgNO3
4) Pb(NO3)2; Ca(OH)2; SO3; HNO3
3
2
3. Свойства веществ зависят не только от состава, но и от
1) условий получения вещества
2) порядка связи атомов в соединении
3) валентности химических элементов
4) агрегатного состояния вещества
2
2
4. Вещество CH2-CH-CH2 относится к классу
| | |
OH OH OH
1) спиртов
2) многоатомных спиртов
3) альдегидов
4) карбоновых кислот
2
2
5. В веществе CH3-CH2-OH связь между атомами углерода
1) ковалентная неполярная
2) ковалентная полярная
3) ионная
4) водородная
1
2
6. Степень окисления атома серы в веществе (NH4)2SO4 равна
1) -2
2) 0
3) +4
4) +6
4
2
7. Какое из перечисленных веществ образует атомную кристаллическую решетку?
1) кислород
2) бром
3) азот
4) бор
4
2
8. На скорость химической реакции не оказывает влияние
1) концентрация вещества в растворе или концентрация газа
2) площадь поверхности твердого вещества
3) условия хранения реактивов
4) температура проведения реакции
3
2
9. Окислительно-восстановительной реакции соответствует уравнение
1) KOH + HCl = KCl + H2O
2) CH2=CH2 + HCl CH3-CH2Cl
3) CuO + 2HCl = CuCl2 + H2O
4) CH3-CH2OH + HCl CH3-CH2Cl + H2O
2
2
10. В каком ряду знаки химических элементов расположены в порядке увеличения атомных радиусов?
1) C N O F
2) Sr Ca Mg Be
3) Na Al P Cl
4) Si Al Mg Na
11. Термин «молекула» нельзя употреблять при характеристике строения
1) сероводорода
2) азотной кислоты
3) озона
4) фторида кальция
4
2
12. Простым веществом является
1) H2S
2) S8
3) SO2
4) H2SO4
4
2
13. Вещество состава C4H10O имеет
1) 7 изомеров
2) 6 изомеров
3) 4 изомера
4) 2 изомера
2
2
14. Если оксид растворяется в воде, то
1) это основный оксид
2) это кислотный оксид
3) это амфотерный оксид
4) на основании этих данных нельзя сделать вывод о кислотно-основных свойствах оксида
1
2
15. В результате реакции пропена с водой образуется
1) пропаналь
2) пропанол-1
3) пропанол-2
4) ацетон
4
2
16. Атом углерода карбоксильной группы находится в гибридном состоянии
1) sp
2) sp2
3) sp3
4) sp3d2
2
2
17. Степень диссоциации не зависит от
1) объема раствора
2) природы электролита
3) растворителя
4) концентрации
1
2
18. Веществом, вступившим в реакцию, сокращенное ионное уравнение которой
… + 2H+ = Cu2+ + 2H2O, является
1) нитрат меди(II)
2) карбонат меди(II)
3) гидроксид меди(II)
4) хлорид меди(II)
3
2
19. В уравнении реакции горения ацетилена коэффициент перед формулой окислителя равен
1) 5
2) 2
3) 3
4) 4
1
2
20. Молекулы какого из перечисленных веществ имеют наименьшую энергию связи?
1) HI
2) HCl
3) HF
4) HBr
1
2
21. Электроны атома фосфора, находящегося в основном состоянии, расположены на орбиталях так:
1) 5s25p5
2) 3s23p5
3) 3s23p3
4) 5s25p3
3
2
22. Различие в значении температур плавления CO2 (- 56,6оС) и SiO2 (1728оС) объясняется
1) различиями в строении атомов углерода и кремния
2) различием в значениях масс молекул
3) разным видом химической связи
4) разным типом кристаллической решетки
4
2
23. Изомерами не являются
1) циклобутан и 2-метилпропан
2) пентен-1 и метилциклобутан
3) бутадиен-1,3 и бутин-1
4) гексан и 2,3-диметилбутан
1
2
24. Сокращенное ионное уравнение реакции между водными растворами хлорида кальция и карбоната натрия
1) CaCl2 + 2Na+ = 2NaCl + Ca2+
2) Ca2+ + Na2CO3 = CaCO3 + 2Na+
3) Ca2+ + CO32- = CaCO3
4) Ca2+ + 2Cl- + 2Na+ + CO32- = 2NaCl + CaCO3
3
2
25. Жиры состоят из фрагментов молекул
1) этиленгликоля и высших карбоновых кислот
2) глицерина и высших карбоновых кислот
3) глицерина и альдегидов
4) этиленгликоля и альдегидов
2
2
26. Какой из перечисленных химических элементов образует только одно простое вещество?
1) водород
2) углерод
3) кислород
4) фосфор
1
2
27. Вещество HCl
1) может быть только окислителем
2) может быть только восстановителем
3) может быть и окислителем, и восстановителем
4) не вступает в окислительно-восстановительные реакции
3
2
28. Амфотерными свойствами обладает оксид элемента, расположенного в
1) IV периоде и побочной подгруппе II группы
2) V периоде и побочной подгруппе I группы
3) III периоде и главной подгруппе II группы
4) II периоде и главной подгруппе I группы
1
2
29. Максимальная валентность азота равна
1) II
2) III
3) IV
4) V
3
2
30. Согласно современным представлениям, периодическое изменение свойств химических элементов зависит от
1) массы ядра атома
2) массы атома
3) заряда атома
4) заряда ядра атома
4
2
31. В основном состоянии наибольшее число неспаренных электронов - в атоме
1) серы
2) кремния
3) хлора
4) фосфора
4
2
32. Закон постоянства состава веществ
1) справедлив для всех веществ
2) справедлив для веществ молекулярного строения
3) справедлив для веществ немолекулярного строения
4) оказался ошибочным
2
2
33. В ряду углеводородов этан - этен - этин длина связи С-С
1) увеличивается
2) уменьшается
3) не изменяется
4) от этана к этену увеличивается, от этена к этину уменьшается
2
2
34. Если к толуолу добавить бром, то
1) образуется вещество 3,5-дибромтолуол
2) образуется вещество бромфенилметан
3) образуется вещество строения 2,4,6-трибромтолуол
4) реакция между веществами не пойдет
3
2
35. Общая формула вторичных аминов
1) R-C-NH2
|
2) R-N-R
|
H
3) H2N-R-NH2
4) R-N=N-R
2
2
2 вариант
Инструкция для обучающихся
При выполнении заданий укажите цифру правильного ответа.
Внимательно прочитайте задание.
Время выполнения задания - 40 мин.
ЗАДАНИЕ
ЭТАЛОН ОТВЕТА
БАЛЛЫ
1. Ген человека- это часть:
а) молекулы белка б) углевода
в) ДНК г) и-РНК.
А
4
2.Генотип организма-это:
а) проявляющиеся внешние и внутренние признаки организма
б) наследственные признаки организма
в) способность организма к изменениям
г) передача признака от поколения к поколению
Б
5
3. Чистой линией называется:
а) потомство, не дающее разнообразия по изучаемому признаку
б) разнообразное потомство, полученное от скрещивания разных особей
в) пара родителей, отличающихся друг от друга одним признаком
г) особи одноговида.
В
4
4. Гомозигота - это пара только:
а) рецессивных аллельных генов б) доминантных аллельных генов
в) неаллельных генов г) одинаковых по проявлению аллельных генов.
А
4
5. Локус -это:
а) пара аллельных генов б) пара неаллельных генов
в) сцепленные гены г) место расположения гена на хромосоме.
В
5
6.Заслуга Г. Менделя заключается в выявлении:
а) распределения хромосом по гаметам в процессе мейоза
б) закономерностей наследования родительских признаков
в) изучение сцепленного наследования
г) выявлении взаимосвязи генетики и эволюции.
Б
5
7.Гибридологический метод Г. Менделя основан на:
а) межвидовом скрещивании растений гороха
б) выращивании растений в различных условиях
в) скрещивании разных сортов гороха, отличающихся по определённым признакам
г) цитологическом анализе хромосомного набора.
В
4
8.Анализирующее скрещивание проводят для:
а) выявление доминантного аллеля
б) того, чтобы выяснить, какой аллель рецессивен
в) выведения чистой линии
г) обнаружения гетерозиготности организма по определённому признаку.
А
5
9.Не наследуется изменчивость:
а) цитоплазматическая б) комбинативная в) фенотипическая г) мутационная
А
4
10.Признаки, степень выраженности которых плавно варьирует в определённых граниуах:
а) качественные б) количественные в) полуколичественные г) неопределённые.
Б
5
11.Пол, образующий гаметы, различающиеся по половой хромосоме:
а) гомогаметный б) гетерозиготный в) гомозиготный г) гетерогаметный
Б
5
12. Геномные - это мутации:
А
) происходящие в гене б) изменяющие внутреннюю структуру хромосом
в) изменяющие число хромосом
г) изменяющие генотип соматических клеток.
А
5
13.Различия в размерах листьев одного дерева-это пример изменчивости:
а) генотипической б) модификационной в) мутационной г) комбинативной.
Б
5
14.Гены, определяющие развитие альтернативных состояний признака:
а) доминантные б) аллельные в) рецессивные г) мутантные.
В
5
ЗАДАНИЕ
ЭТАЛОН ОТВЕТА
БАЛЛЫ
1. Сумма протонов, нейтронов и электронов в атоме 40Са равна
1)
40
2)
60
3)
30
4)
50
2
2
2. Электронная конфигурация 1s22s22p63s23p6 соответствует иону
1)
Sc2+
2)
Al3+
3)
Cr3+
4)
Ca2+
4
2
3. В молекуле аммиака NH3 химическая связь
1)
ионная
2)
ковалентная неполярная
3)
ковалентная полярная
4)
водородная
3
2
4. Степень окисления элемента в высшем оксиде равна + 6, а в водородном соединении его степень окисления равна
1)
- 2
2)
+ 2
3)
+ 6
4)
- 6
1
2
5. Молекулярную кристаллическую решетку имеет соединение
1)
HBr
2)
Li2O
3)
BaO
4)
KCl
1
2
6. Аллотропные модификации кислорода не отличаются
1)
физическими свойствами
2)
типом химической связи между атомами
3)
химическими свойствами
4)
числом атомов, входящих в состав молекул
2
2
7. Из приведенных ниже металлов наиболее активным является
1)
бериллий
2)
магний
3)
кальций
4)
барий
4
2
8.
2
2
9. Элемент, образующий водородное соединение с наиболее сильными оснóвными свойствами - это
1)
C
2)
N
3)
F
4)
O
2
2
10. В ряду F2 - Cl2 - Br2 - I2
окислительная активность
1)
увеличивается
2)
уменьшается
3)
не изменяется
4)
изменяется периодически
2
2
11. Водные растворы серной и азотной кислот можно различить с помощью
1)
Cu
2)
MgO
3)
Fe(OH)3
4)
Na2CO3
1
2
12. В цепочке превращений
Сa 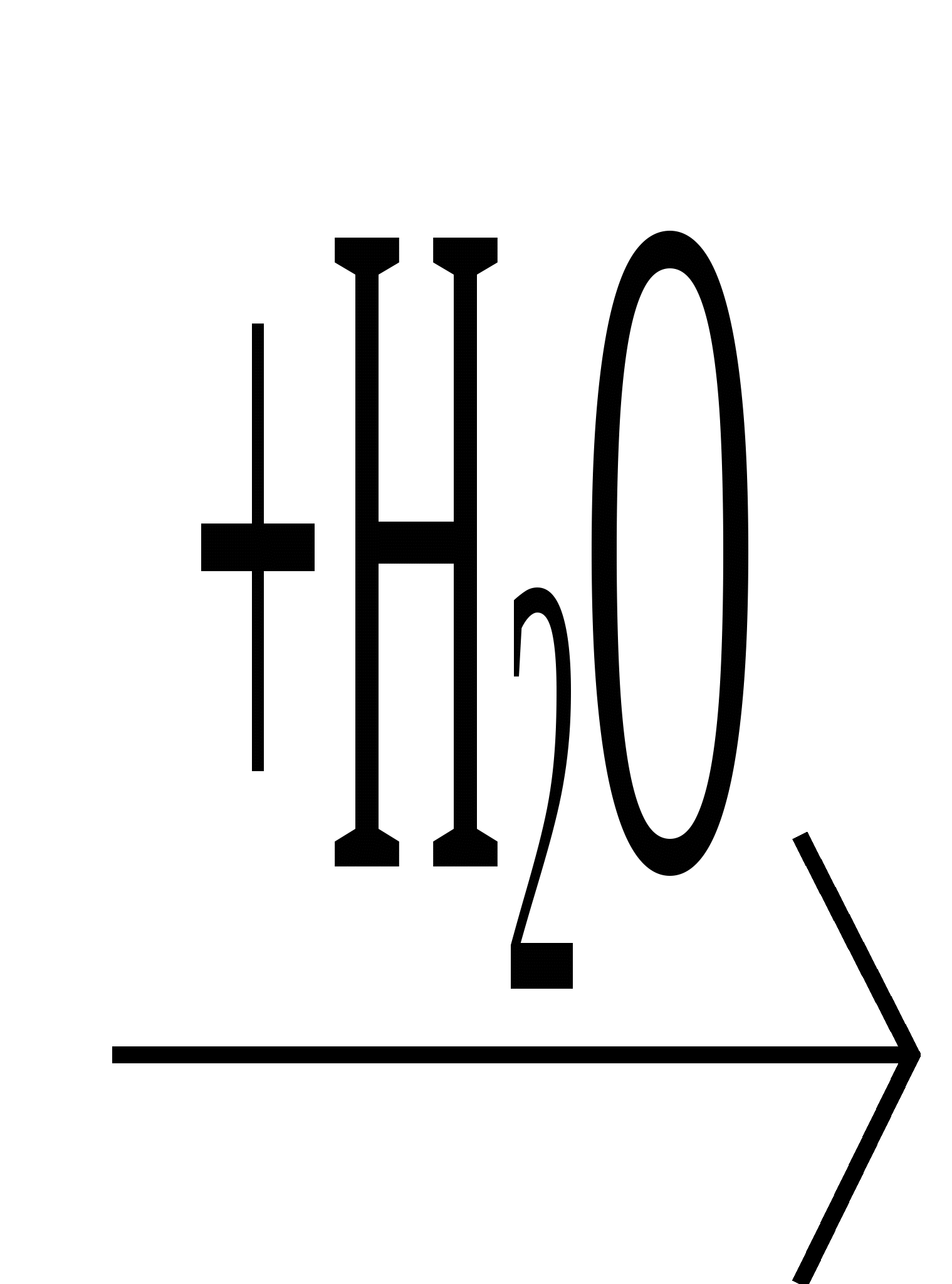 X1
X1 X2
X2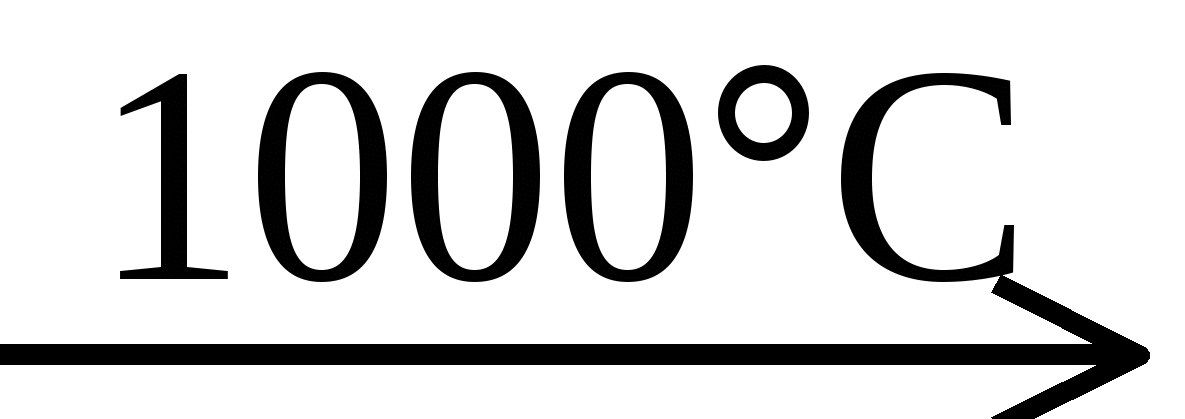 X3
X3
конечным продуктом «Х3» является
1)
CaO
2)
CaСО3
3)
CaH2
4)
CaC2
1
2
13.
2
2
14.
3
2
15. Жидкий углеводород, молекула которого при жестком УФ освещении присоединяет шесть атомов хлора, а в присутствии железа с хлором образует монохлорпроизводное, называется
1)
пропеном
2)
бензолом
3)
гексаном
4)
метилциклопентаном
2
2
16.
1
2
17.
Вещество, которое может реагировать с уксусной кислотой и с этаналем, имеет формулу
1)
NaOH
2)
Cu(OH)2
3)
CH4
4)
HBr
2
2
18. Сложный эфир можно получить при взаимодействии уксусной кислоты с
1)
пропеном
2)
метанолом
3)
диэтиловым эфиром
4)
муравьиной кислотой
2
2
19. Углевод, для которого характерна реакция «серебряного зеркала», - это
1)
сахароза
2)
крахмал
3)
фруктоза
4)
глюкоза
4
2
20.
3
2
21. Аминоуксусная кислота реагирует с каждым из двух веществ:
1)
HСl, KOH
2)
NaCl, NH3
3)
C2H5OH, KCl
4)
CO2, HNO3
1
2
22. Аминоуксусная кислота реагирует с каждым из двух веществ:
1)
HСl, KOH
2)
NaCl, NH3
3)
C2H5OH, KCl
4)
CO2, HNO3
2
2
23. Реакция, уравнение которой
CaCO3 (к) CaO (к) + CO2 (г) - Q,
CaO (к) + CO2 (г) - Q,
относится к реакциям
1)
соединения, экзотермическим
2)
разложения, эндотермическим
3)
соединения, эндотермическим
4)
разложения, экзотермическим
1
2
24. При комнатной температуре с наибольшей скоростью протекает реакция между
1)
NaOH(р-р) и HCl(р-р)
2)
CuO(тв.) и H2SO4 (р-р)
3)
CaCO3 (тв.) и HCl(р-р)
4)
Zn(тв.) и H2SO4 (р-р)
3
2
25.
Согласно термохимическому уравнению
C2H4 + H2![]() C2H6 + 311,4 кДж
C2H6 + 311,4 кДж
можно утверждать, что при образовании 2 моль этана
1)
выделяется 311,4 кДж теплоты
2)
поглощается 311,4 кДж теплоты
3)
выделяется 622,8 кДж теплоты
4)
поглощается 622,8 кДж теплоты
4
2
26. Химическое равновесие в системе
CO2 (г) + C (тв)  2CO (г) - Q
2CO (г) - Q
сместится вправо при
1)
повышении давления
2)
понижении температуры
3)
повышении концентрации СO
4)
повышении температуры
4
2
27.
1
2
28.
3
2
29.
Только окислительные свойства проявляет
1)
сульфид натрия
2)
сера
3)
серная кислота
4)
сульфит калия
2
2
30. При пропускании избытка пропилена через бромную воду наблюдается
1)
выпадение осадка
2)
обесцвечивание раствора
3)
синее окрашивание раствора
4)
пожелтение раствора
4
2
31.
При щелочном гидролизе 1,2-дихлорпропана образуется
1)
пропанол-1
3)
пропанол-2
2)
пропаналь
4)
пропандиол-1,2
1
2
32.
1
2
33. Присоединение HCl к метилпропену, в соответствии с правилом В.В. Марковникова, приводит к образованию
1)
2-метил-2-хлорпропана
2)
2-метил-1-хлорпропана
3)
2-метил-2-хлорпропена
4)
2-метил-1-хлорпропена
2
2
34. Реактивами для получения водорода и кислорода в лаборатории могут быть, соответственно, следующие вещества:
1)
Cu и HCl; KClO3
2)
Zn и HCl; KMnO4
3)
H2O2; HgO
4)
HCl; Na2O
1
2
35.
4
2
1


