- Преподавателю
- Другое
- Основные конструктивные типы промышленных реакторов
Основные конструктивные типы промышленных реакторов
| Раздел | Другое |
| Класс | - |
| Тип | Конспекты |
| Автор | Закирова Е.А. |
| Дата | 25.09.2015 |
| Формат | doc |
| Изображения | Есть |
Основные конструктивные типы промышленных реакторов.
Многолетний опыт и научные изыскания позволили к настоящему времени разработать несколько основных конструктивных типов химических реакторов. Эти базовые конструкции также лежат в основе устройства более сложных реакторов.
Принципиальная общность конструктивных решений в реакторах каждого класса определяется их назначением, т.е. в первую очередь фазовым состоянием реакционной системы и температурным режимом ХП. В каждом классе существует много конкретных вариантов конструктивного исполнения аппарата.
Таблица 2- Основные конструктивные типы реакторов, применяемых в производствах ТОС
Конструктивный
тип реактора
Область и условия применения
Фазовое
состояние
систем
Температура
и давление
(конструктивные)
Тип процесса
1. Реактгоры-котлы. (Ёмкостные с перемешивающими устройствами).
В отраслях ТОС
≈ 95% всего парка реакторов
Ж
Ж-Ж
Г-Ж
Ж-Т
Г-Ж-Т
T =[ (-80)…400]OC
P=[(-0,001)…40] МПа
Разнообразные каталитические и нека-талитические процессы в конденсированных средах с интенсивным перемешиванием и теплообменом при различных температурах и режимах движения реакционной среды в периодических и непрерывных процессах.
2. Ёмкостные барботажные А. без с перемешивающх устройств
Г:Ж
T =[ (-20)…300]OC
P=[(-0,01)…1] МПа
Ряд процессов сульфирования, галогенирования, дедиазонирования с азеотропной отгонкой воды из продуктов
3. Трубчатые.
«труба-в-трубе»
В т.ч. пульсационные
Г, Ж
Ж-Ж
Г-Ж
Ж-Т
Г-Ж-Т
T =[(-100)…1000] OC
P=[(-0,001)…50] Мпа
Разнообразные каталитические и нека-талитические непрерывные процессы с интенсивным перемешиванием и теплообменом при различных температурах.
4. Кожухотрубчатые
Г, Ж
Ж-Ж
Г-Ж
Ж-Т
Г-Ж-Т
T =[(-100)…1000] OC
P=[(-0,001)…10] Мпа
Разнообразные каталитические и некаталити-ческие непрерывные процессы с интенсивным перемешиванием и теплообменом при различных температурах.
5. Колонны (насадочные и тарельчатые)
Г-Ж
T =[(-20)…500] OC
P=[(-0,001)…50] МПа
Процессы в условиях кипения реакционной среды или с интенсивным барботажем газа
6. Полочные
Г
Г-Т
Г-Ж
T =[(-50)…200] OC
P=[(-0,001)…1] Мпа
Обжиг твёрдых продуктов. Каталитические процессы в условиях неподвижного, движущегося и псевдоожиженного слоя катализатора. Абсорбционно-химические процессы
7. Многозонные контактные аппараты со встроенными теплообменными
устройствами
Г-Т
Г-Ж-Т
T =[(-100)…1300] OC
P=[(-0,001)…10] Мпа
Каталитические процессы в услових не-подвижного, движущегося и псевдоожи-женного слоя катализатора с организацией интенсивного теплообмена
8. Ванные
Ж
T =[(-10)…100] OC
P:= атмосферное
Процессы электрохимического синтеза
9. Камерные
Г, Г-Т
Г-Ж
T =[500…2500] OC
P=[0,1…1] Мпа
Печи обжига. Коксовые печи. Камеры сгорания тепловых двигателей и энергоустановок
Выбор типа реактора производится с учётом всей полноты действующих факторов.
3.3. Макрокинетика ХП и динамика химических реакторов.
3.3.1. ПОСТАНОВКА ЗАДАЧИ. ЭЛЕМЕНТЫ ТЕОРИИ ПОДОБИЯ ДЛЯ РЕАКТОРОВ.
Главная задача, решаемая технологом при использовании реакторов: определение типа, конструктивных и технических параметров аппарата; оптимизация условий ведения процесса и работы (эксплуатации) аппарата; принятие необходимых мер по обеспечению безопасности и устойчивости работы реактора. Успешное решение её невозможно без правильного по существу и полного по содержанию понимания сути и механизма протекающих в реакторе процессов и явлений.
Здесь необходимо сделать ряд ссылок на ранее изучавшиеся курсы. Классическая теория ПАХТ изучает все процессы, кроме химических. С другой стороны химия - неорганическая, органическая, в меньшей степени физическая - изучают именно химические процессы, мало занимаясь явлениями переноса. В реальных же процессах (осуществляемых в реакторах) одновременно протекают и химические реакции и явления переноса. Химические превращения изменяют состав среды, что изменяет все её физические свойства - плотность, теплоёмкость, вязкость, теплопроводность, диффузию, упругость; с другой стороны (что яснее видно из курса ПАХТ) теплопередача и диффузия в огромной степени влияют на температуру и концентрации всех реагентов в реакторе - т.е., на протекание химических реакций.
Поэтому строгие расчёты, выполняемые технологами - как при проектировании (проверке правильности выбора реактора), так и при оптимизации технологических режимов работы уже функционирующих в реальных процессах реакторов, - должны учитывать все характерные для реакторов явления. Задача эта решается путем исследования макрокинетики ХП и динамики реакторов.
Def. Макрокинетика: кинетика реальных сложных химических процессов с учётом явлений переноса массы, количества вещества, теплоты, импульса, поглощения и испускания излучений.
Def. Динамика: реальные изменения состояния реактора и хода ХП, обусловленные внутренним механизмом процесса, условиями его проведения и влиянием различных возмущений, возникающих в ходе работы.
В основе описания макрокинетики и динамики ХП лежат дифференциальные уравнения движения вещества, импульса, энергии (и иных свойств материи) в физико-химическом процессе с учётом конвективного и турбулентного переноса вещества - уравнения Умова (Умова-Пойнтинга). Это уравнение, в отличие от уравнений Навье-Стокса, Рейнольдса, Фурье-Кирхгофа и Фика, учитывает то, что химические превращения, а также межфазный перенос, загрузки в реактор реагентов и отвод продуктов из реактора приводят к образованию и исчезновению веществ внутри реактора - такие эффекты в теоретической физике называют источниками и стоками субстанций. Под «субстанцией» понимают как вещество, так и присущие ему свойства (наиболее общее свойство - химический потенциал).
Общая форма этого уравнения
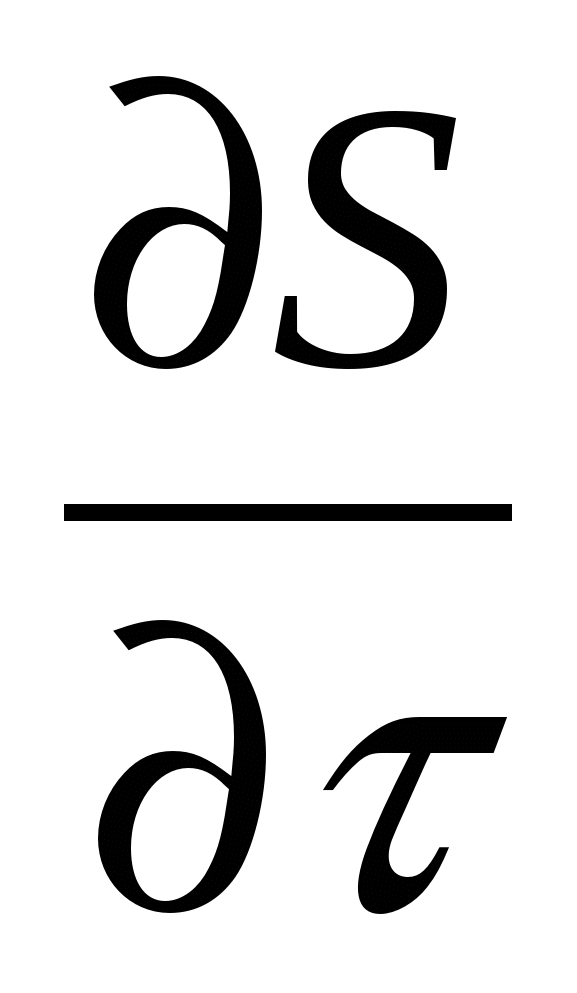 = Σ IOS - Σ ICS - div (J + S w) (1)
= Σ IOS - Σ ICS - div (J + S w) (1)
S - субстанция (свойство);
IOS - мощность источников субстанции;
ICS - мощность стоков субстанции;
J - конвективный поток;
w - линейная скорость.
Для прояснения физико-химической сущности явлений достаточно рассмотреть задачу в одномерном представлении. Рассмотрим элемент объёма реактора dV. Движение среды будем считать одномерным. Изменением удельного объёма среды пренебрежём.
_________
| Wr | Wr - векторная сумма скоростей химических реакций, кмоль/с;
 | IOIC |
| IOIC |![]() wl wl - линейная скорость потока, м/с;
wl wl - линейная скорость потока, м/с;
|_________ | (ρλην) С - концентрация в сечении l, кмоль/м3
| | C+dC - концентрация в сечении l+dl, кмоль/м3
l l+dl ρ - плотность среды, кг/м3
C C+dC λ - теплопроводность среды, Вт/м К
ή - обобщённый динамический коэффициент вязкости среды, Па.с
ΰ- обобщённый кинематический коэффициент вязкости среды, м2/с
СР - теплоёмкость среды, Дж/кг.К;
ά= λ/ ρСР - - температуропроводность среды, м2/с
IO - мощность физических источников вещества, кмоль/с;
IC- мощность физических стоков вещества, кмоль/с;
Рисунок 2. Схема элемента реакционного объёма.
В отсутствие внешних полей динамика процесса в элементе объёма реактора dV выражается системой уравнений Умова - Пойнтинга для переноса массы, количества вещества, тепла и импульса - т.н., характеристической системой уравнений
Перенос массы (материальный баланс) - выражается уравнением сплошности
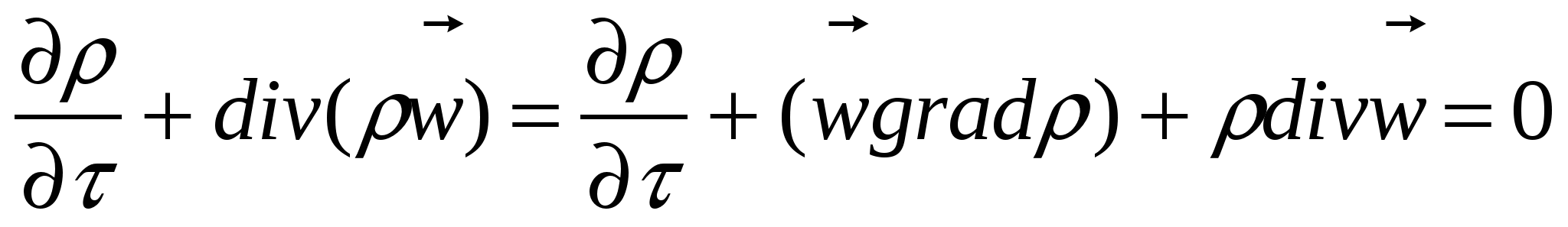 (2)
(2)
Перенос количества вещества - макрокинетика
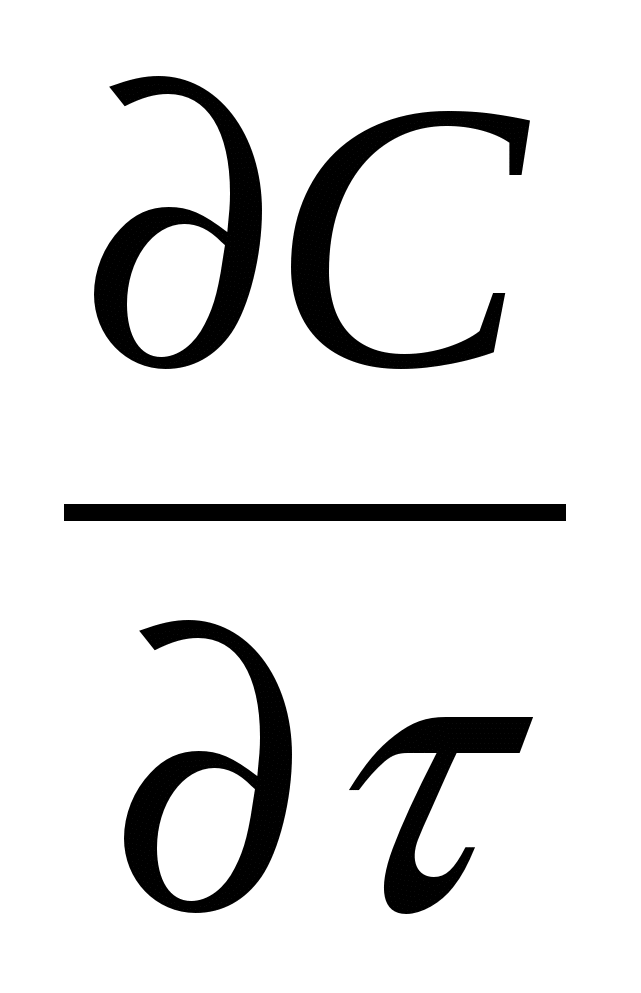 = Σ IOS - Σ ICS
= Σ IOS - Σ ICS 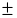 Wr (1 - С
Wr (1 - С 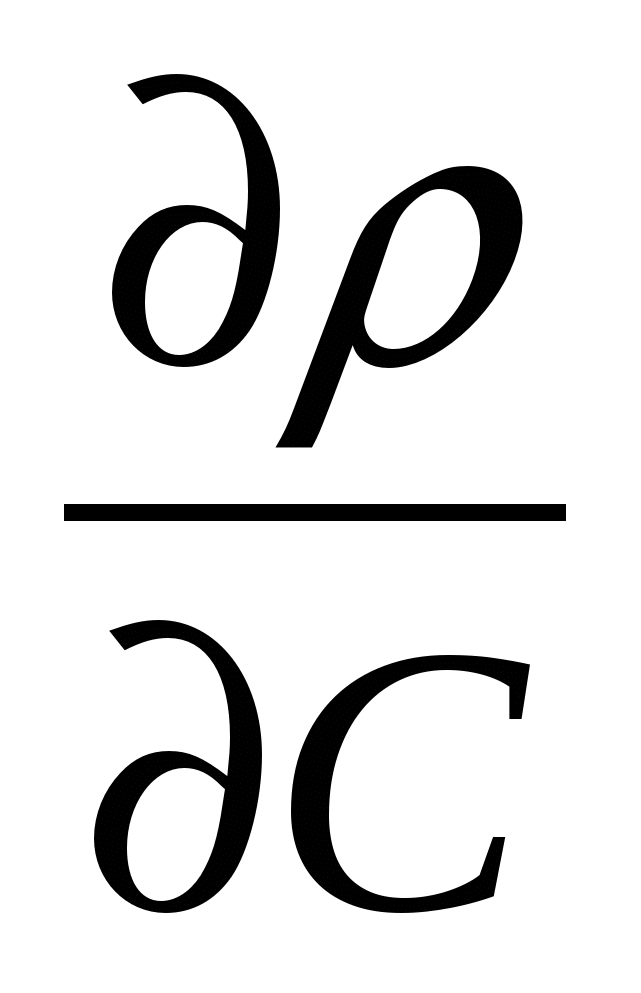 ) - wl
) - wl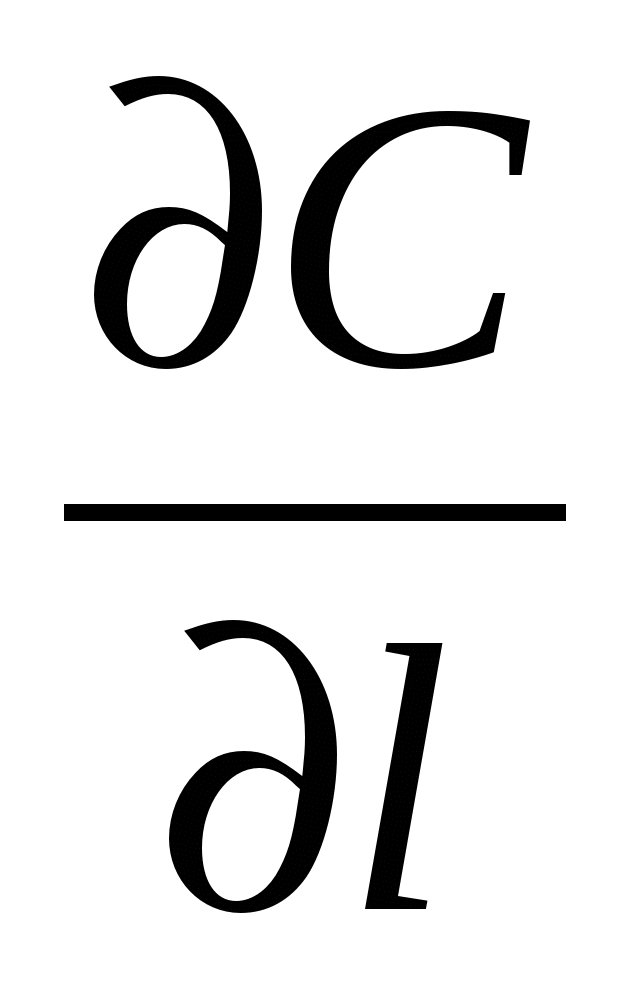 + D
+ D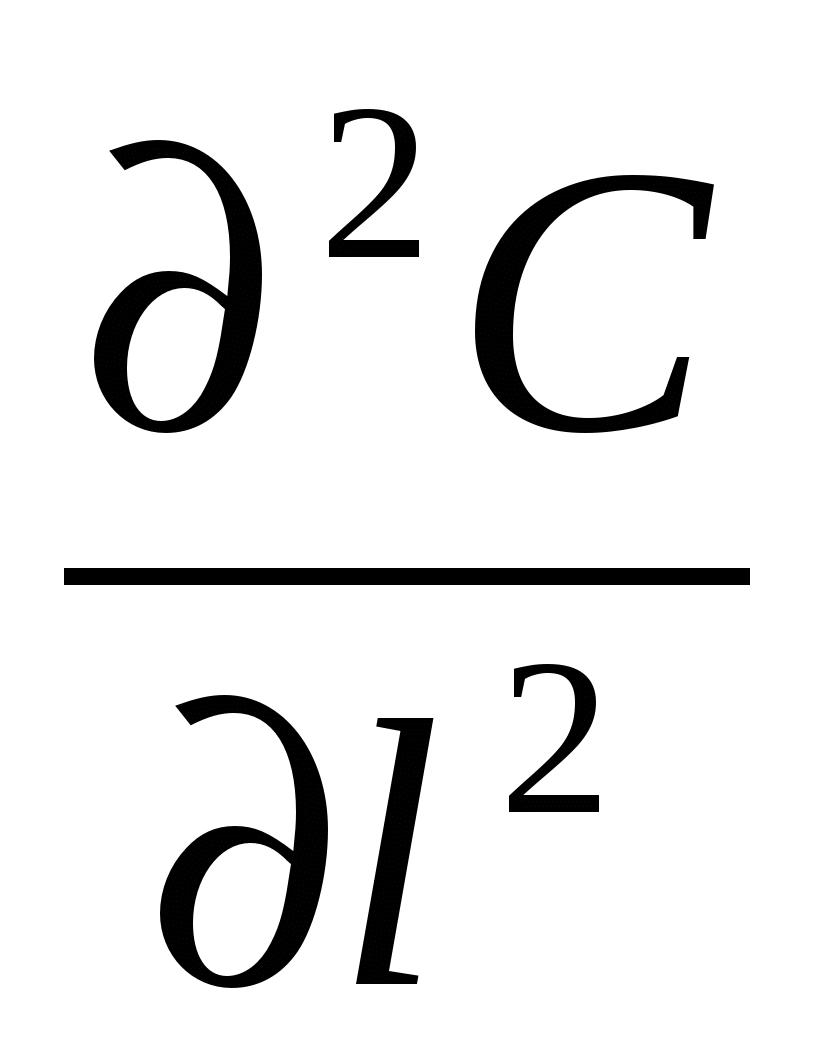 (3)
(3)
I II III IV V
где D - коэффициент перемешивания, м2/с.
Перенос тепла
ρСР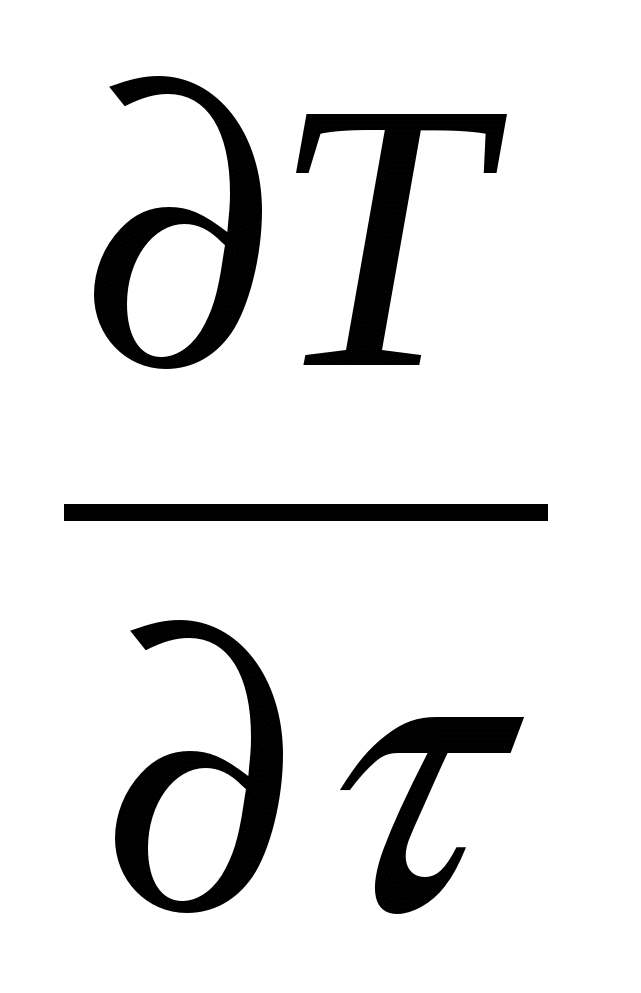 = Σ IOSН0S - Σ ICSНСS- Σ WR ΔНR + Wr ρСР Т
= Σ IOSН0S - Σ ICSНСS- Σ WR ΔНR + Wr ρСР Т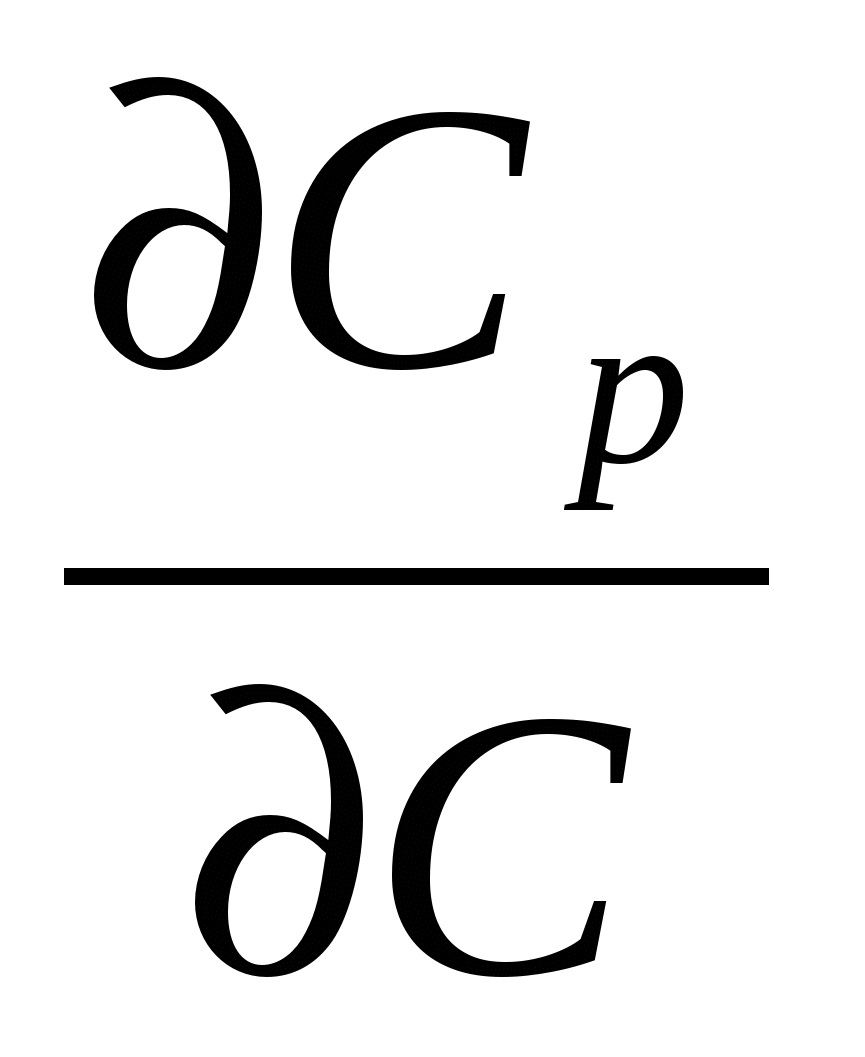 - wl ρСР
- wl ρСР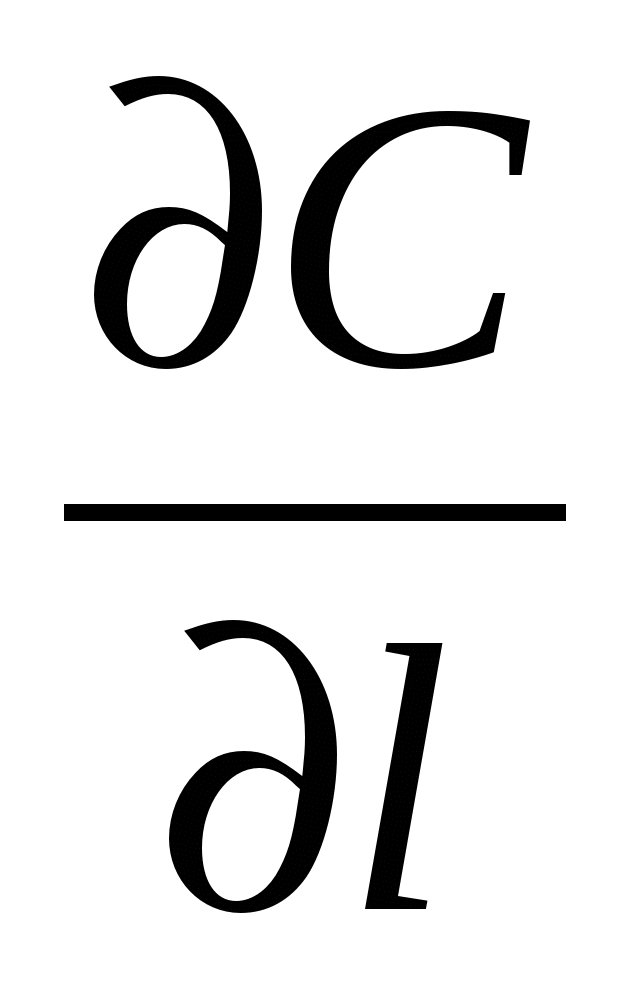 + λ
+ λ 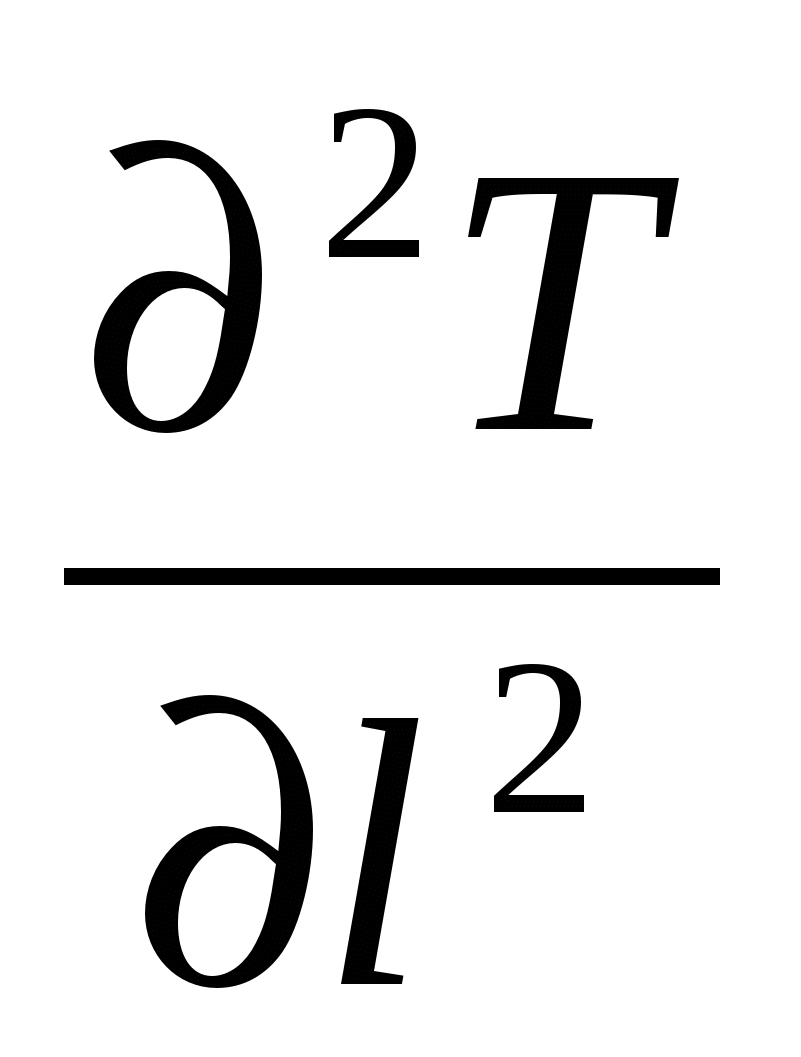 (4)
(4)
VI VII VIII IX X XI XII
Перенос импульса (течение среды)
ρ 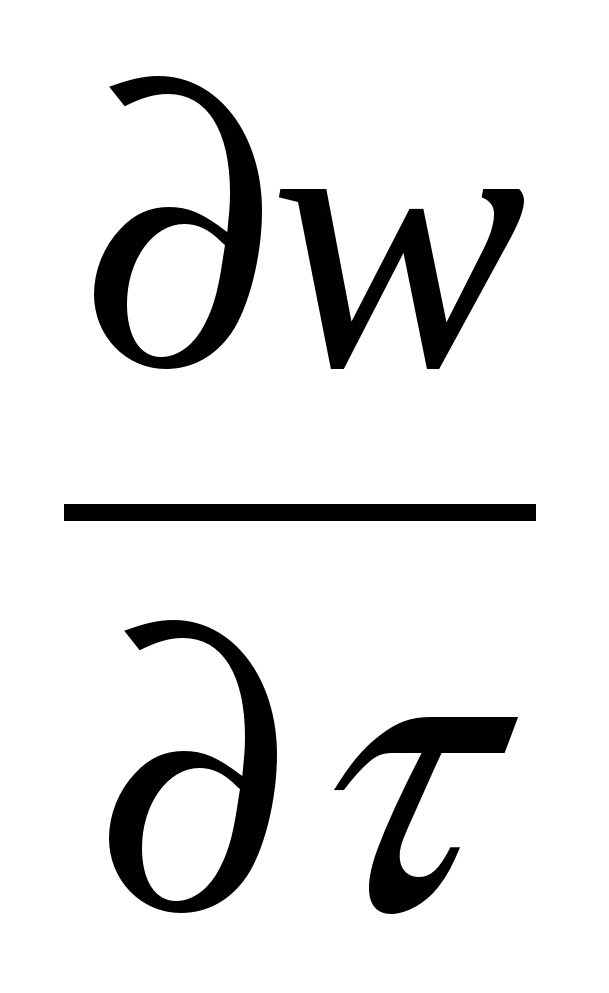 = ρ wl (WRΔV -
= ρ wl (WRΔV - 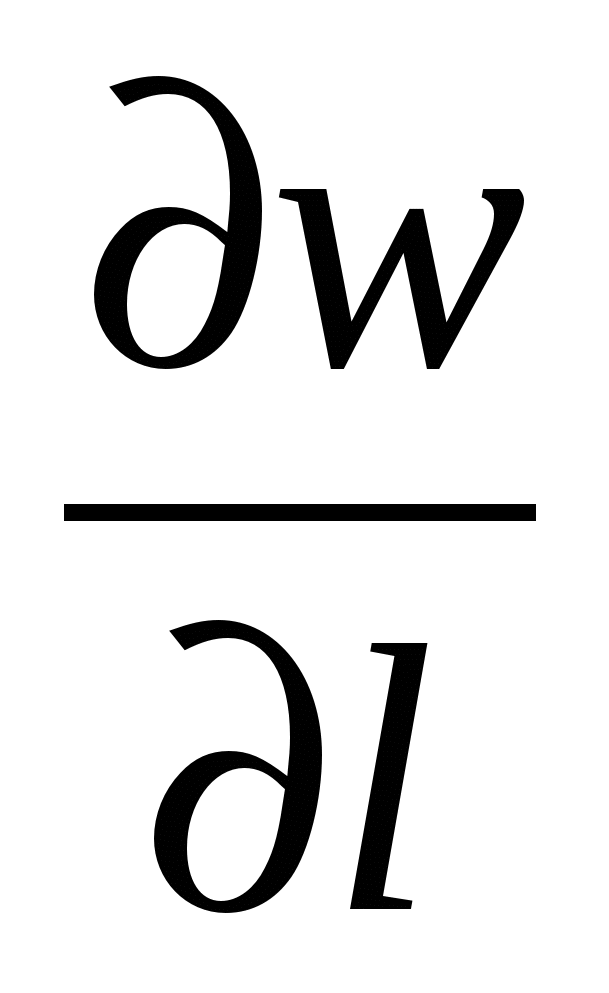 ) -
) - 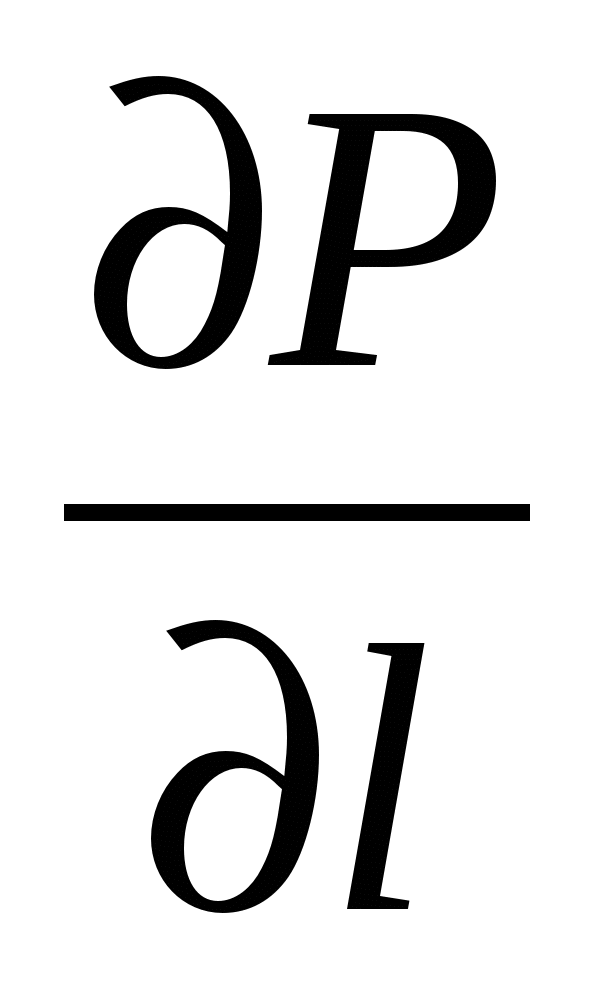 + ή
+ ή 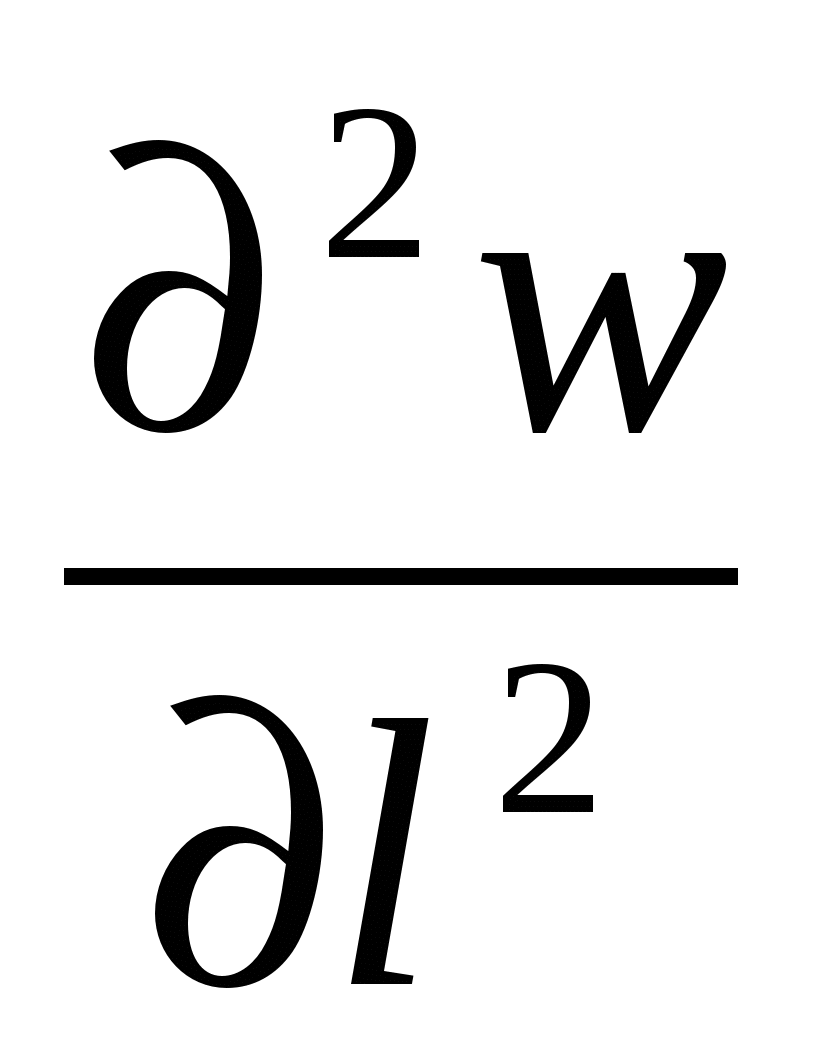 (5)
(5)
XIII XIV XV XVI XVII
Где Σ IOS - интенсивность физических источников вещества, кмоль/м3с;
Σ ICS- интенсивность физических стоков вещества, кмоль/м3с;
Н0S, НСS - энтальпии вносимых и уносимых веществ, Дж/кмоль;
ΔНR - тепловой эффект реакции, Дж/кмоль;
ΔV - изменение молярного объёма в результате реакции, м3/кмоль;
D - коэффициент перемешивания (турбулентно-молекулярной диффузии), м2/с;.
ή - динамический коэффициент турбулентно-молекулярной вязкости, Па.с.
Знак «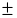 » зависит от того, рассматривается ли концентрация реагента или продукта реакции.
» зависит от того, рассматривается ли концентрация реагента или продукта реакции.
Для полной характеристики задачи требуется также формулирование начальных и граничных условий. В целом это требует проведения большого объёма экспериментальных работ и вычислений. Сложность уравнений Умова приводит к тому, что в подавляющем большинстве случаев для практических целей прибегают к их упрощению на основе теории подобия. Т.е., упрощают задачу путём осреднения ряда параметров. Это позволяет перейти от уравнений математической физики к обыкновенным дифференциальным уравнениям, и в ряде случаев получить аналитические выражения, хорошо приближающиеся к эксперименту.
В качестве примера рассмотрим уравнение переноса количества вещества (5).
Преобразование формулы (5) в соответствии с теорией подобия даёт выражение (членом III обычно пренебрегают)
С/τ = Σ IOS - Σ ICS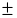 Wr - wl С/L + D С/ L2, (8)
Wr - wl С/L + D С/ L2, (8)
Iа IIа IIIа IVа
где L - определяющий линейный размер, м.
Из этого выражения получают основные критерии подобия.
Делением членов (III) : (IV) - критерий Боденштайна (иногда называют критерием Пекле для реакторов) - выражающий соотношение конвективного и турбулентного переноса вещества.
Во = 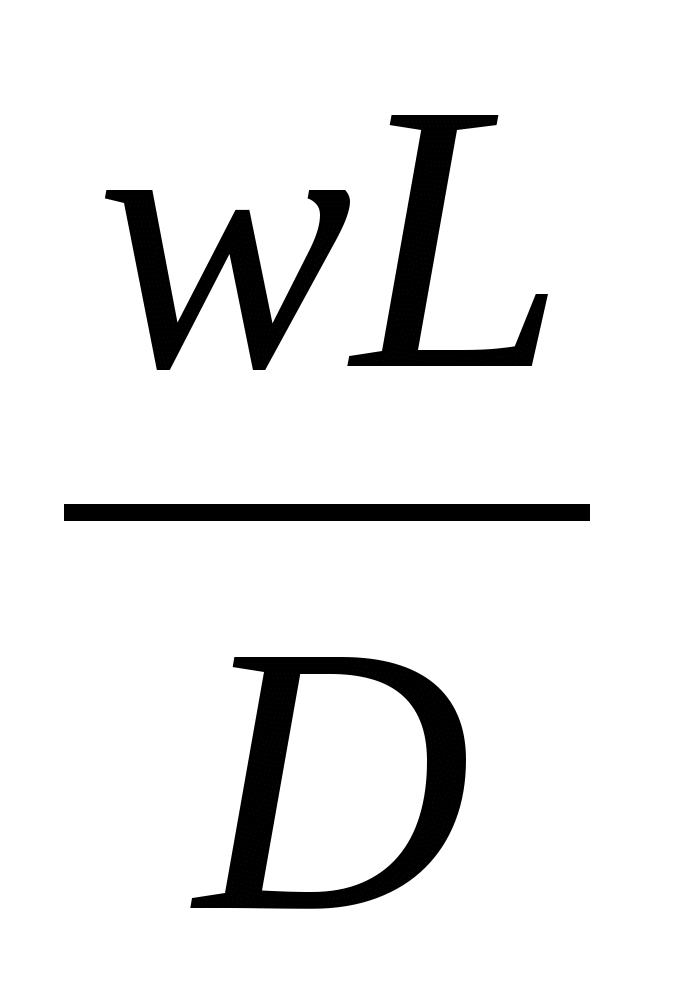 , (9)
, (9)
Делением членов (II): (III) - первый критерий Дамкелера - выражающий соотношение скорости реакции и конвективного переноса вещества.
DaI =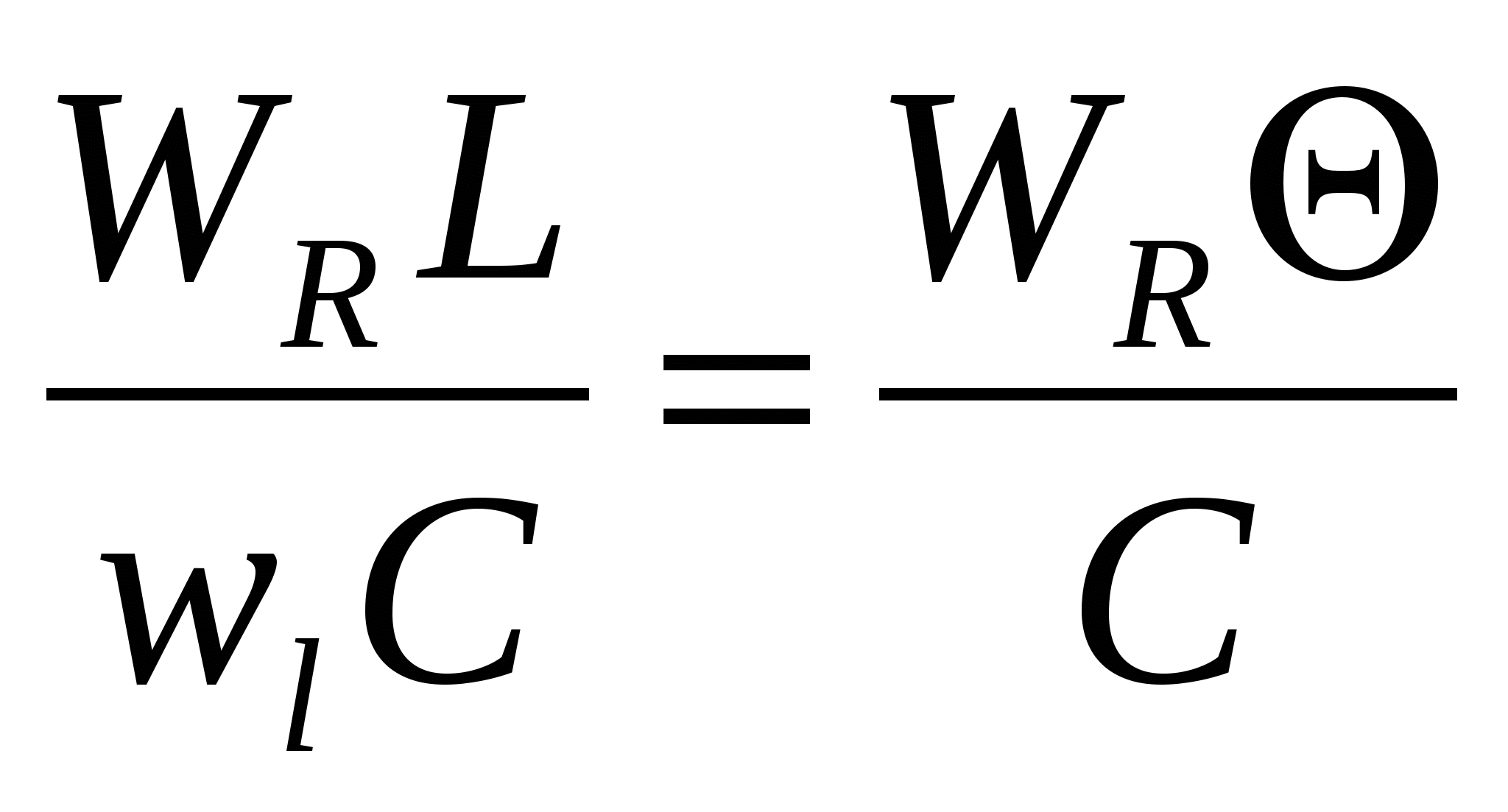 , (10)
, (10)
где 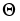 = L/ wl - среднее время пребывания потока в реакторе, с.
= L/ wl - среднее время пребывания потока в реакторе, с.
Делением членов (II): (IV) - второй критерий Дамкелера
DaII = 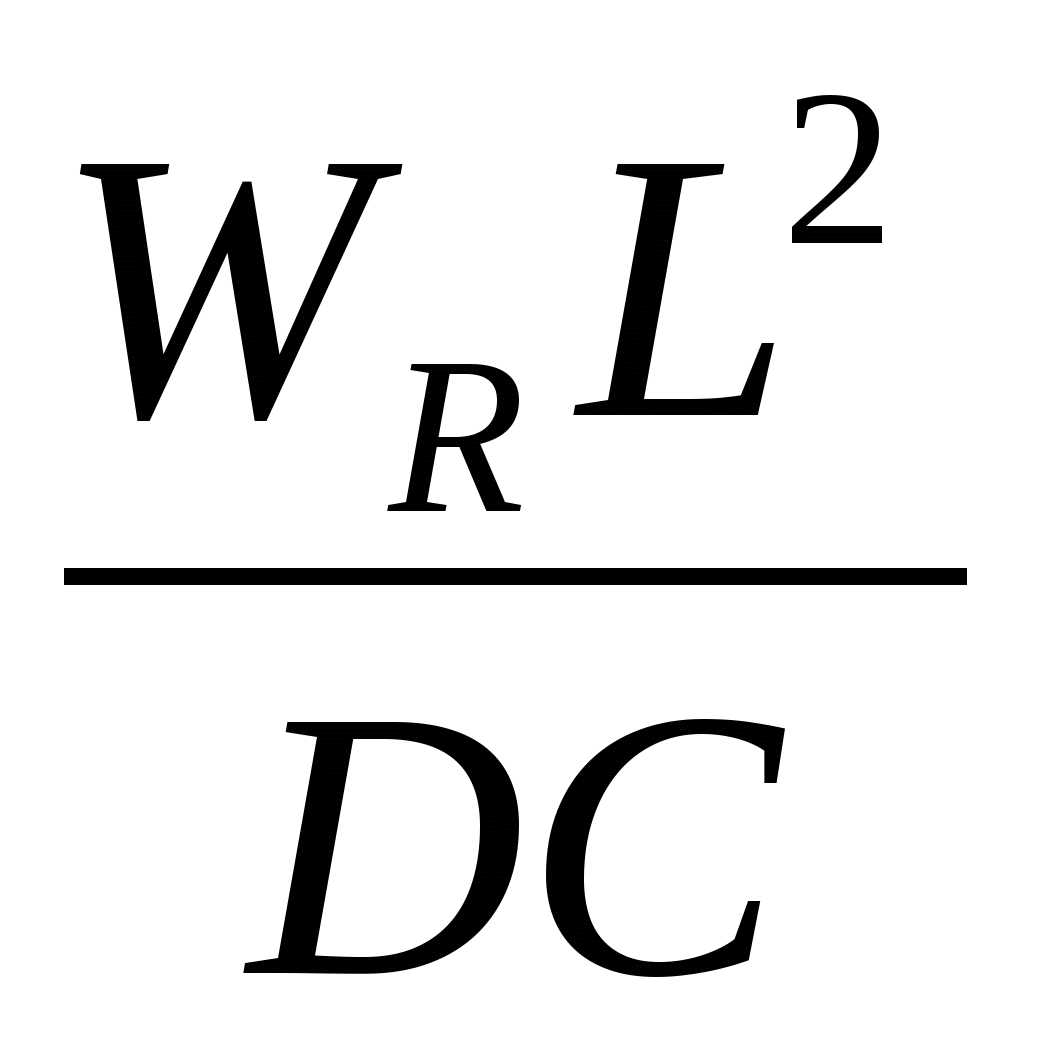 , (11)
, (11)
DaII выражает соотношение скорости реакции и интенсивности турбулентного переноса вещества.
Аналогично из уравнения (6) выводят третий и четвёртый критерии Дамкелера.
Делением членов (II): (III) - третий критерий Дамкелера, выражающий соотношение тепловой мощности реакции и конвективного переноса тепла.
DaIII= 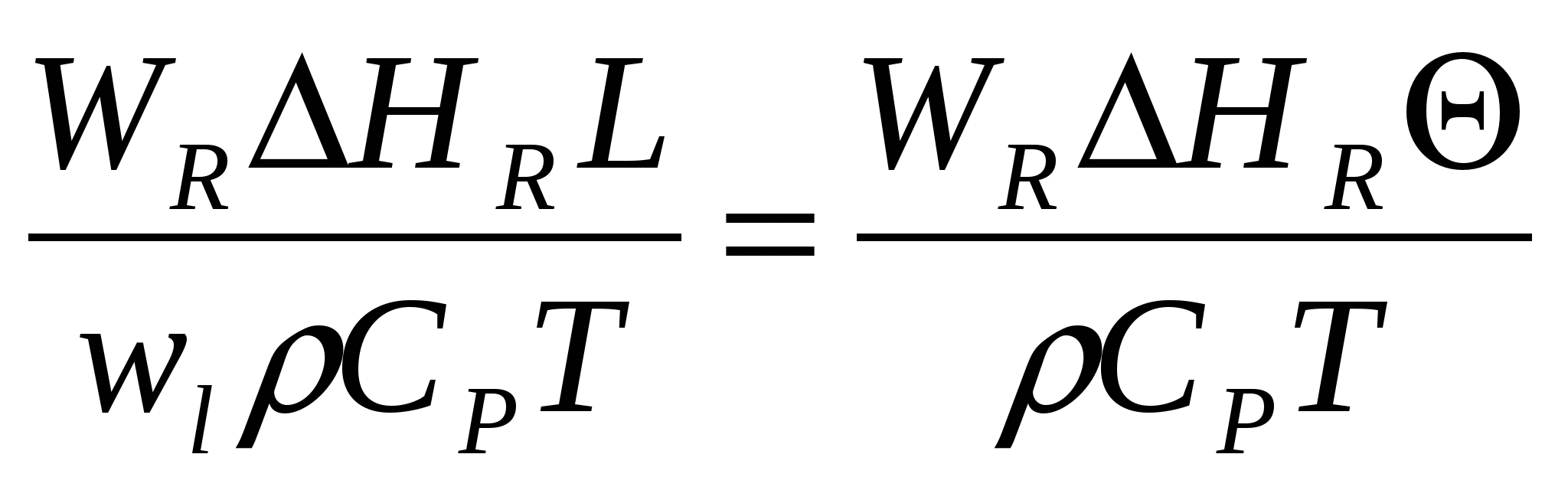 , (12)
, (12)
где 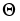 = L/ wl - среднее время пребывания потока в реакторе, с.
= L/ wl - среднее время пребывания потока в реакторе, с.
Делением членов (II): (IV) - четвёртый критерий Дамкелера, выражающий соотношение тепловой мощности реакции и турбулентного переноса тепла.
DaIV= 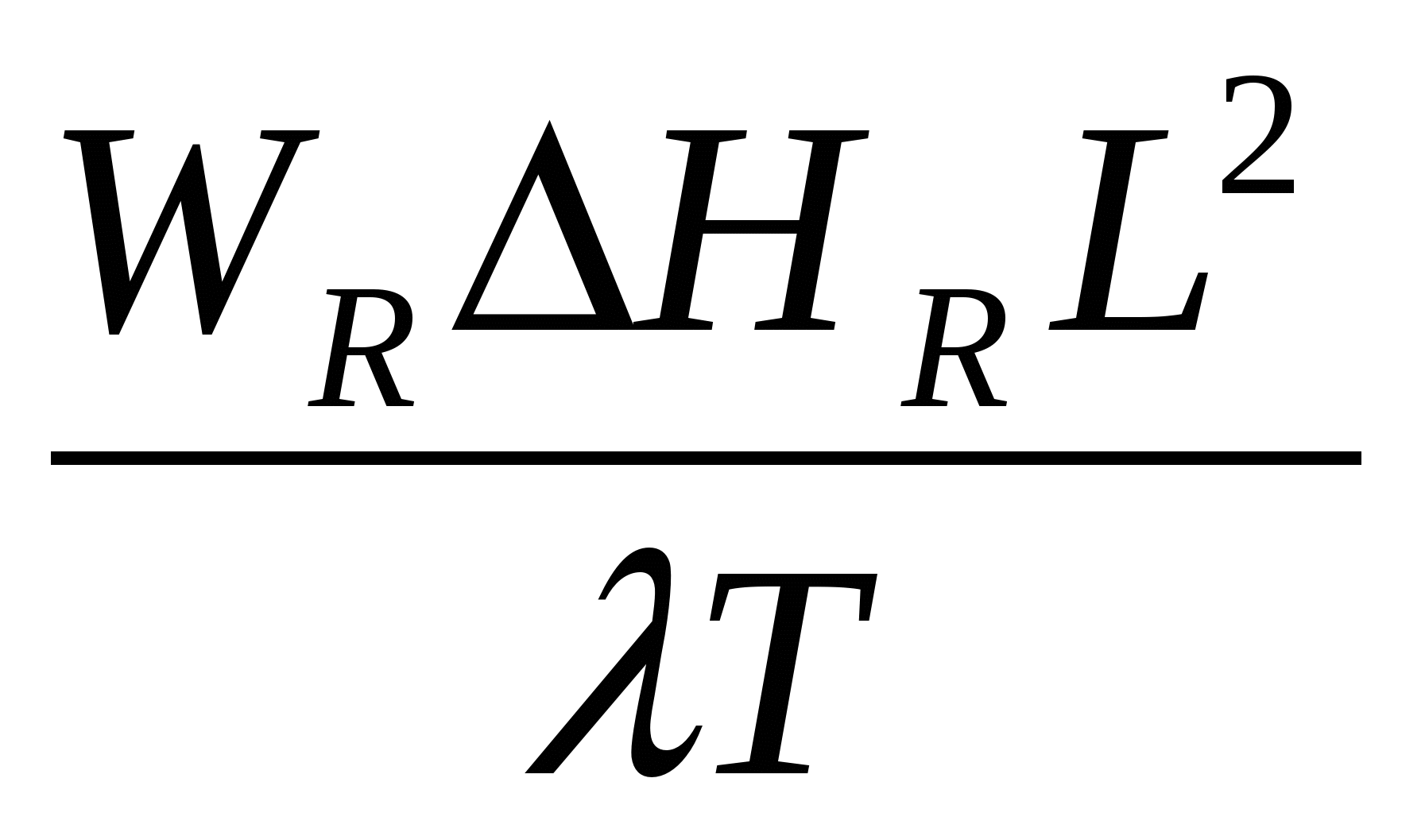 , (13)
, (13)
На основании вышеприведённых соотношений выводят т.н. характеристическое уравнение реактора, а точнее -характеристическую систему уравнений, выражающих связь между степенью превращения, скоростью и временем протекания ХП. Характеристическое уравнение - основа технологического расчёта реакторного процесса.
Def. Характеристическое уравнение - уравнение, связывающее скорость процесса, концентрации (и степени превращения) реагентов и необходимое время.
Применение преобразований подобия (9)-(13) обычно позволяет заменить систему уравнений математической физики (5)-(8) системой обыкновенных дифференциальных, критериальных и алгебраических уравнений вида.
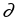 С/
С/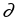
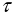 = FC(WR; DaI; DaII; DaIII ; DaIV; Re; Bo; IC; IS ) (14)
= FC(WR; DaI; DaII; DaIII ; DaIV; Re; Bo; IC; IS ) (14)
ρСР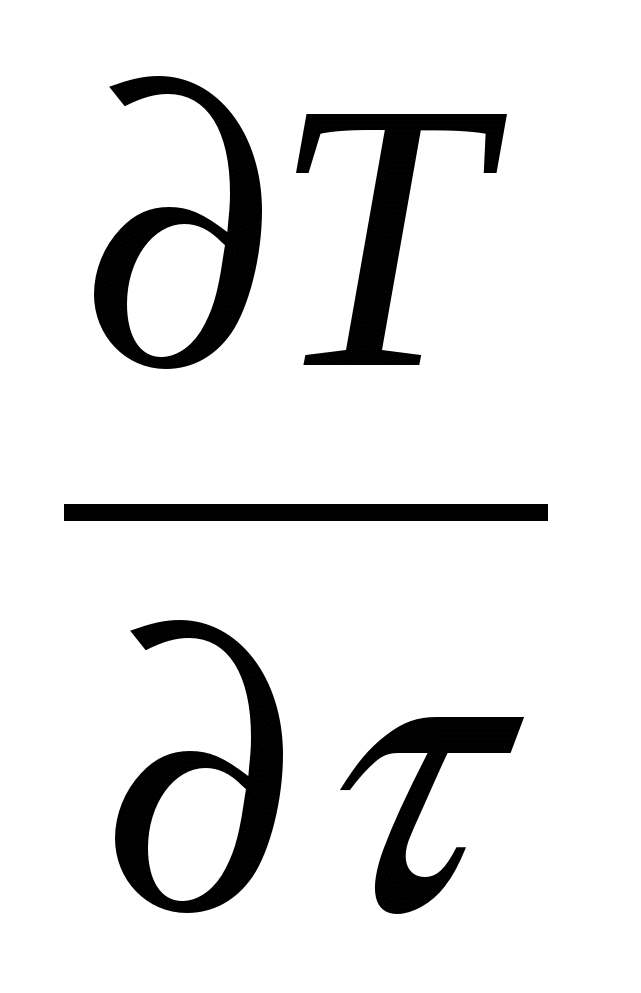 = FT(WR; DaI; DaII; DaIII ; DaIV; Re; Bo; IC; IS Gr; Ki; Bi… ) (15)
= FT(WR; DaI; DaII; DaIII ; DaIV; Re; Bo; IC; IS Gr; Ki; Bi… ) (15)
Eu = FP (WR; DaI; DaII; DaIII ; DaIV; Re; Bo; IC; IS ; Fr; Gr; Ki; Bi…) (16)
Где Eu, Re, Fr, Gr; Ki; Bi, - соответственно критерии (числа) Эйлера, Рейнольдса, Фруда,
Грасгофа, Кирпичёва, Био и т.д.
Как правило, на практике идут по пути дальнейших упрощений уравнений (14) -(16), основанных на следствиях, вытекающих из существования определённых областей качественно своеобразных условий протекания, выражаемых «граничными» значений критериев Во, DaII; DaIV. Эти упрощения позволили вывести основные группы моделей движения среды, определяющих тип макрокинетики процессов в реакторах.
К таковым базовым моделям относятся следующие: идеального/полного смешения (РИС); идеального/полного вытеснения (РИВ);. диффузионная (ДРВ) и ячеечная (КРИС-Н).
Сложные модели реальных аппаратов строят на основе комбинации вышеприведённых базовых моделей. Характеристика этих моделей и область их применения к реальным аппаратам приведены в таблице
МОДЕЛИ ПРОЦЕССОВ В РЕАКТОРАХ ОСНОВНЫХ ТИПОВ
1. РЕАКТОРЫ С МЕШАЛКАМИ (АППАРАТЫ-КОТЛЫ)
Основная модель для описания процессов в аппаратах этого типа - модель идеального/полного смешения (РИС). В основе её лежит допущение, что интенсивное перемешивание практически обеспечивает выравнивание концентраций и температуры по всему объёму реактора. Математически это отражается следующим образом.
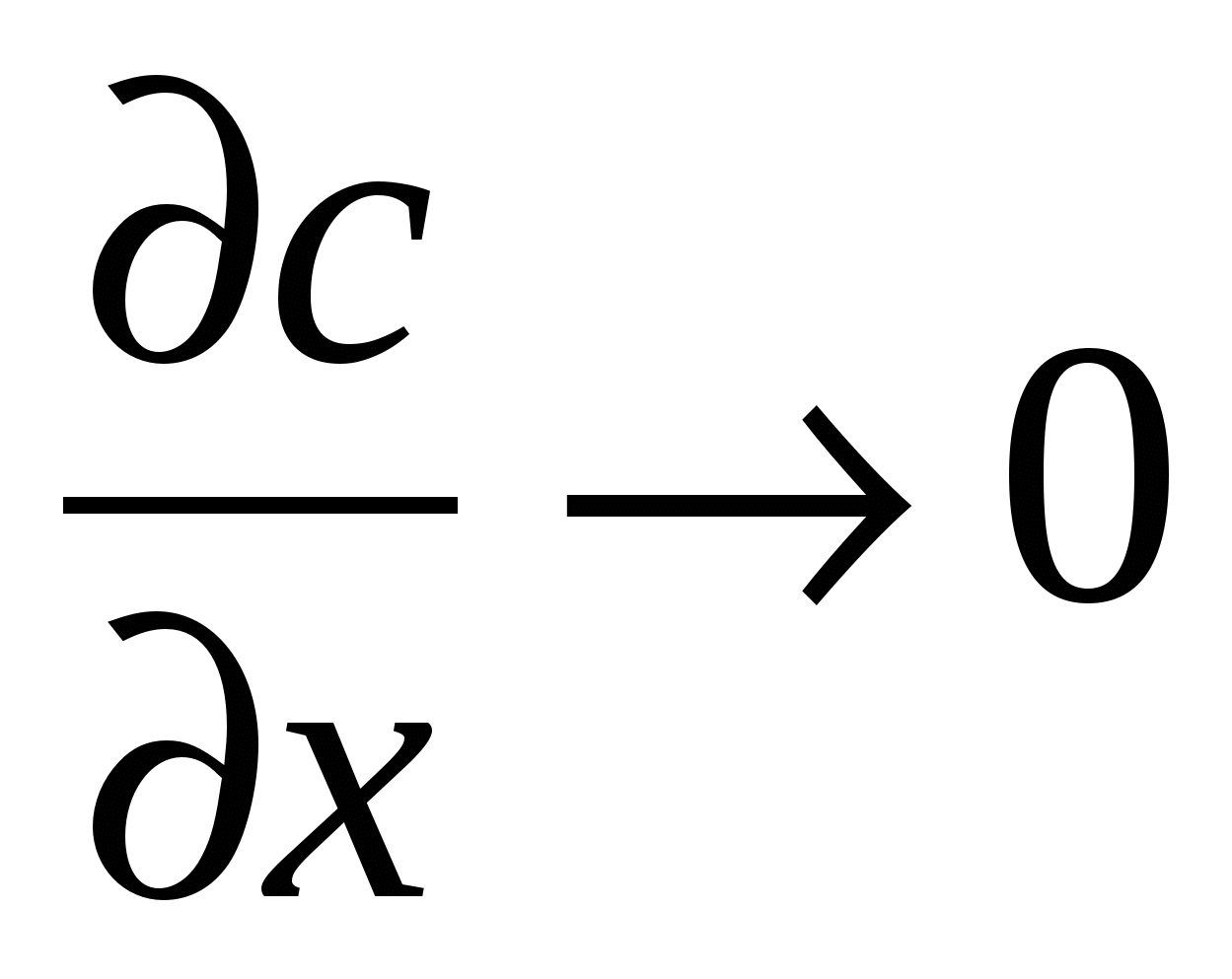 (17а)
(17а)
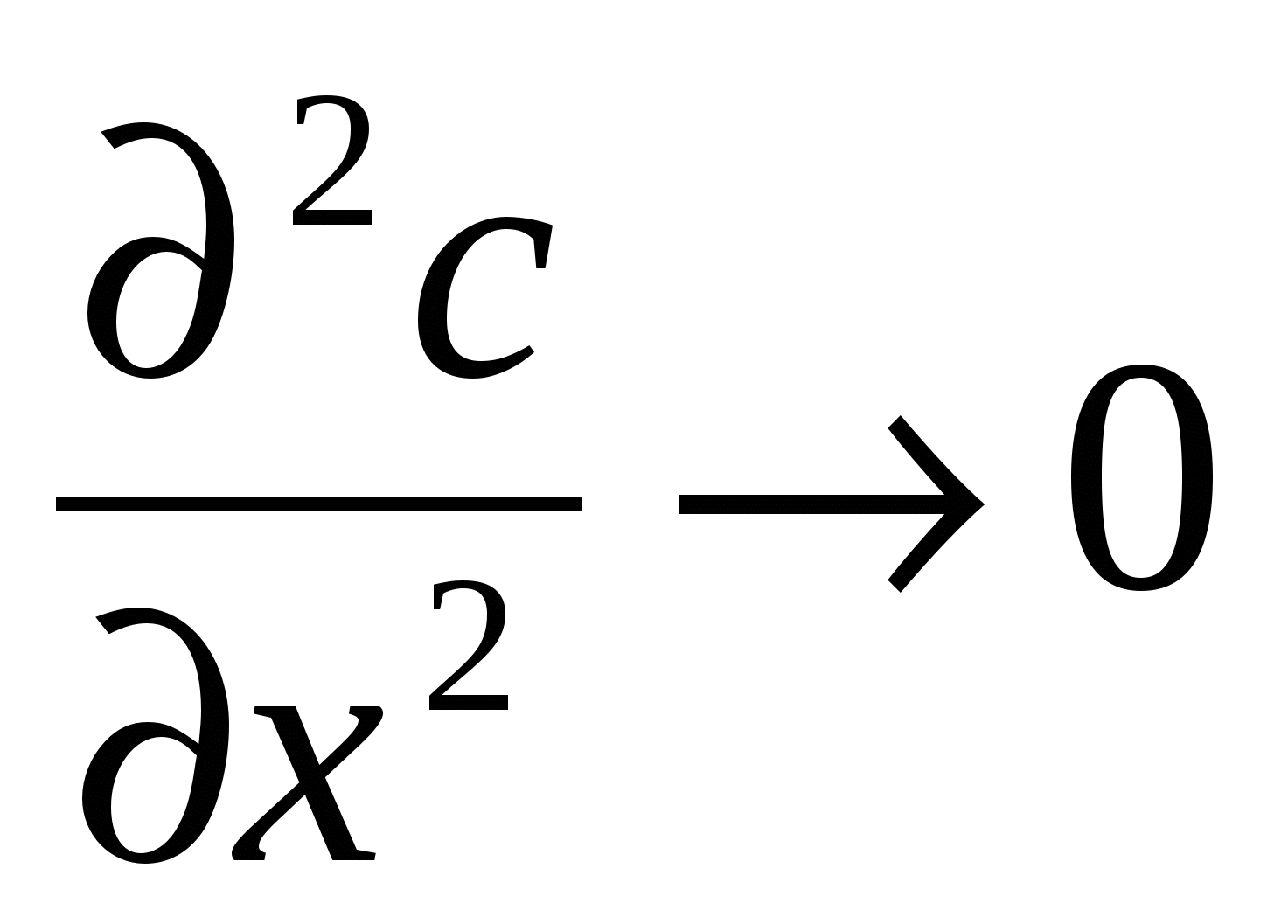 (17б)
(17б)
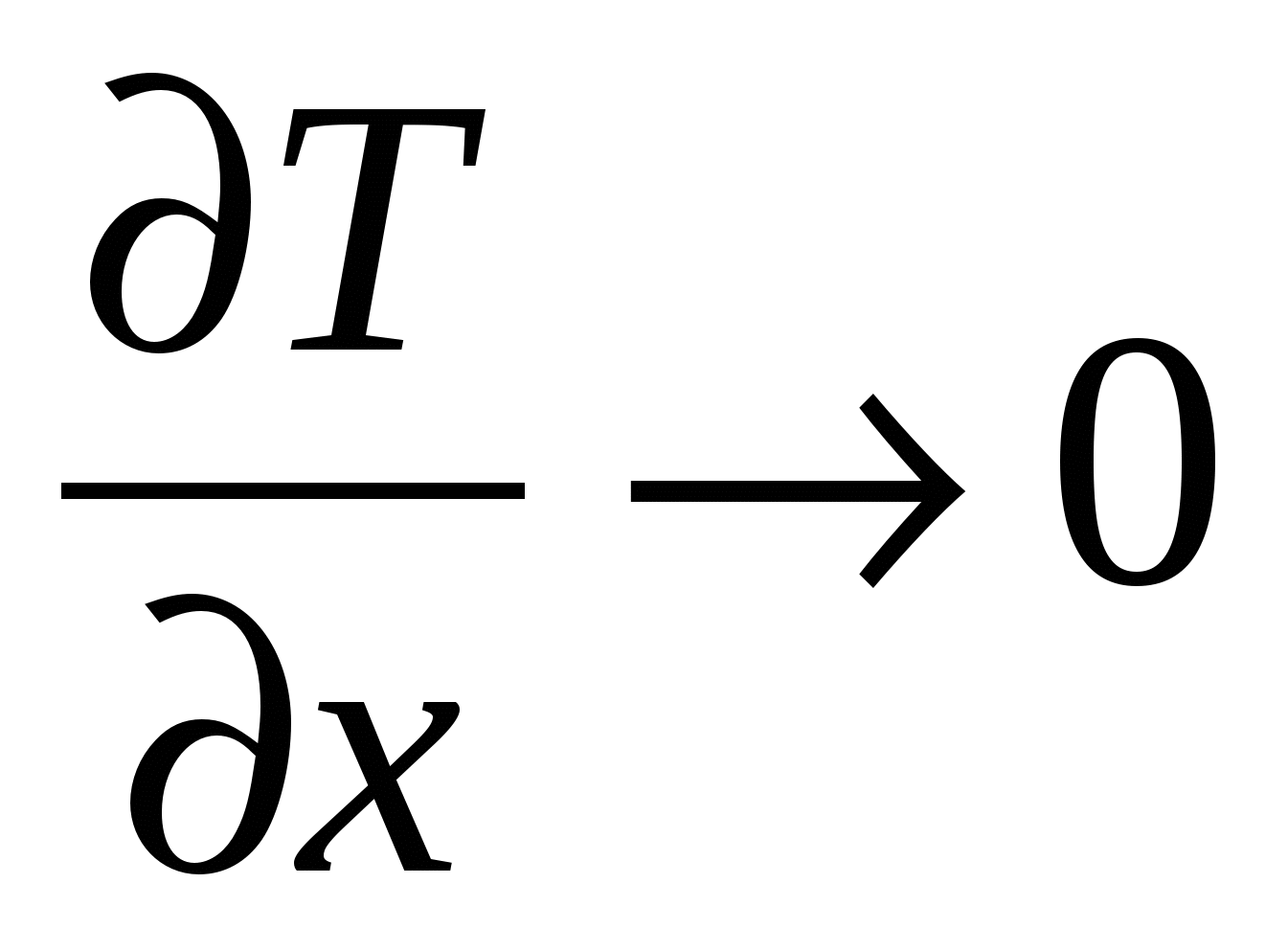 (17в)
(17в)
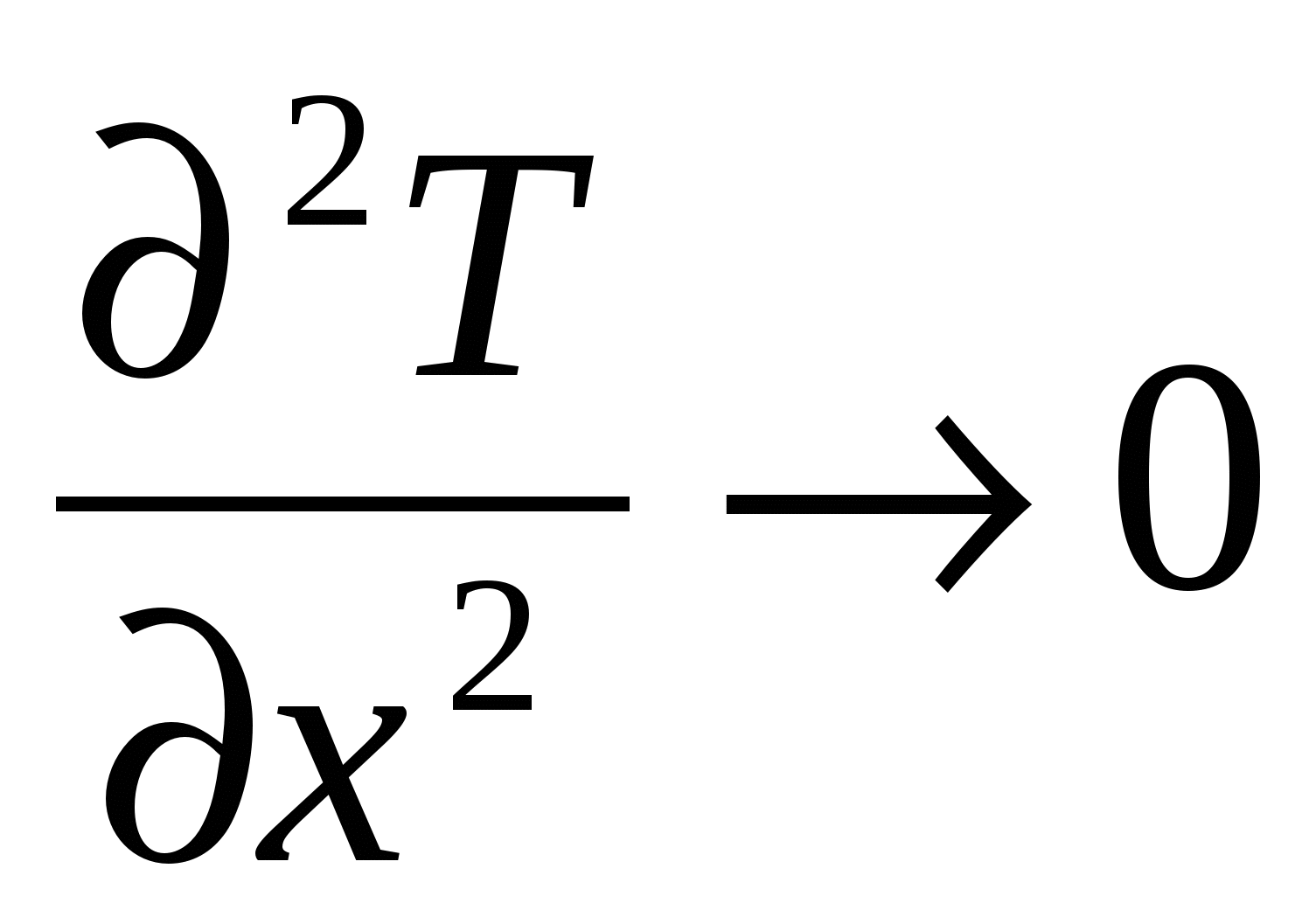 (17г)
(17г)
Bo<<1 (17д)
DaII<<1 (17е)
DaIV<<1 (17ж)
В большинстве случаев в средах невысокой вязкости относительная неоднородность концентраций действительно не превышает (1…2) %, а перепады температуры не превышают (1…2) градуса (и приходятся на пограничный слой). Для этих условий модель РИС вполне корректна. Модель применяют и к периодическим и к непрерывным процессам.
1.1 Реакторы периодического действия - РИС-П.
Эта модель применяется к периодическим процессам, при осуществлении которых все реагенты загружают за время, пренебрежимо малое по сравнению с общей продолжительностью реакционного цикла, т.е., практически единовременно. До окончания процесса продукты реакции из реактора не отводят. Поэтому все изменения концентраций и температуры обусловлены только происходящими в реакторе процессами.
Рисунок . Схема РИС-П
Математическое описание процесса.
Реакция aIAI = bIBI
Масса веществ неизменна
М = М0 = Const (18а)
Скорость реакции (макрокинетика процесса)
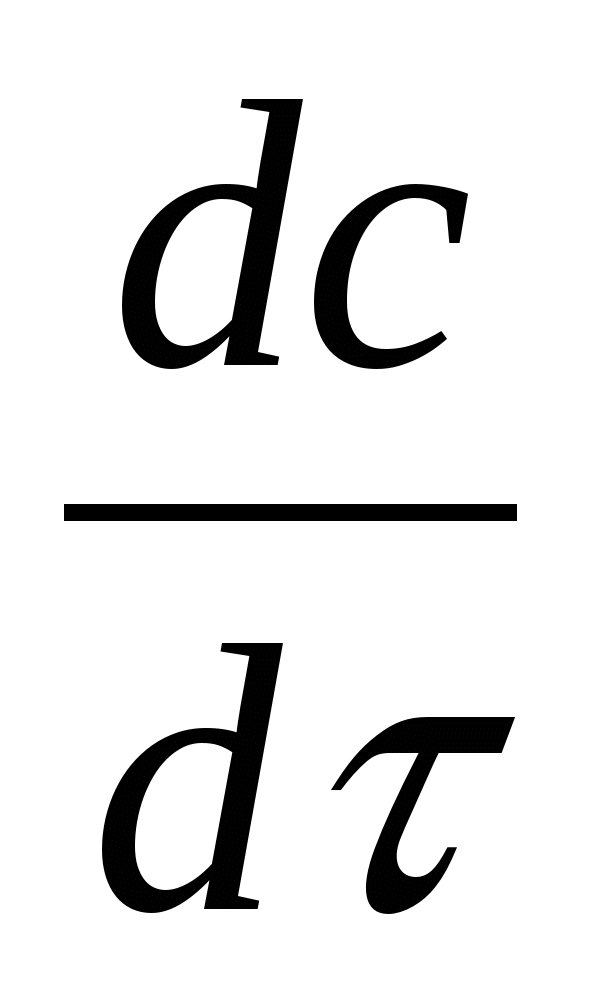 = WR + WR
= WR + WR ![]() - C
- C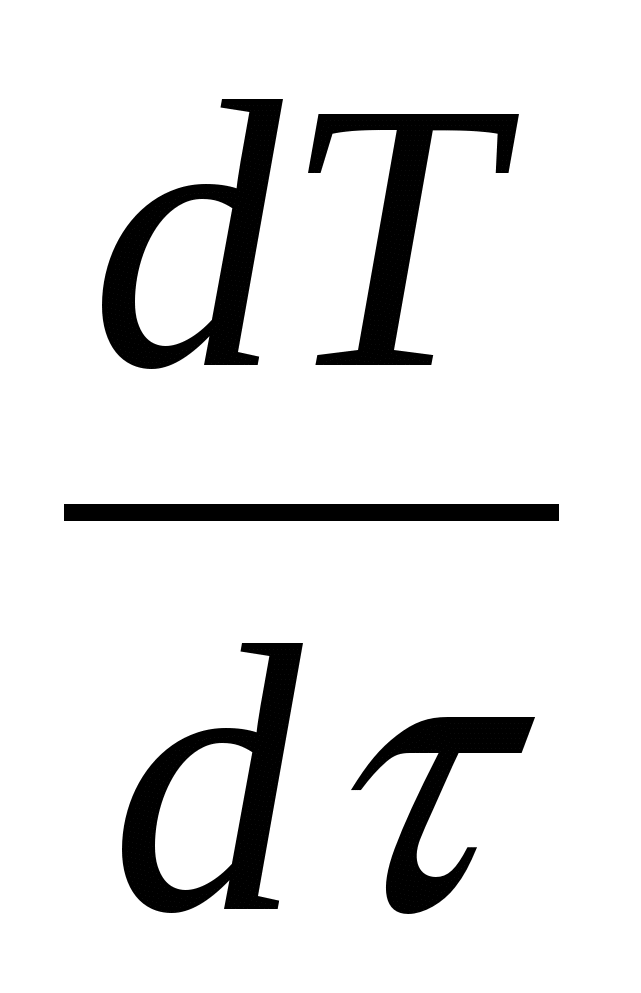 (18б)
(18б)
Температура (дифференциальный тепловой баланс определяется тепловыми эффектами химических и массообменных процессов; организованным теплообменом; мощностью, диссипируемой мешалкой и теплообменом с окружающей средой).
MCр*![]() + MACA
+ MACA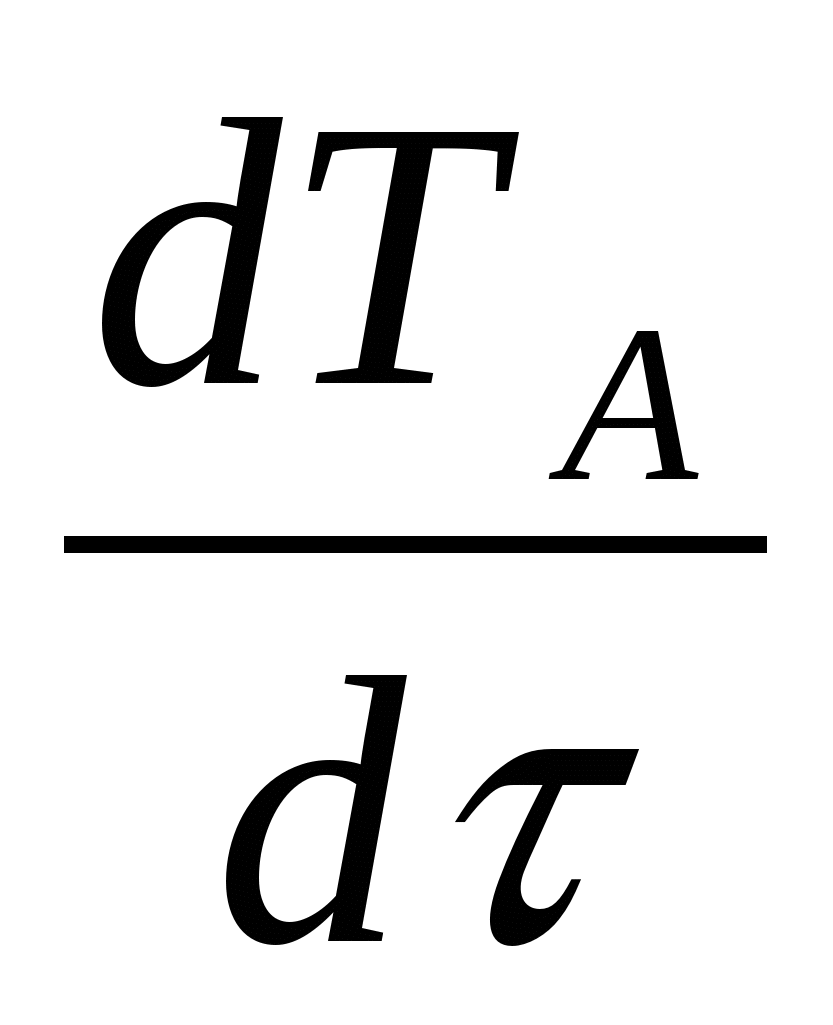 = - ΔНR | WR | - ΔНm | Wm | - КF Δ
= - ΔНR | WR | - ΔНm | Wm | - КF Δ - КПFП(Т-) + NЖ (18в)
- КПFП(Т-) + NЖ (18в)
Где С - концентрации веществ, моль/м3;
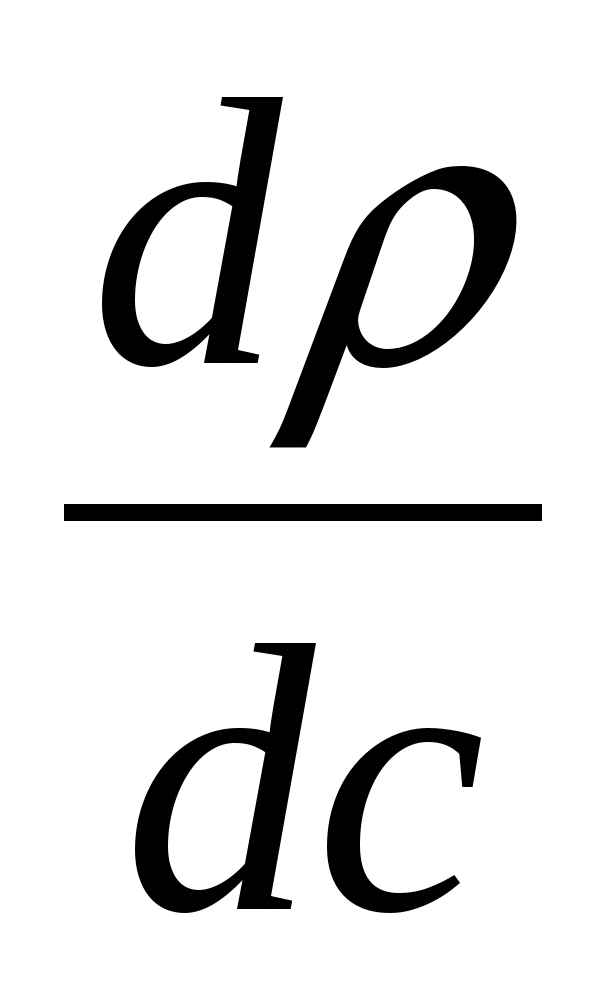 =
=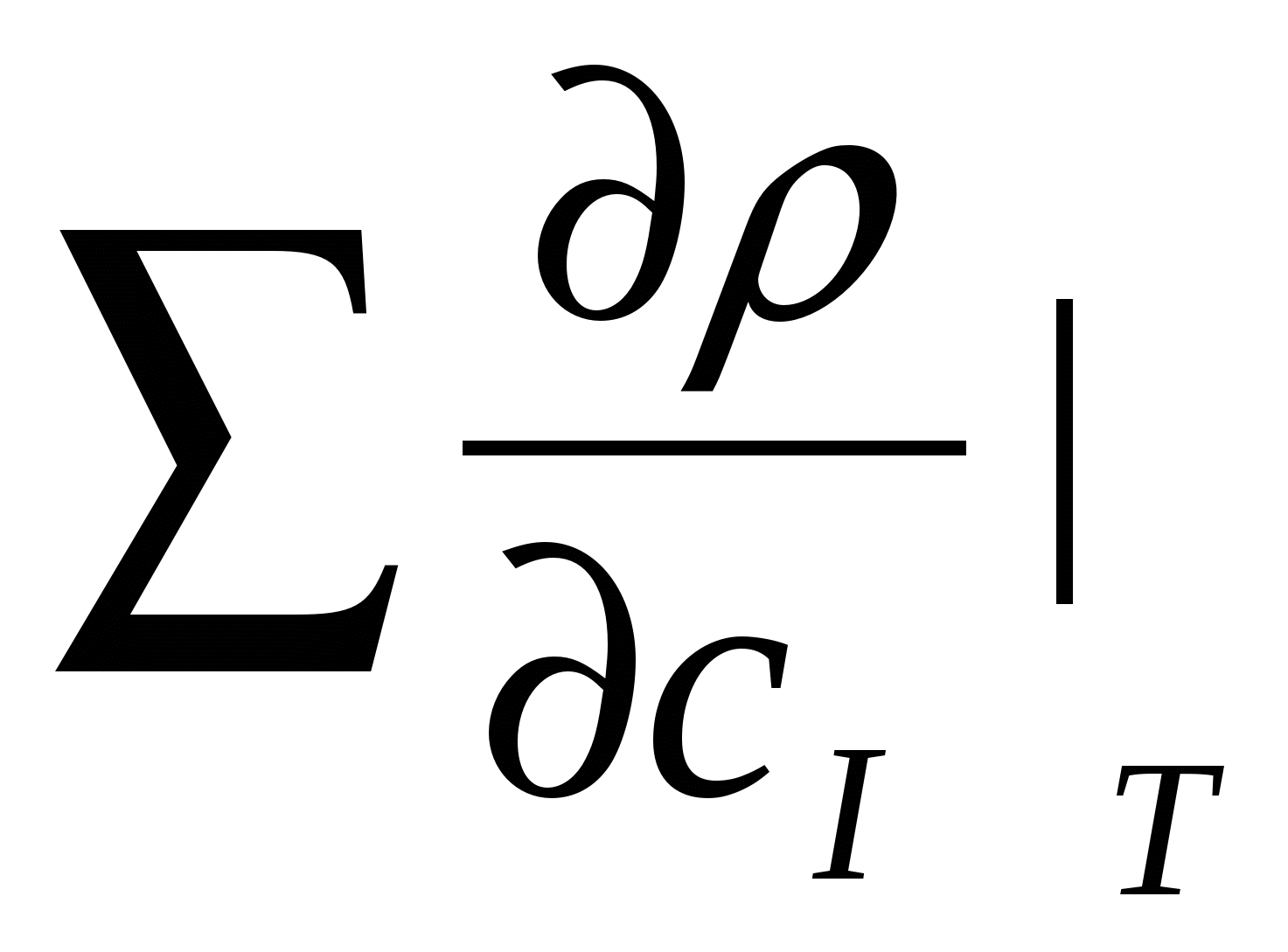 изменение плотности, вызываемое изменением состава среды, кг/кмоль;
изменение плотности, вызываемое изменением состава среды, кг/кмоль;
M = V - масса реакционной среды, кг;
MA - масса корпуса реактора, кг;
- плотность среды, кг/м3;
Т- температура в среде, К;
ΔНm - тепловой эффект химических процессов, Дж/моль;
Wm - скорость химических процессов, моль/с;
ΔНm - тепловой эффект массообменных процессов, Дж/моль;
Wm - скорость массообменных процессов, моль/с;
ТА - средняя температура корпуса реактора, К;
- коэффициент объёмного расширения, К-1;
Cр*- удельная теплоёмкость среды, Дж/(кг.К);
CA - удельная теплоёмкость материала корпуса реактора, Дж/(кг.К);
К- коэффициент теплопередачи, Вт/(м2К );
F - поверхность теплопередачи, м2;
Δ =
= 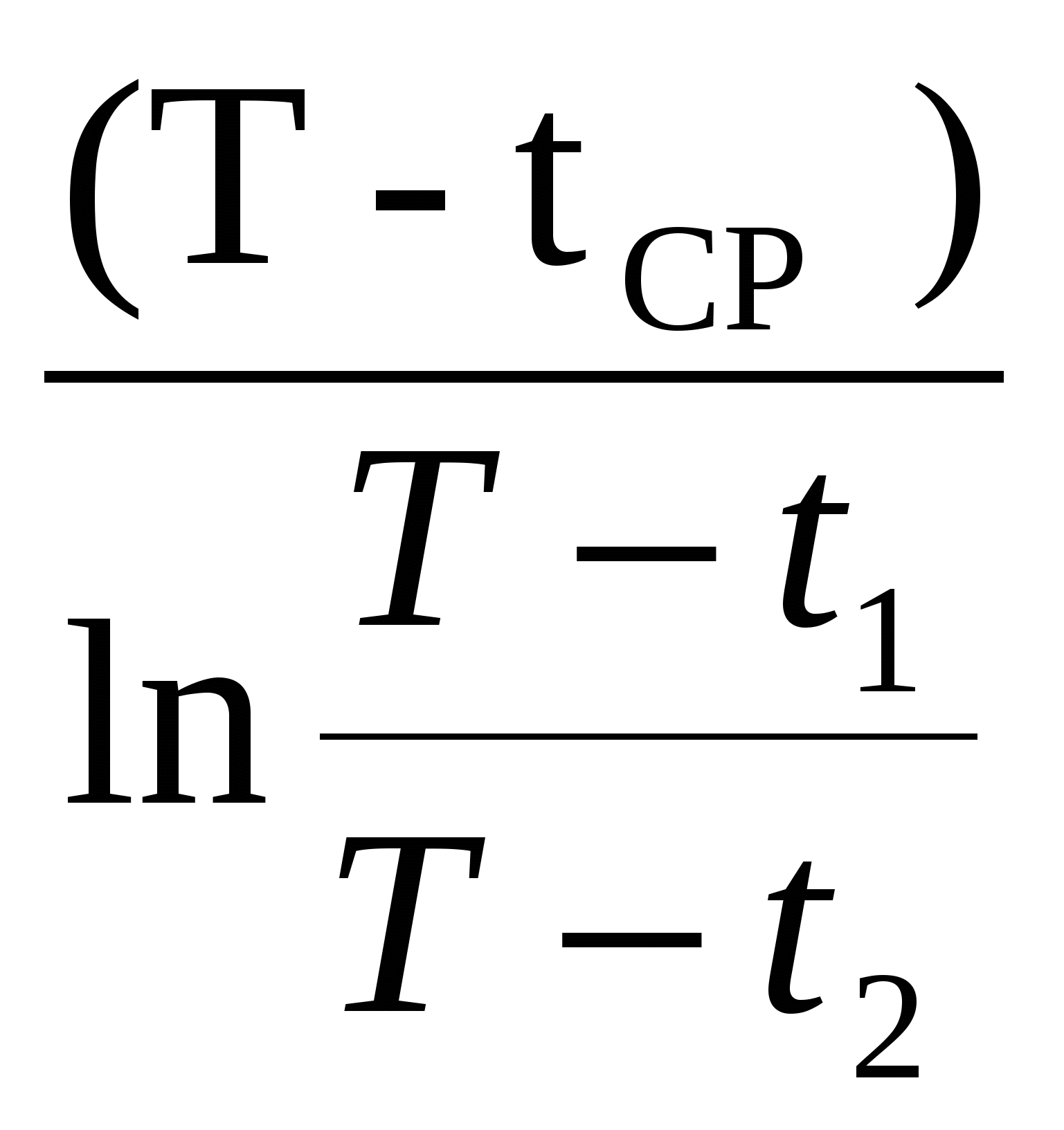 средняя разность температур, отсчитываемая от температуры среды, К; (18г)
средняя разность температур, отсчитываемая от температуры среды, К; (18г)
КП - коэффициент тепловых потерь, Вт/(м2К );
FП - поверхность тепловых потерь, м2;
T1, t2, tCP - начальная, конечная и средняя температура теплоносителя, К;
- температура окружающей среды.
Гидродинамика (течение среды определяется перемешиванием)
NЖ = КN n3 d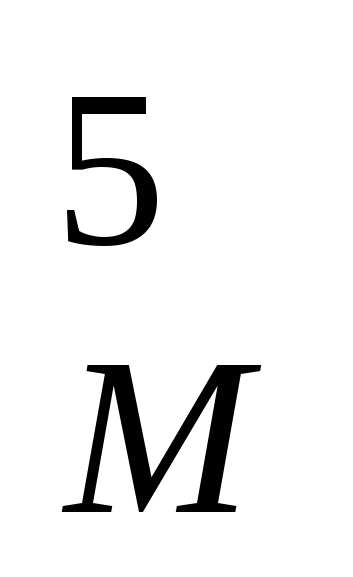 - мощность, диссипируемая (рассеиваемая мешалкой) в среде, Вт; (19а)
- мощность, диссипируемая (рассеиваемая мешалкой) в среде, Вт; (19а)
КN = F(Re; Fr; Г) - критерий мощности (критерий Эйлера для мешалок). (19б)
Интегрированием системы уравнений (18а)- (18г) получают зависимость концентраций и температур от времени; результаты представляют графически или в виде таблиц.
Рисунок Графическая зависимость
концентраций и температуры
Особую роль играют изотермические РИС-П, для которых
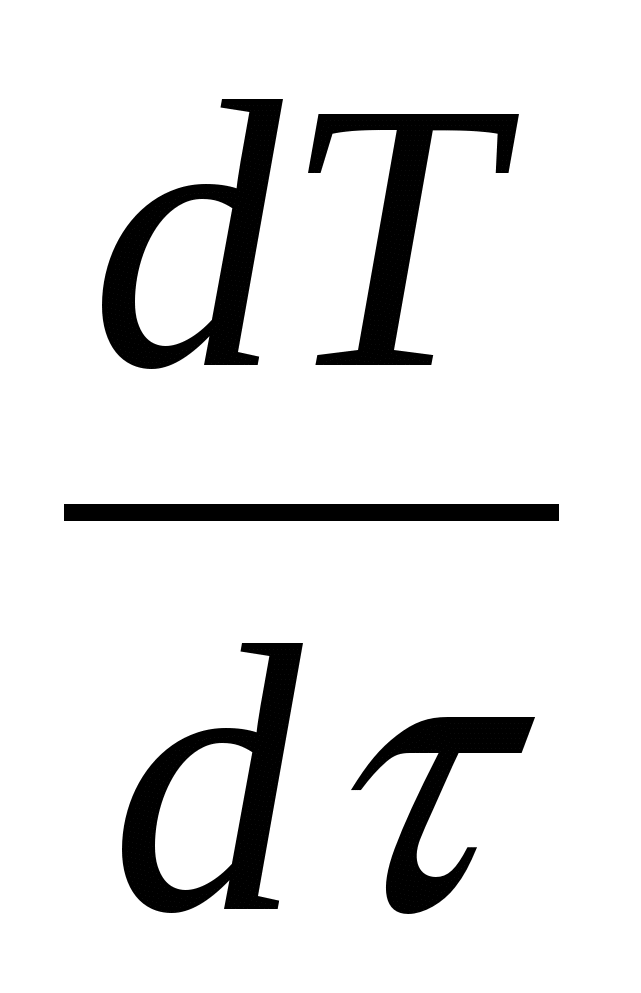 =0 (20а)
=0 (20а)
Постоянство температуры обеспечивается за счёт её регулирования
КF Δ = - ΔНR | WR | - КПFП(Т-) + NЖ (20б)
= - ΔНR | WR | - КПFП(Т-) + NЖ (20б)
Постоянство температуры исключает влияние объёмного расширения на концентрации веществ. Вследствие этого для И-РИС-П характеристическая система упрощается.
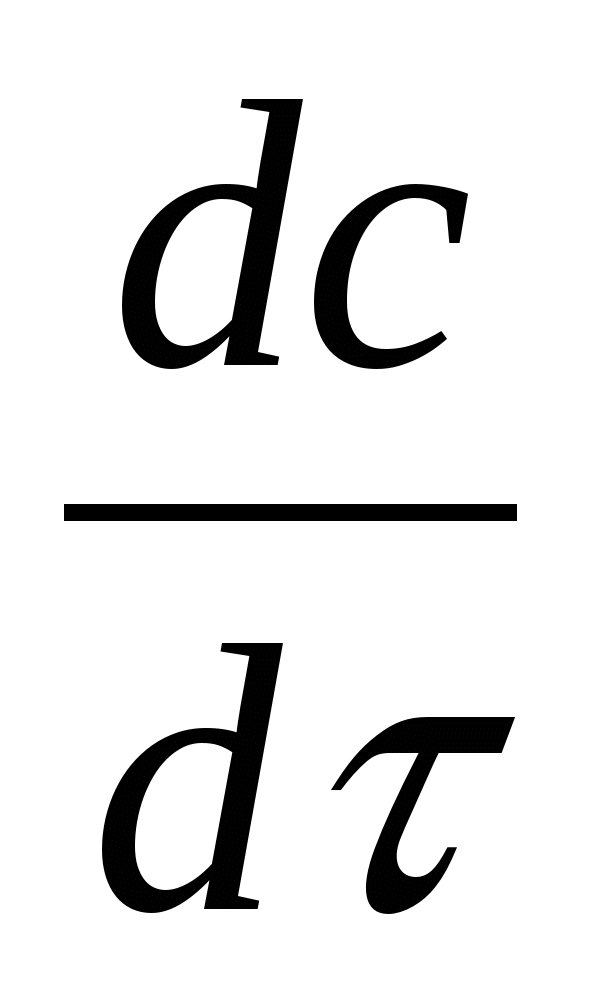 = WR (1+
= WR (1+![]() ) (20а)
) (20а)
Довольно часто влиянием состава среды на плотность - особенно в случае реакций в разбавленных растворах - можно пренебречь, т.е
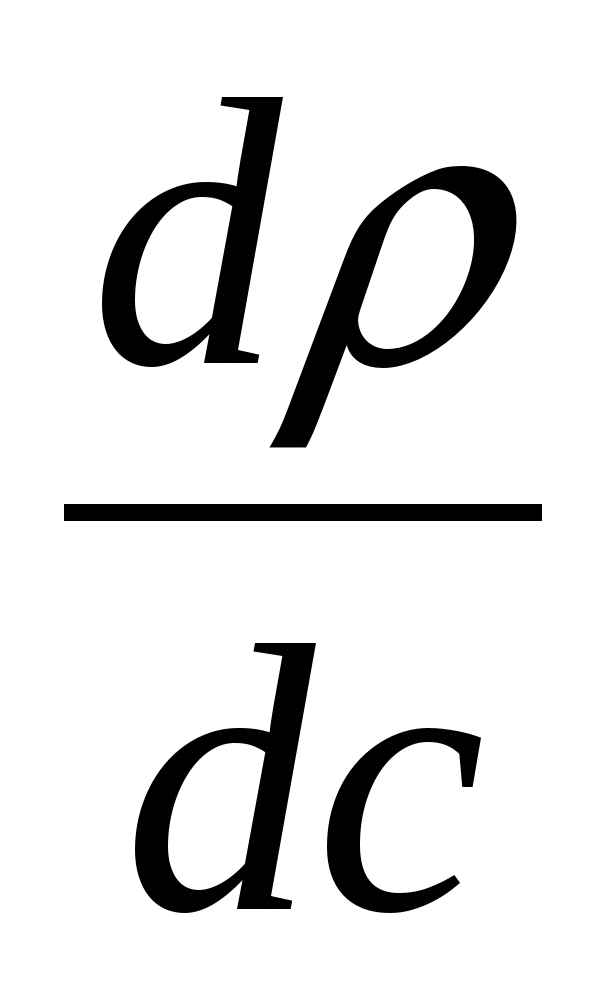 <<1 (20б)
<<1 (20б)
Тогда характеристическое уравнение упрощается
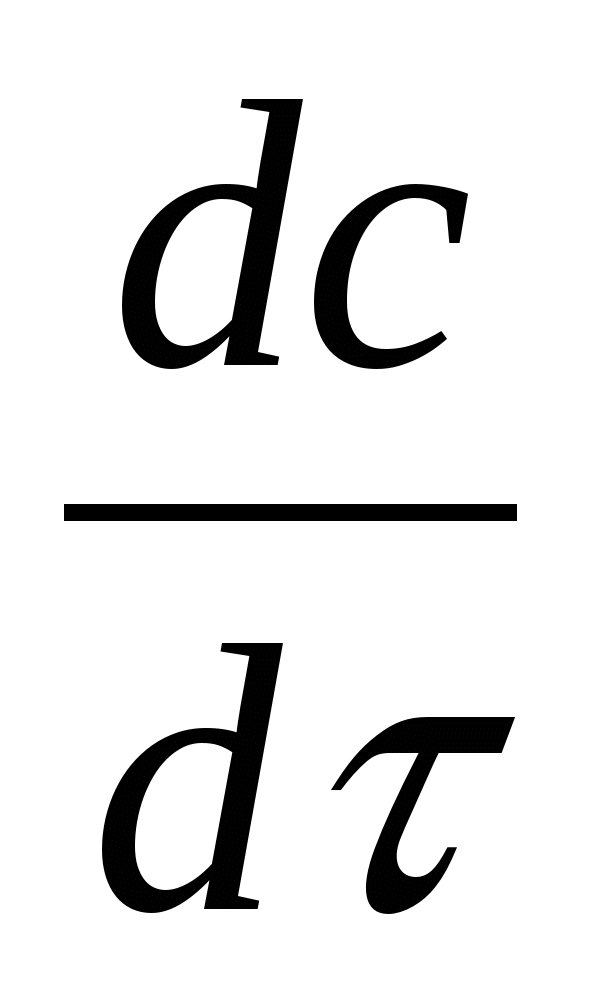 WR (20в)
WR (20в)
Уравнение (20в) имеет общее интегральное решение
= 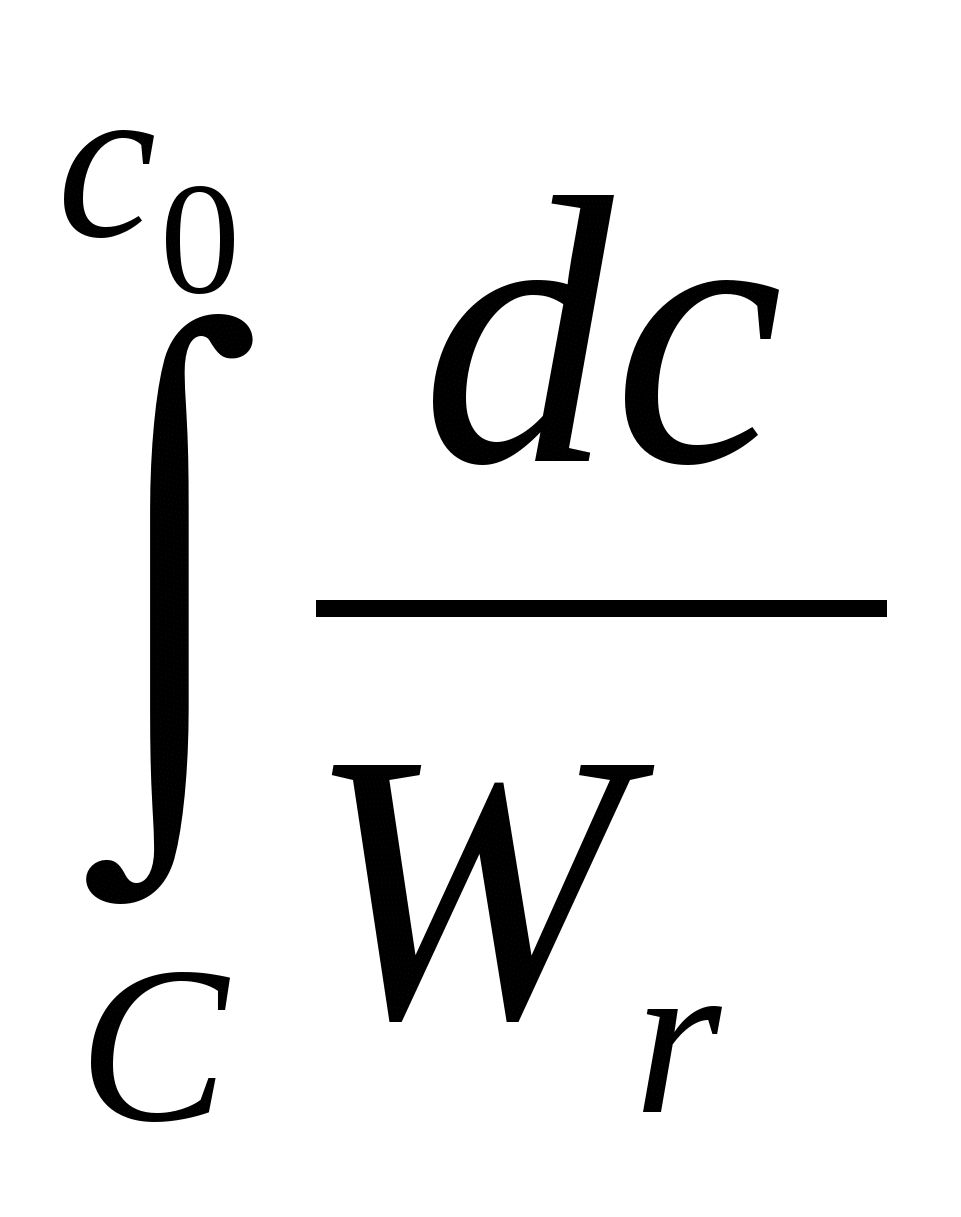 С0
С0 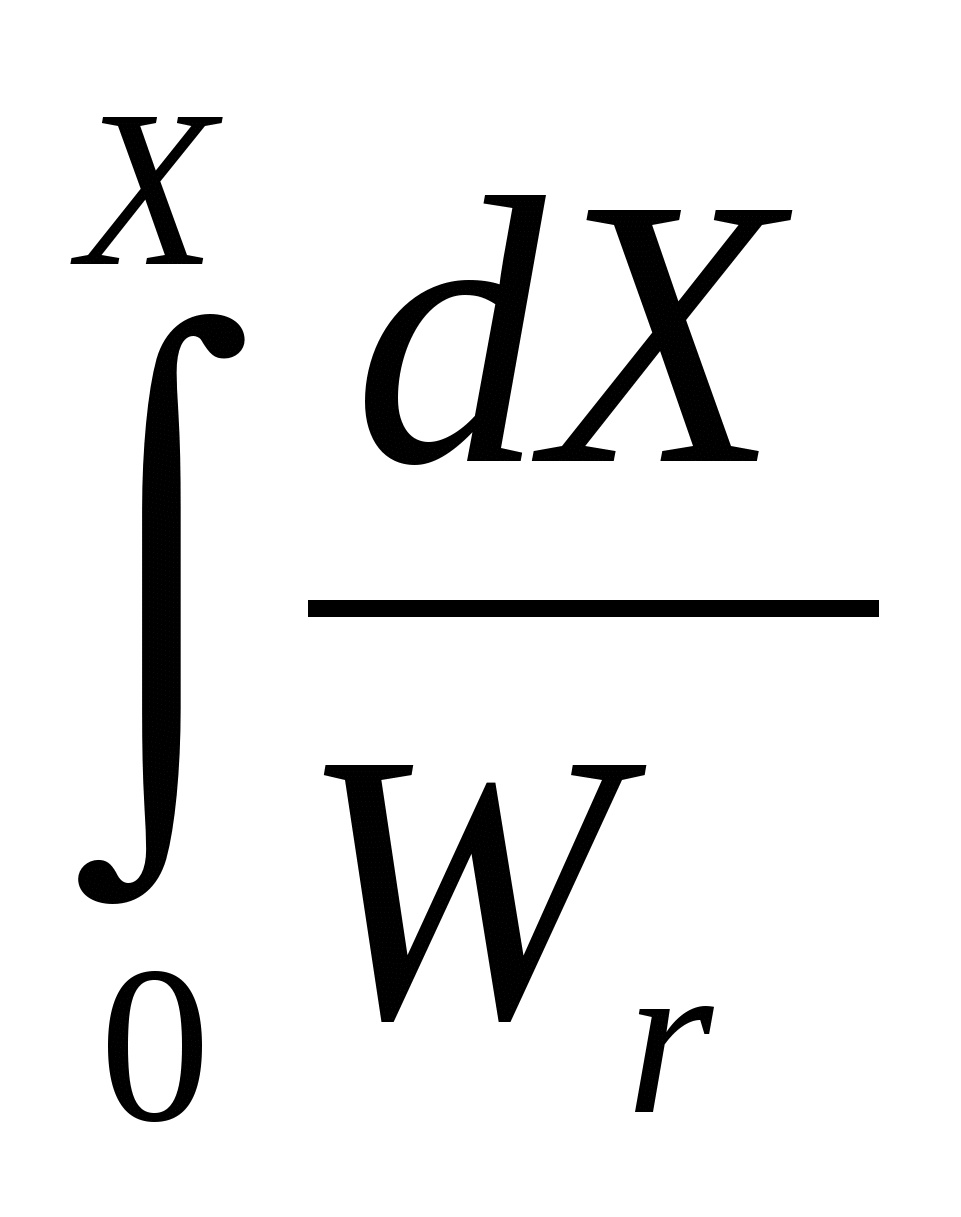 (21)
(21)
где Х -степень превращения.
Возможность практически обеспечить выполнение условий (19)-(21) [например, в разбавленных растворах] делает И-РИС-П чрезвычайно важными для кинетических исследований. По существу, это основной тип т.н. кинетических ячеек. Уравнения (20в) и (21) используют для вычисления кинетических параметров реакций.
Достоинство РИС-П в том, что этот тип режима характеризуется максимальной средней концентрацией реактантов в среде, т.е., максимальной движущей силой процесса. Поэтому время, необходимое для достижения заданной степени превращения при прочих равных условиях для РИС-П минимально из всех типов реакторов периодического действия.
Нужно отметить однако, что обеспечить возможность вести процессы в режиме РИС-П достаточно сложно. Как правило, тепловые эффекты химических и массообменных процессов приводят к тому, что при высоких концентрациях реактантов - и высоких скоростях процессов - очень трудно удержать температуру в реакторе в безопасных пределах; также трудно бывает предотвратить массовую лавинную кристаллизацию, выбросы реакционной массы и другие негативные явления. Кроме того, для сложных процессов с последовательно-параллельными реакциями максимальная концентрация не всегда позволяет достичь высокой селективности процесса и максимального выхода целевого продукта - что гораздо важнее высокой скорости процесса. Поэтому процессы РИС-П сравнительно редки в практике химической технологии БАВ.
Для поддержания безопасных и рациональных режимов ведения процессов, как правило, приходится ограничивать концентрации реактантов. Для этого необходимо загружать реагенты постепенно - в течение времени, сопоставимого с временем протекания процесса.
Кроме того, довольно часто из реактора необходимо отводить продукты, могущие вызвать побочные реакции, или сдвинуть равновесие в нежелательную сторону, или снизить температуру и тем самым замедлить процесс. Как правило, это делают отгонкой, экстракцией или кристаллизацией.
Реализация этих технологических приёмов формирует два основных режима ведения периодических процессов: - - реакторы полупериодического действия - РИС-ПП;
- реакторы полупериодически-непрерывного действия - РИС-ППН.
1.2 Реакторы полупериодического действия - РИС-ПП.
Эта модель применяется к периодическим процессам, при осуществлении которых часть реагентов изначально находится в реакторе, а другие загружают в течение времени, сопоставимого с временем протекания процесса. По окончании загрузки проводят выдержку, необходимую для достижения требуемого выхода целевого продукта. До окончания процесса продукты реакции из реактора не отводят. Поэтому все изменения концентраций и температуры обусловлены только происходящими в реакторе процессами.
Технологический цикл т.о. распадается на две фазы: дозирование и выдержка.
Рисунок . Схема РИС-ПП
Рассмотрим осуществляемую в РИС-ПП необратимую реакцию
A+ В D + E (III)
Будем считать, что раствор реагента В находится в реакторе, а раствор реагента А из мерника равномерно - т.е. с постоянным расходом - дозируют (сливают ) в реактор. Будем также считать, что изначально продукты реакции D и Е в среде отсутствуют
Математическое описание процесса в фазе дозирования.
Масса веществ
Унос отсутствует:= Gs =0
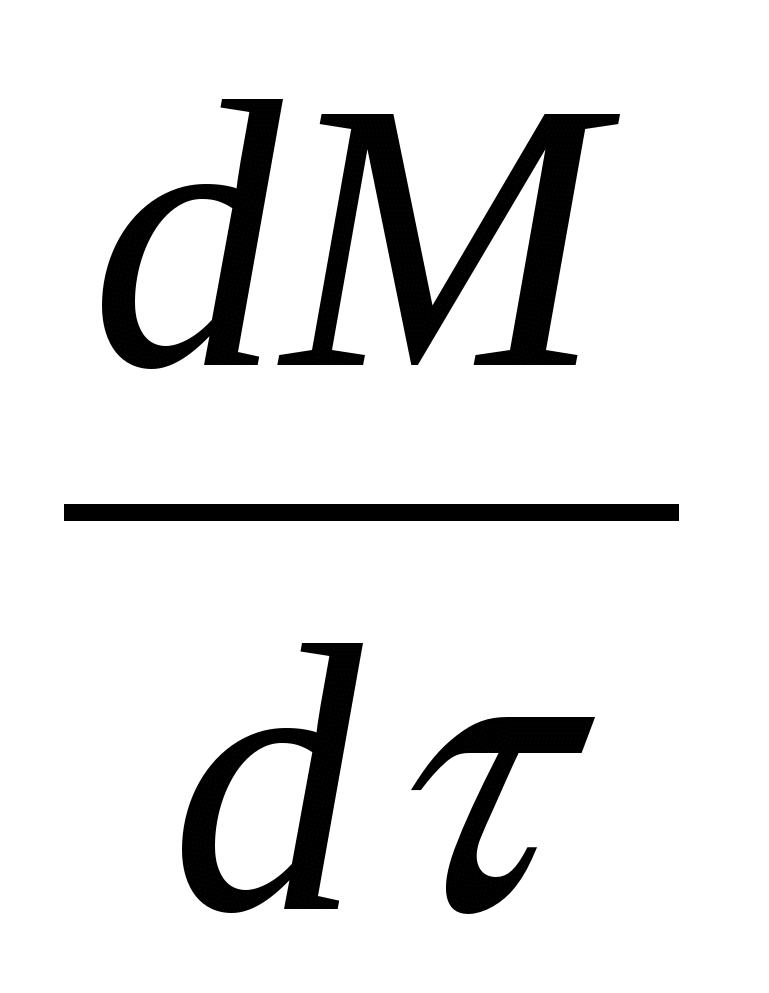 = GA=АVA (22а)
= GA=АVA (22а)
Объёмный и массовый расходы постоянны
GA=Const (22б)
VA =Const (22в)
Отсюда
М = МО + GA= МО + VA (22г)
Скорость реакции (макрокинетика процесса)
Концентрация А возрастает за счёт дозирования и убывает вследствие протекания реакции и увеличения объёма
реакционной среды
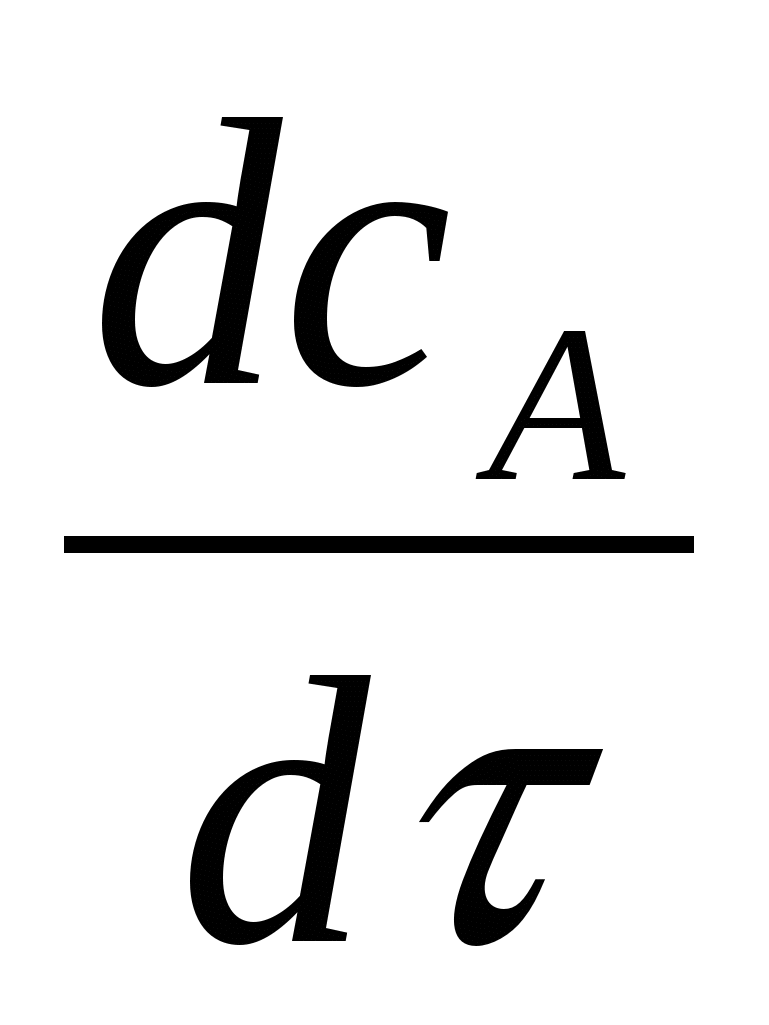 =
= 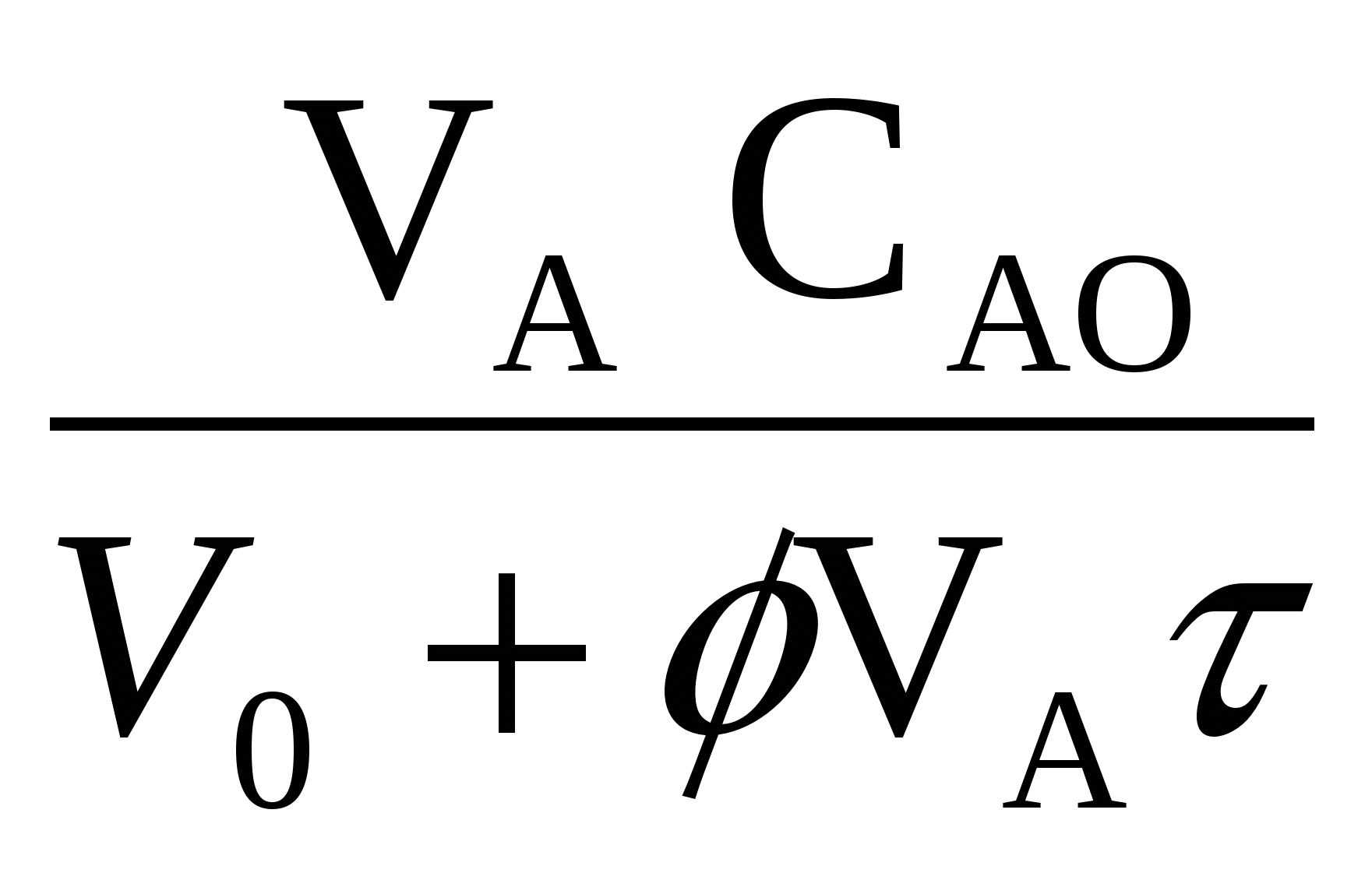 - WR (1-
- WR (1- ![]() ) - CА
) - CА![]() (23а)
(23а)
Концентрация В только убывает вследствие протекания реакции и увеличения объёма реакционной среды
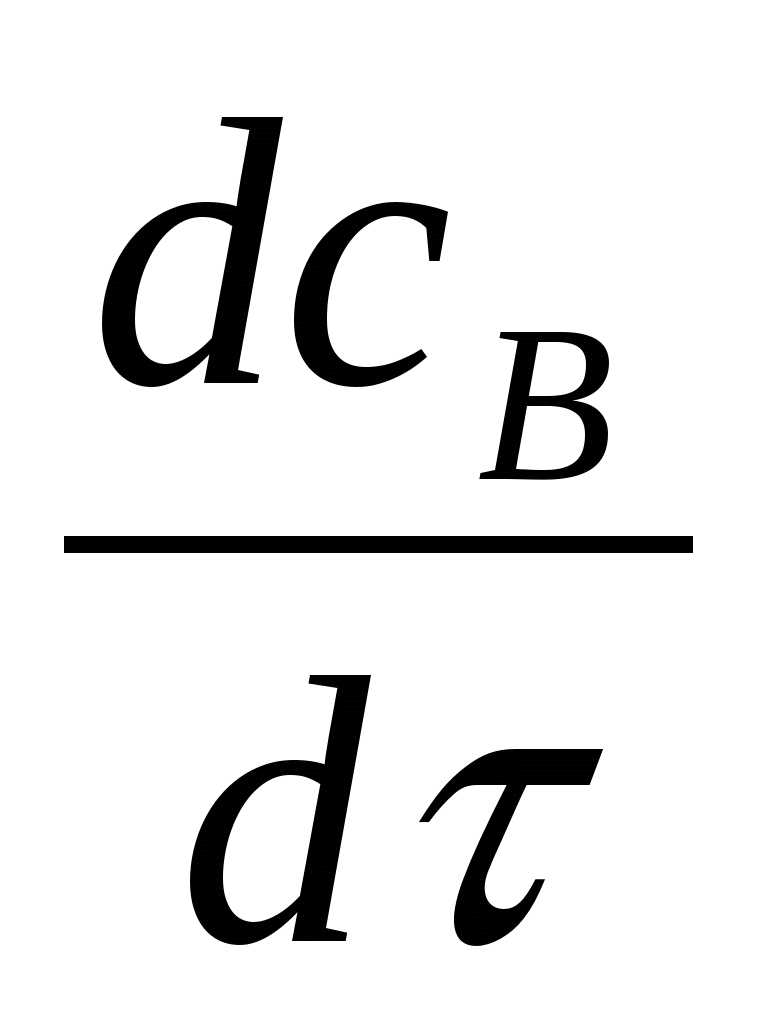 = -
= - 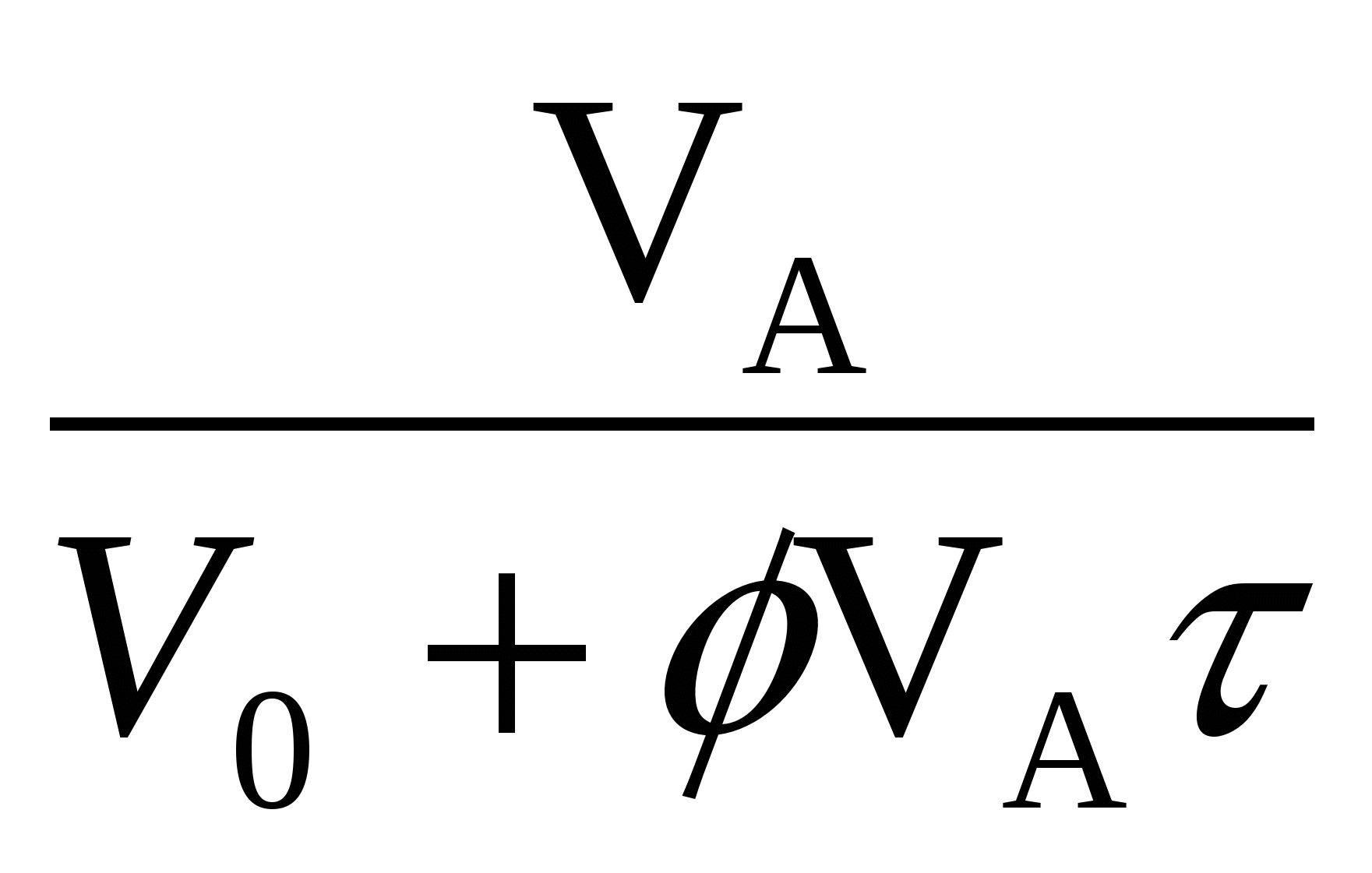 - WR (1-
- WR (1- ![]() ) - CВ
) - CВ![]() (23б)
(23б)
где - т.н. коэффициент контракции, отражающий отклонение объёма раствора от аддитивности.
Температура (дифференциальный тепловой баланс определяется тепловыми эффектами химических и массо-обменных процессов; энтальпией загружаемых продуктов; организованным теплообменом; мощностью диссипируе-
мой мешалкой и теплообменом с окружающей средой).
MCр*![]() + MACA
+ MACA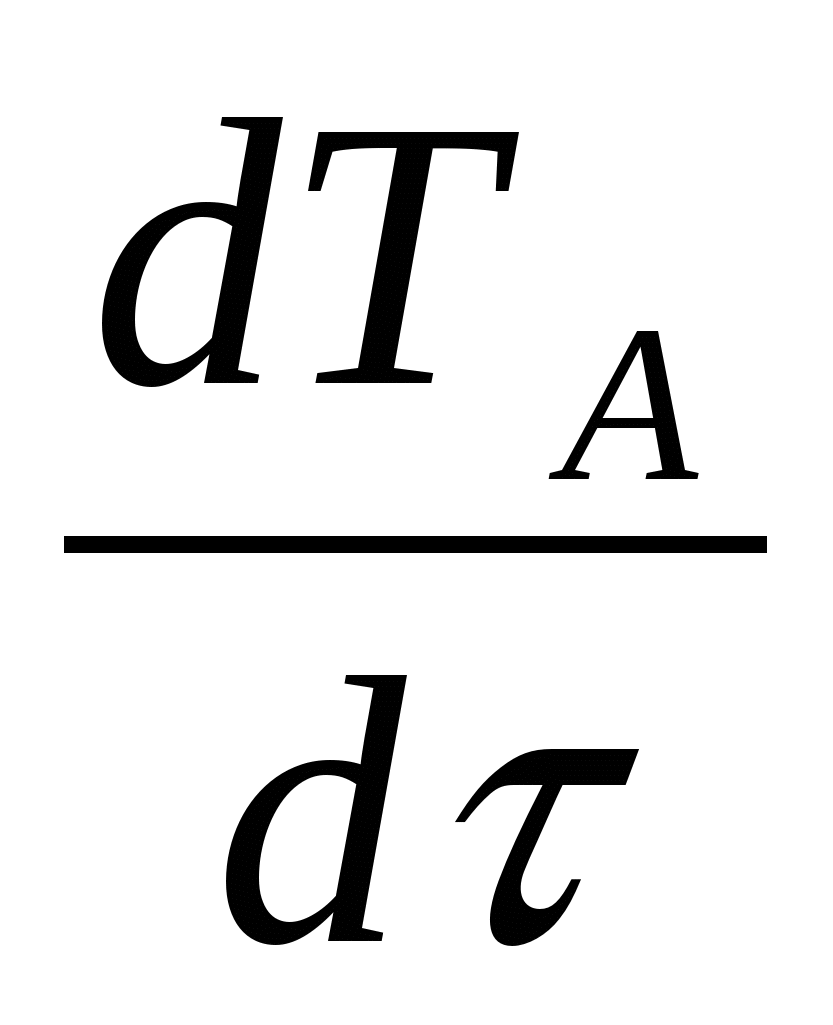 = GAH
= GAH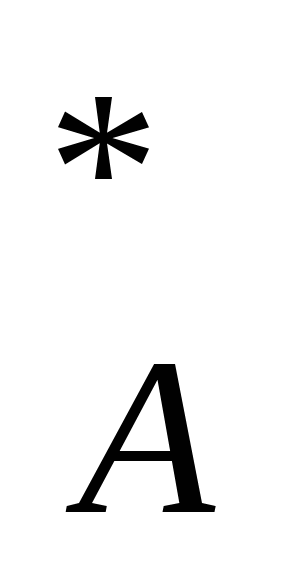 - (V0+VA ) {ΔНR | WR | - ΔНm | Wm | }-КF Δ
- (V0+VA ) {ΔНR | WR | - ΔНm | Wm | }-КF Δ - КПFП(Т-) + NЖ (23в)
- КПFП(Т-) + NЖ (23в)
Где H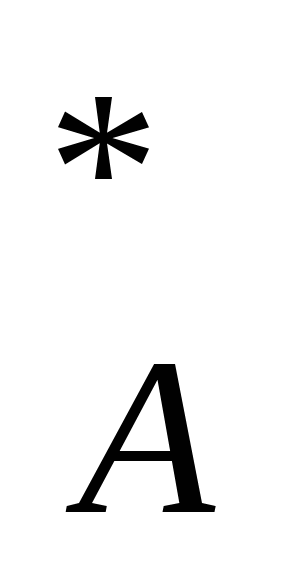 = mXIHIN - удельная энтальпия раствора реагента А, Дж/кг;
= mXIHIN - удельная энтальпия раствора реагента А, Дж/кг;
HIN- удельная энтальпия компонента I в растворе реагента А, Дж/кг;
mXI - массовая доля компонента I в растворе реагента А;
Гидродинамика (течение среды определяется перемешиванием)
NЖ = КN n3 d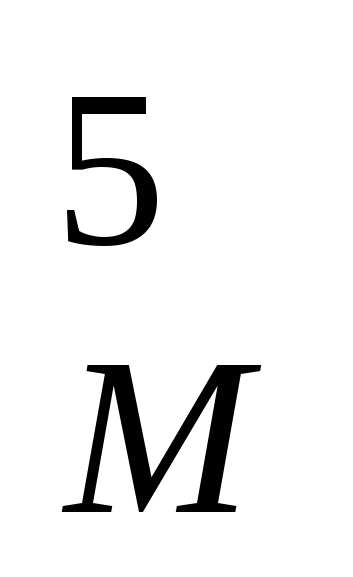 - мощность, диссипируемая (рассеиваемая мешалкой) в среде, Вт; (23г)
- мощность, диссипируемая (рассеиваемая мешалкой) в среде, Вт; (23г)
В фазе выдержки РИС-ПП идентичен РИС-П; процесс также описывется системой уравнений (18а)- (18г). Очевидно, что характеристическая система уравнений (23а)- (23г) весьма сложна; аналитические решения возможны только для реакций первого порядка и изотермических режимов.
Численное интегрирование системы уравнений (23а)- (23г) для фазы дозирования и системы уравнений (18а)- (18г) для фазы выдержки при задании различных условий ведения процесса (начальной температуры - Т0; расхода реагента А - GA; температуры теплоносителя - t0; температуры окружающей среды - ) получают зависимость концентраций и температур от времени; результаты представляют графически или в виде таблиц.
Рисунок Графическая зависимость концентраций и температуры для РИС-ПП
1.3 Реакторы полупериодически-непрерывного действия - РИС-ППН.
Эта модель применяется к любым периодическим процессам, при осуществлении которых часть реагентов изначально находится в реакторе, а другие загружают в течение времени, сопоставимого с временем протекания процесса. По окончании загрузки проводят выдержку, необходимую для достижения требуемого выхода целевого продукта. При этом как в фазе дозирования, так и в фазе выдержки часть продуктов реакции или избыток растворителя отводят из реактора.
Это наиболее сложный из всех режимов периодических процессов. Изменения концентраций и температуры обусловлены всей совокупностью происходящих в реакторе процессов. Для РИС-ППН не всегда даже возможно однозначно разделить цикл на фазы дозирования и выдержки.
Рисунок . Схема РИС-ППН
Рассмотрим осуществляемую в РИС-ППН необратимую реакцию
A+ В D + E (III)
Будем считать, что раствор реагента В находится в реакторе, а раствор реагента А из мерника равномерно - т.е. с постоянным расходом - дозируют (сливают ) в реактор. Будем также считать, что изначально продукты реакции D и Е в среде отсутствуют
Математическое описание процесса
Масса веществ
Gs =0
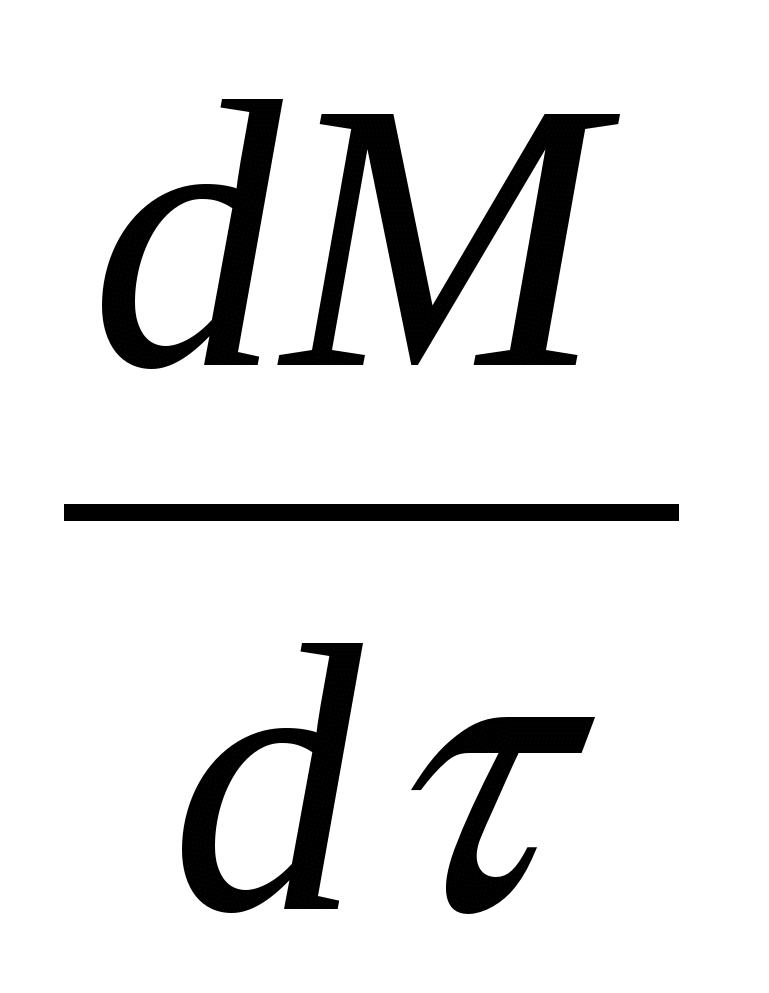 = GI - Gs = IVI - SVS (24а)
= GI - Gs = IVI - SVS (24а)
где М - масса веществ в аппарате, кг;
GI - суммарный массовый расход загружаемых веществ, кг/с;
Gs- суммарный массовый расход отводимых веществ, кг/с;
Объёмные и массовые расходы постоянны
{GI; Gs }=Const (24б)
{VI; Vs }=Const (24в)
Отсюда
М = МО + (GI- Gs)= МО + ( IVI - SVS) (24г)
Объём среды в аппарате
V= M/ (24д)
Скорость реакции (макрокинетика процесса)
Концентрация А возрастает за счёт дозирования и убывает вследствие протекания реакции, возможного уноса с отводимыми компонентами и увеличения объёма реакционной среды
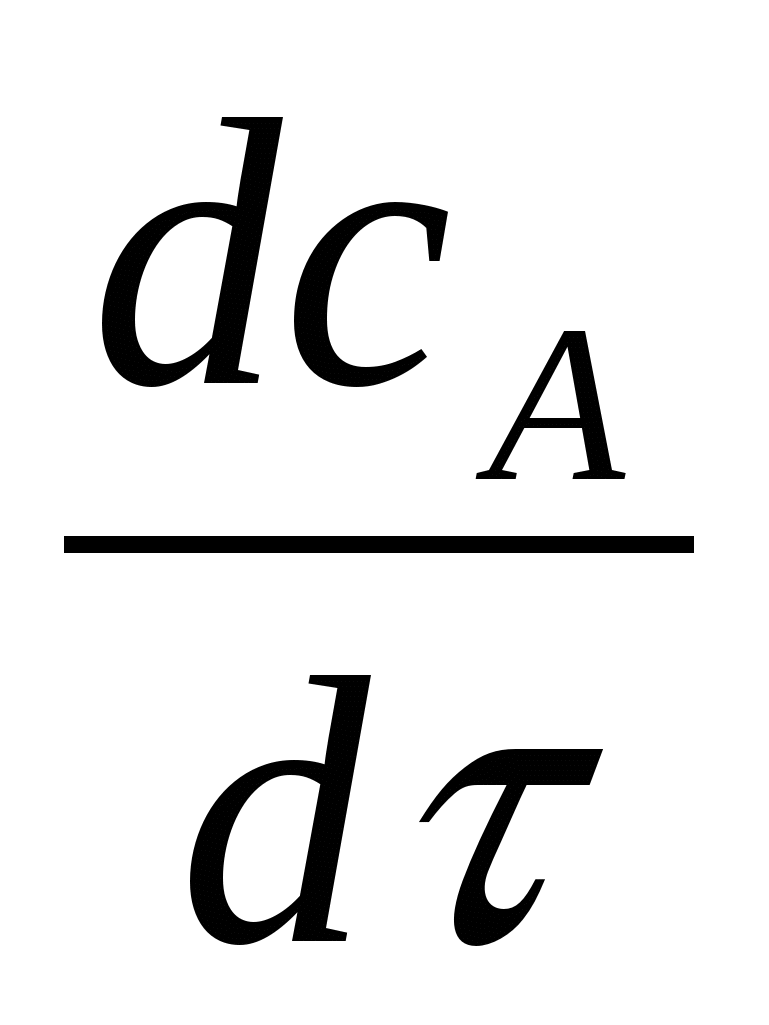 =
= 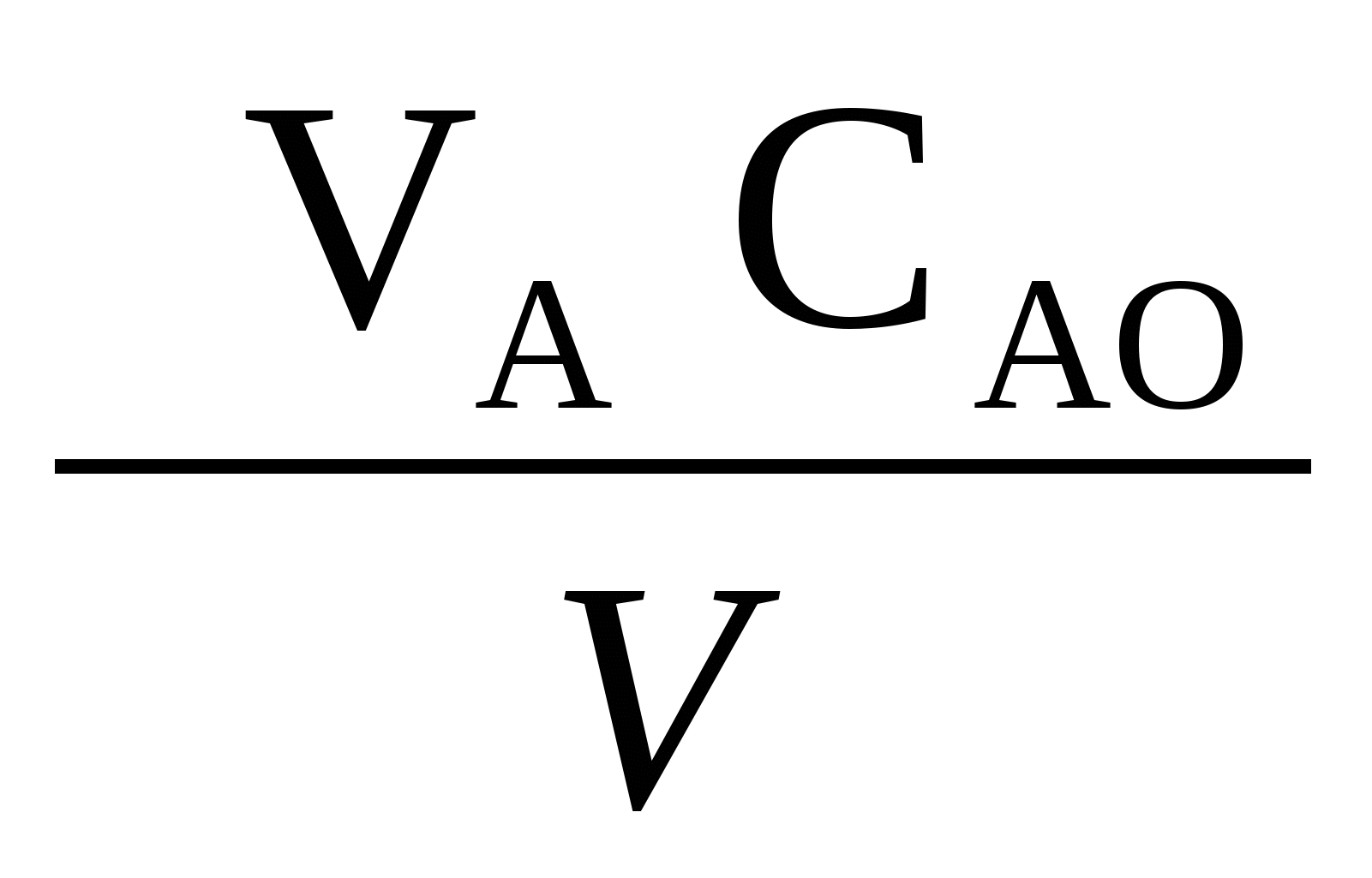 - WR (1-
- WR (1- ![]() ) - CА
) - CА![]() (24е)
(24е)
Концентрация В только убывает вследствие протекания реакции, возможного уноса с отводимыми компонентами и увеличения объёма реакционной среды
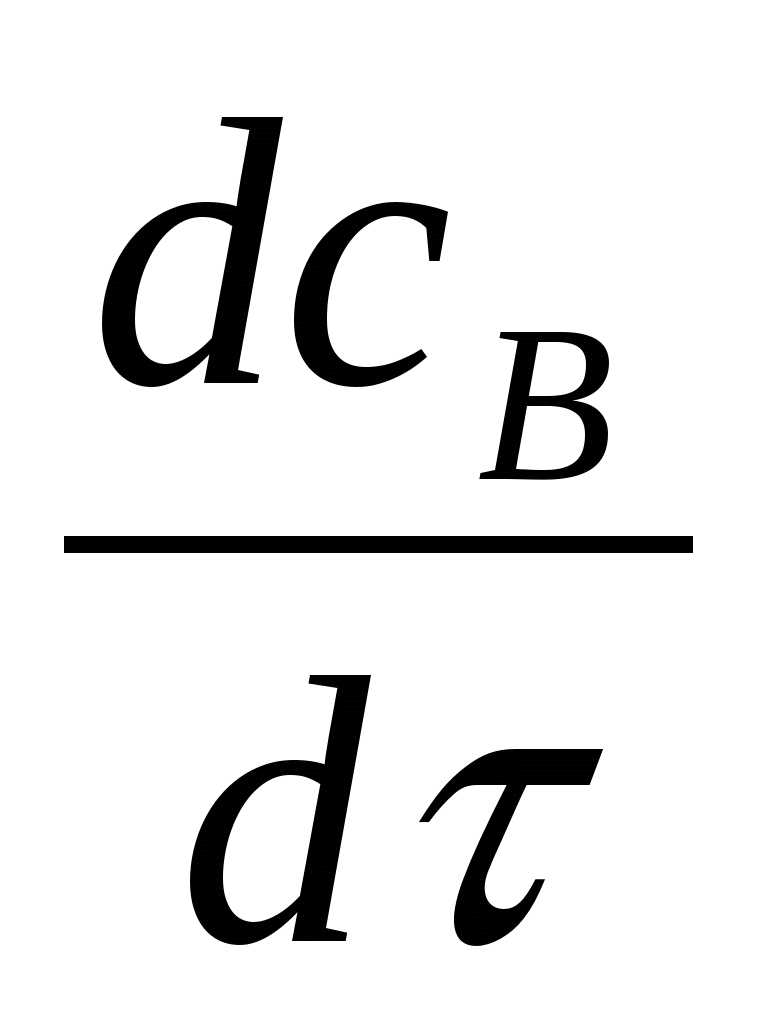 = -
= - 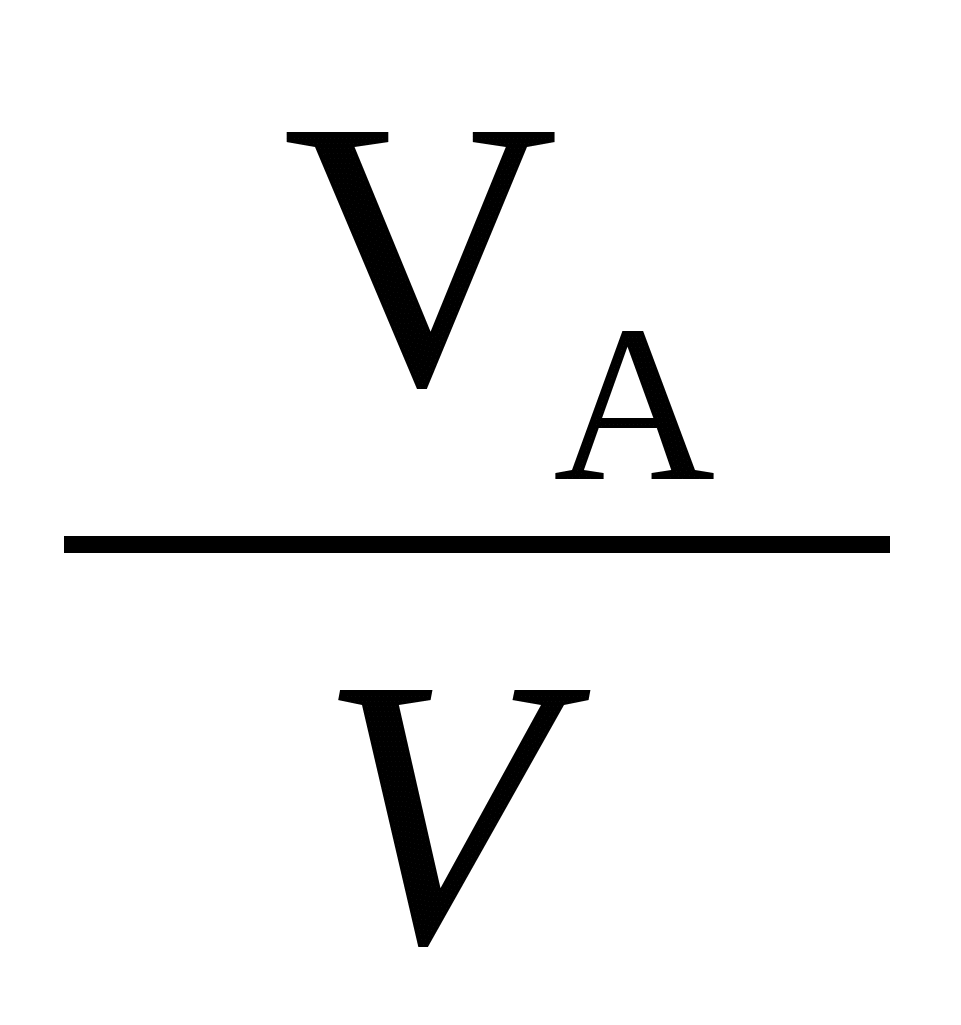 - WR (1-
- WR (1- ![]() ) - CВ
) - CВ![]() (24ж)
(24ж)
где - т.н. коэффициент контракции, отражающий отклонение объёма раствора от аддитивности.
Температура (дифференциальный тепловой баланс определяется тепловыми эффектами химических и массо-обменных процессов; энтальпией загружаемых и отводимых продуктов; организованным теплообменом; мощностью диссипируемой мешалкой и теплообменом с окружающей средой).
MCр*![]() + MACA
+ MACA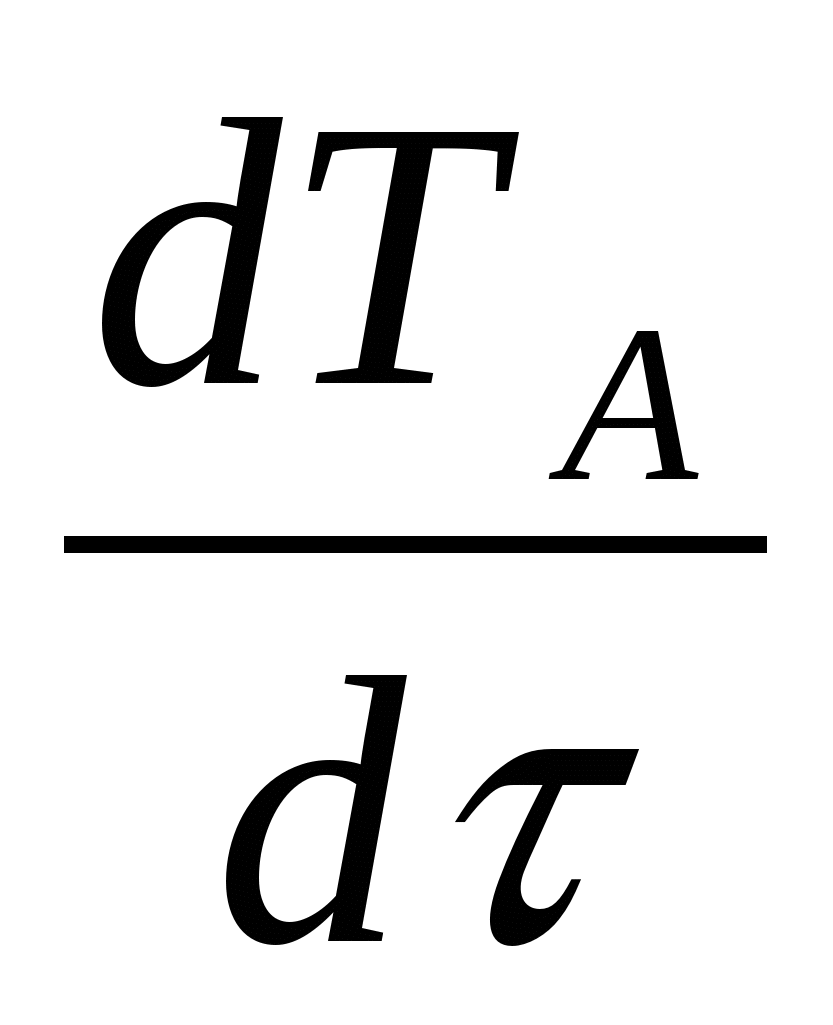 = GAH
= GAH![]() - GSH*S- V{ΔНR | WR | - ΔНm | Wm | }- КF Δ
- GSH*S- V{ΔНR | WR | - ΔНm | Wm | }- КF Δ - КПFП(Т-) +NЖ (24з)
- КПFП(Т-) +NЖ (24з)
Где HS*= mXIHIN - удельная энтальпия отводимого продукта S, Дж/кг;
Гидродинамика (течение среды определяется перемешиванием)
NЖ = КN n3 d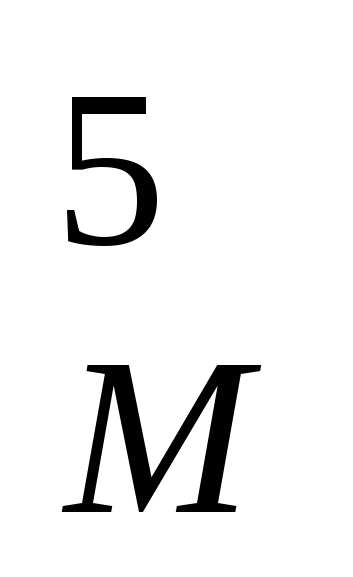 - мощность, диссипируемая (рассеиваемая мешалкой) в среде, Вт; (24и)
- мощность, диссипируемая (рассеиваемая мешалкой) в среде, Вт; (24и)
Численным интегрированием системы уравнений (24а)- (24и) при задании различных условий ведения процесса (начальной температуры - Т0; расхода реагента А - GA; температуры теплоносителя - t0; температуры окружающей среды - ) получают зависимость концентраций и температур от времени; результаты представляют графически или в виде таблиц.
На основании полученных результатов делают вывод о соответствии типов и технических характеристик реакторов задачам проекта и производят выбор рациональных условий ведения процесса.
Критерии выбора.
1. Параметры процесса: температура, давление, расходы сред - должны находиться в пределах норм безопасности.
2. Достигаемый выход целевого продукта должен высоким, а количество побочных продуктов, отходов и потерь - минимальным.
3. Расход энергоносителей и их параметры должны быть минимально достаточными для гарантии управления процессом.
4. Скорости изменения температуры и давления не должны превышать пределов быстродействия современных средств КИПСА (dT/d < 2 K/c; dP/d<1 Бар/с).
5. Трудоёмкость процесса должна быть минимальной.


